题目内容
17.实验室用NaClO3与Na2SO3制取ClO2气体,再由ClO2在强碱性条件下与过量的H2O2反应制得漂白剂NaClO2(装置如图1所示).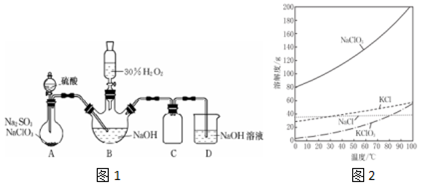
已知(如图2):(I)NaClO2饱和溶液在温度低于38℃时析出的晶体是NaClO3•3H2O,高于38℃时析出晶体是NaClO2;(Ⅱ)30% H2O2超过40℃时会完全分解;(Ⅲ)高于60℃时NaClO2分解成NaClO3和NaCl.
(1)图1装置A发生的反应中,还原剂是Na2SO3.
(2)图1装置B中反应生成NaClO2的化学方程式为2NaOH+2ClO2+H2O2=2NaClO2+2H2O+O2.
②实验中图1装置B需进行温度控制不超过40℃,在不改变NaOH溶液浓度和体积的条件下,可采取的措施有缓慢滴加硫酸、H2O2、装置B加冷水浴等.
(3)请补充从图1装置B反应后的溶液中获得NaClO2晶体的操作步骤.
①在55℃时蒸发结晶;②趁热(不低于38℃)过滤;③用38~60℃热水洗涤;④低于60℃干燥;得到成品.
(4)图1装置C的作用是防止D中的溶液倒吸到B瓶(或安全瓶)中.
(5)证明实验后图1装置B所得混合溶液中的NaClO2具有氧化性的实验方案是混合溶液加热至40℃至60℃之间除去H2O2,冷却后再加入FeCl2溶液与几滴KSCN溶液,溶液呈血红色,证明NaClO2具有氧化性.(可供选用的试剂:稀H2SO4、FeCl2溶液、KSCN溶液)
分析 装置A中用NaClO3与Na2SO3制取ClO2气体,发生反应:2NaClO3+Na2SO3+H2SO4=2ClO2↑+2Na2SO4+H2O,由ClO2在强碱性条件下与过量的H2O2在B装置中反应制得漂白剂NaClO2:2NaOH+2ClO2+H2O2=2NaClO2+2H2O+O2,C为安全瓶,防止倒吸,D装置由氢氧化钠溶液吸收未反应完的ClO2气体,防止污染空气,将B装置反应后的溶液在55℃时蒸发结晶,趁热(不低于38℃)过滤;用38~60℃热水洗涤;低于60℃干燥,得NaClO2晶体,据此分析解答.
解答 (1)A装置的反应为2NaClO3+Na2SO3+H2SO4=2ClO2↑+2Na2SO4+H2O,Na2SO3中硫元素化合价升高,被氧化,做还原剂;
故答案为:Na2SO3;
(2)①B装置为ClO2在强碱性条件下与过量的H2O2反应制得漂白剂NaClO2,化学方程式为:2NaOH+2ClO2+H2O2=2NaClO2+2H2O+O2;
故答案为:2NaOH+2ClO2+H2O2=2NaClO2+2H2O+O2;
②实验中图1装置B需进行温度控制不超过40℃,在不改变NaOH溶液浓度和体积的条件下,可采取的措施有缓慢滴加硫酸、H2O2、装置B加冷水浴等;
故答案为:缓慢滴加硫酸、H2O2、装置B加冷水浴等;
(3)已知:NaClO2饱和溶液在温度低于38℃时析出的晶体是NaClO3•3H2O,高于38℃时析出晶体是NaClO2,高于60℃时NaClO2分解成NaClO3和NaCl,从图1装置B反应后的溶液中获得NaClO2晶体的操作步骤为:在55℃时蒸发结晶,趁热(不低于38℃)过滤;用38~60℃热水洗涤;低于60℃干燥,得到成品;
故答案为:趁热(不低于38℃)过滤;用38~60℃热水洗涤;低于60℃干燥;
(4)C装置为安全瓶,防止D中的溶液倒吸到B瓶中;
故答案为:防止D中的溶液倒吸到B瓶(或安全瓶)中;
(5)装置B所得混合溶液中的NaClO2混有H2O2,验证NaClO2具有氧化性,需先将H2O2除去,再用亚铁离子检验,实验方案是:装置B所得混合溶液加热至40℃至60℃之间除去H2O2,冷却后再加入FeCl2溶液与几滴KSCN溶液,溶液呈血红色,证明NaClO2具有氧化性;
故答案为:混合溶液加热至40℃至60℃之间除去H2O2,冷却后再加入FeCl2溶液与几滴KSCN溶液,溶液呈血红色,证明NaClO2具有氧化性.
点评 本题考查物质的制备、对信息的利用、对装置的理解、氧化还原反应、实验设计等,理解反应原理,掌握实验基本操作是解题的关键,同时考查学生分析问题、解决问题的能力,难度较大.

| A. | 属于酯类的有4种 | |
| B. | 属于羧酸的有2种 | |
| C. | 存在有能使溴的四氯化碳溶液褪色的同分异构体 | |
| D. | 存在分子中含有五元环的酯类化合物 |
| A. | 只根据反应NH3(g)+HCl(g)═NH4Cl(s)在低温下能自发进行,不能判断出该反应△H的正负 | |
| B. | 对于反应N2(g)+3H2(g)$?_{催化剂}^{高温、高压}$2NH3(g),加入更多的催化剂会使平衡向正反应方向移动 | |
| C. | 向纯水中加入盐酸能使水的电离平衡逆向移动,但水的离子积不变 | |
| D. | 用惰性电极电解1 L 1 mol/L的CuSO4溶液,当阴极析出3.2 g铜时,加入0.05 mol Cu(OH)2固体可将溶液恢复至原浓度 |
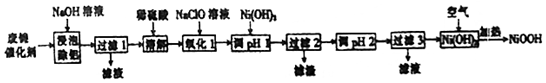
回答下列问题:
(1)“浸泡除铝”时,发生反应的化学方程式为2Al+2NaOH+2H2O═2NaAlO2+3H2↑.
(2)“溶解”时放出的气体为H2、H2S(填化学式).
(3)“氧化1”时,酸性条件下,溶液中的Fe2+被氧化为Fe3+,其离子方程式为ClO-+2Fe2++2H+=2Fe3++Cl-+2H2O.
(4)已知该条件下金属离子开始沉淀和完全沉淀的pH如表:
| 开始沉淀的pH | 完全沉淀的pH | |
| Ni2+ | 6.2 | 8.6 |
| Fe2+ | 7.6 | 9.1 |
| Fe3+ | 2.3 | 3.3 |
| Cr2+ | 4.5 | 5.6 |
(5)写出在空气中加热Ni(OH)2制取NiOOH的化学方程式4Ni(OH)2+O2$\frac{\underline{\;\;△\;\;}}{\;}$4NiOOH+2H2O.
(6)若加热不充分,则制得的NiOOH会混有Ni(OH)2,其组成可表示为xNiOOH•yNi(OH)2.现称取8.29gxNiOOH•yNi(OH)2样品溶于稀硫酸,搅拌至溶液清亮,定容至200mL,从中移取20.00mL,用0.010mol•L-1的,KMnO4标准溶液滴定,重复上述操作2次,平均消耗KMnO4标准溶液20.00mL.已知5Ni2++MnO4-+8H+═5Ni2++Mn2++4H2O,则x=8,y=1.
| A. | 甲酸(HCOOH)与正丁醇 | B. | 乙酸与甲醇(CH3OH) | ||
| C. | 乙醇与CH3CH2COOH | D. | CH3CH2COOH与甲醇(CH3OH) |
| A. | 通HCl(g) | B. | 加入少量KF(s) | C. | 加入少NaOH(s) | D. | 通入少量HF(g) |
| A. | 光催化还原水制氢比电解水制氢更节能环保、更经济 | |
| B. | 铁表面镀锌可增强其抗腐蚀性 | |
| C. | 用聚乙烯塑料代替聚乳酸塑料可减少白色污染 | |
| D. | 制饭勺、饭盒、高压锅等的不锈钢是合金 |
