题目内容
8.某有机物的分子式为C4H8O2,有关其同分异构体数目的说法错误的是( )| A. | 属于酯类的有4种 | |
| B. | 属于羧酸的有2种 | |
| C. | 存在有能使溴的四氯化碳溶液褪色的同分异构体 | |
| D. | 存在分子中含有五元环的酯类化合物 |
分析 A、C4H8O2属于酯类时,为饱和一元酯,根据酸和醇的种类来确定同分异构体;
B、C4H8O2属于羧酸时,可以根据羧基位置异构可以得到丁酸的同分异构体;
C、能与溴的四氯化碳溶液反应说明此分子含有碳碳双键;
D、根据分子的不饱和度确定.
解答 解:A、C4H8O2属于酯类时,为饱和一元酯,若为甲酸与丙醇形成的酯,甲酸只有1种结构,丙醇有2种,形成的酯有2种,若为乙酸与乙醇形成的酯,乙酸只有1种结构,乙醇只有1种结构,形成的乙酸乙酯有1种,若为丙酸与甲醇形成的酯,丙酸只有1种结构,甲醇只有1种结构,形成的丙酸甲酯只有1种,所以C4H8O2属于酯类的同分异构体共有4种,故A正确;
B、C4H8O2属于羧酸时,可以是丁酸或2-甲基丙酸,共有2种同分异构体,故B正确;
C、分子式为C4H8O2可以是不饱和二元醇,分子中存在碳碳双键,能使溴的四氯化碳溶液褪色,故C正确;
D、分子式为C4H8O2的不饱和度为1,五元环的酯类化合物的不饱和度为2,所以分子式为C4H8O2的同分异构体中不含有五元环的酯类化合物,故D错误;
故选D.
点评 本题考查同分异构体的判断,属于中等难度的试题,试题基础性强,侧重对酯类组成与结构的熟悉掌握程度,有利于培养学生的逻辑推理能力.

练习册系列答案
相关题目
18.某研究性学习小组为了变废为宝,用绿矾[FeSO4•7H2O]处理含铬(Cr2O72-)废水,反应中铁元素和铬元素完全转化为沉淀,该沉淀再处理得到磁性材料n molCrxFe1.5FeO4(Fe的化合价依次为+3、+2)(不考虑处理过程中的实际损耗),下列叙述错误的是( )
| A. | 处理废水中Cr2O72- 的物质量为$\frac{nx}{2}$mol | |
| B. | 消耗绿矾的物质量为n(2-x)mol | |
| C. | 反应中发生转移的电子数为3nx mol | |
| D. | 反应中Cr2O72-被还原 |
19.下列有机物发生的反应属于加成反应的是( )
| A. | 乙醇燃烧 | B. | 乙烯使溴的四氯化碳溶液褪色 | ||
| C. | 甲烷和氯气混合,见光 | D. | 用乙醇、乙酸与浓H2SO4混合加热 |
16.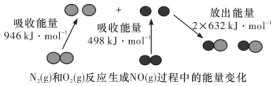 化学反应中的能量变化是由化学反应中旧化学键断裂时吸收的能量与新化学键形成时放出的能量不同引起的.如图为N2(g)和O2(g)反应生成NO(g)过程中的能量变化,下列说法中正确的是( )
化学反应中的能量变化是由化学反应中旧化学键断裂时吸收的能量与新化学键形成时放出的能量不同引起的.如图为N2(g)和O2(g)反应生成NO(g)过程中的能量变化,下列说法中正确的是( )
 化学反应中的能量变化是由化学反应中旧化学键断裂时吸收的能量与新化学键形成时放出的能量不同引起的.如图为N2(g)和O2(g)反应生成NO(g)过程中的能量变化,下列说法中正确的是( )
化学反应中的能量变化是由化学反应中旧化学键断裂时吸收的能量与新化学键形成时放出的能量不同引起的.如图为N2(g)和O2(g)反应生成NO(g)过程中的能量变化,下列说法中正确的是( )| A. | 1 mol N2(g)和1 mol O2(g)反应放出的能量为180 kJ | |
| B. | 1 mol N2(g)和1 mol O2(g)具有的总能量小于2 mol NO(g)具有的总能量 | |
| C. | 在1 L的容器中发生反应,10 min内 N2 减少了1 mol,因此10 min内的平均反应速率为v(NO)=0.1 mol/(L•min) | |
| D. | NO是一种酸性氧化物,能与NaOH溶液反应生成盐和水 |
3.标准状况下,将V L A气体(摩尔质量为Mg/mol)溶于0.1L水(密度1g/cm3)中,所得溶液的密度为dg/mL,则此溶液的物质的量浓度(mol/L)为( )
| A. | $\frac{Vd}{MN+2240}$ | B. | $\frac{1000Vd}{MN-2240}$ | C. | $\frac{1000VdM}{MN+2240}$ | D. | $\frac{MN}{22.4(V+0.1)d}$ |
13.下列物质中含有共价键的离子化合物的是( )
| A. | H2O | B. | CaCl2 | C. | KOH | D. | Cl2 |
20.把碎纸片b补充到a中,可得到一个完整的离子方程式(未配平).下列说法正确的是( )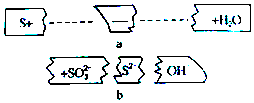

| A. | 氧化剂与还原剂的物质的量之比为2:1 | |
| B. | 该反应可能在酸性条件下进行 | |
| C. | 反应物微粒是S、SO32-、OH- | |
| D. | .2molS参加反应时,转移的电子数为$\frac{8}{3}$ NA |
11.能证明某溶液中含有Fe2+的是( )
| A. | 该溶液呈浅绿色 | |
| B. | 该溶液中加入NaOH溶液,生成白色沉淀 | |
| C. | 向该溶液中加入氯水,再滴入几滴KSCN溶液,呈红色 | |
| D. | 向该溶液中滴入几滴KSCN溶液,不变色,再加入氯水,呈红色 |