题目内容
11.下列有机反应中,不属于氧化还原反应的是( )| A. | 葡萄糖变为葡萄糖酸 | B. | 植物油变成硬化油 | ||
| C. | 蛋白质变为氨基酸 | D. | 油脂变质(酸败) |
分析 有元素化合价变化的反应为氧化还原反应,在有机反应中加H去氧的反应为还原反应,加O去H的反应为氧化反应,以此来解答.
解答 解:A.葡萄糖变为葡萄糖酸,发生氧化反应,故A不选;
B.植物油变成硬化油,植物油与氢气加成,发生还原反应,故B不选;
C.蛋白质变为氨基酸,蛋白质发生了水解反应,不是氧化原反应,故C选;
D.油脂变质(酸败)是油脂被氧化,是氧化原反应,故D不选;
故选C.
点评 本题考查氧化还原反应,明确反应中加H去氧为还原,加氧去氢为氧化即可解答,侧重有机反应类型的考查,题目难度不大.

练习册系列答案
相关题目
1.下列各组物质不属于同系物的是( )
| A. | 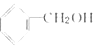 和 和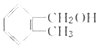 | B. | HOCH2-CH2OH和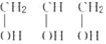 | C. | CH3CH2OH和 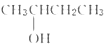 | D. | HOCH2CH2OH和 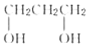 |
19.化学与生产、生活联系紧密,下列有关说法正确的是( )
| A. | 铵态氮肥和草木灰适宜混合使用 | |
| B. | 75%的酒精溶液可用作皮肤消毒剂 | |
| C. | SO2可用于漂白银耳 | |
| D. | 油脂和纤维素均可为人体提供能量. |
6.下列说法正确的是( )
| A. | 二氧化硫可用于杀菌、消毒 | |
| B. | 煤经过气化和液化等物理变化可转化为清洁能源 | |
| C. | 氯气和明矾均可做自来水的消毒剂 | |
| D. | 食品保鲜剂中所含铁粉和生石灰均作还原剂 |
2. 草酸(H2C2O4)是一种重要的有机化工原料.为探究草酸的制取和草酸的性质,进行如下实验.
草酸(H2C2O4)是一种重要的有机化工原料.为探究草酸的制取和草酸的性质,进行如下实验.
实验Ⅰ:实验室用硝酸氧化淀粉水解液法制备草酸,装置如图所示
①一定量的淀粉水解液加入三颈烧瓶中
②控制反应温度55-60℃,边搅拌边缓慢滴加一定量的混合酸(65%的HNO3与98%的H2SO4的质量比2:1.25)
③反应3小时,冷却,抽滤后再重结晶得到草酸晶体,硝酸氧化淀粉水解液的反应为:C6H12O6+12HNO3→3H2C2O4+9NO2↑+3NO↑+9H2O
(1)如图实验装置中仪器乙的名称为:冷凝管.装置B的作用是防C中液体倒吸进A中(安全瓶).
(2)检验淀粉是否水解完全的方法:取样,加碘水,看是否变蓝,变蓝则证明水解不完全,否则,水解完全.
实验Ⅱ:探究草酸与酸性高锰酸钾的反应
(3)向草酸溶液中逐滴加入硫酸酸化的高锰酸钾溶液时,可观察到溶液由紫红色变为近乎无色,写出上述反应的离子方程式:5H2C2O4+2MnO4-+6H+=10CO2↑+2Mn2++8H2O.
(4)学习小组的同学发现,当向草酸溶液中逐滴加入硫酸酸化的高锰酸钾溶液时,溶液褪色总是先慢后快.为探究其原因,同学们做了如下对比实验;
由此你认为溶液褪色总是先慢后快的原因是Mn2+起了催化剂的作用.
(5)草酸亚铁在工业中有重要作用,草酸可以制备草酸亚铁,步骤如下:
称取FeSO4•7H2O 固体于小烧杯中,加入水和少量稀H2SO4溶液酸化,加热溶解.向此溶液中加入一定量的H2C2O4溶液,将混合溶液加热至沸,不断搅拌,以免暴沸,待有黄色沉淀析出并沉淀后,静置.倾出上清液,再加入少量水,并加热,过滤,充分洗涤沉淀,过滤,用丙酮洗涤固体两次并晾干.
①生成的草酸亚铁需充分洗涤沉淀,检验是否洗涤完全的方法是取最后一次洗涤液1~2mL置于试管中,向其中滴加盐酸酸化的BaCl2溶液,若无白色沉淀产生,则表明已洗涤干净.
②用丙酮洗涤固体两次的目的是降低草酸亚铁的溶解量,同时更快洗去表面的水分.
 草酸(H2C2O4)是一种重要的有机化工原料.为探究草酸的制取和草酸的性质,进行如下实验.
草酸(H2C2O4)是一种重要的有机化工原料.为探究草酸的制取和草酸的性质,进行如下实验.实验Ⅰ:实验室用硝酸氧化淀粉水解液法制备草酸,装置如图所示
①一定量的淀粉水解液加入三颈烧瓶中
②控制反应温度55-60℃,边搅拌边缓慢滴加一定量的混合酸(65%的HNO3与98%的H2SO4的质量比2:1.25)
③反应3小时,冷却,抽滤后再重结晶得到草酸晶体,硝酸氧化淀粉水解液的反应为:C6H12O6+12HNO3→3H2C2O4+9NO2↑+3NO↑+9H2O
(1)如图实验装置中仪器乙的名称为:冷凝管.装置B的作用是防C中液体倒吸进A中(安全瓶).
(2)检验淀粉是否水解完全的方法:取样,加碘水,看是否变蓝,变蓝则证明水解不完全,否则,水解完全.
实验Ⅱ:探究草酸与酸性高锰酸钾的反应
(3)向草酸溶液中逐滴加入硫酸酸化的高锰酸钾溶液时,可观察到溶液由紫红色变为近乎无色,写出上述反应的离子方程式:5H2C2O4+2MnO4-+6H+=10CO2↑+2Mn2++8H2O.
(4)学习小组的同学发现,当向草酸溶液中逐滴加入硫酸酸化的高锰酸钾溶液时,溶液褪色总是先慢后快.为探究其原因,同学们做了如下对比实验;
| 实验序号 | H2C2O4(aq) | KMnO4(H+)(aq) | MnSO4(S) (g) | 褪色时间(S) | ||
| C(mol•L-1) | V(mL) | C(mol•L-1) | V(mL) | |||
| 实验1 | 0.1 | 2 | 0.01 | 4 | 0 | 30 |
| 实验2 | 0.1 | 2 | 0.01 | 4 | 5 | 4 |
(5)草酸亚铁在工业中有重要作用,草酸可以制备草酸亚铁,步骤如下:
称取FeSO4•7H2O 固体于小烧杯中,加入水和少量稀H2SO4溶液酸化,加热溶解.向此溶液中加入一定量的H2C2O4溶液,将混合溶液加热至沸,不断搅拌,以免暴沸,待有黄色沉淀析出并沉淀后,静置.倾出上清液,再加入少量水,并加热,过滤,充分洗涤沉淀,过滤,用丙酮洗涤固体两次并晾干.
①生成的草酸亚铁需充分洗涤沉淀,检验是否洗涤完全的方法是取最后一次洗涤液1~2mL置于试管中,向其中滴加盐酸酸化的BaCl2溶液,若无白色沉淀产生,则表明已洗涤干净.
②用丙酮洗涤固体两次的目的是降低草酸亚铁的溶解量,同时更快洗去表面的水分.
7.下列各化合物的命名中正确的是( )
| A. | H2C=CH-CH=CH2 1,3-二丁烯 | B. |  :间二甲苯 :间二甲苯 | ||
| C. |  2,6-二甲基-5-乙基庚烷 2,6-二甲基-5-乙基庚烷 | D. |  2-乙基-1-丁烯 2-乙基-1-丁烯 |

 三氯氧磷(POCl3)常温下为无色液体,有广泛应用,近年来,三氯氧磷的工业生产由三氧化磷的“氯气直接氧化法”代替传统的三氯化磷“氯化水解法”(由氯气、三氯化磷和水为原料反应得到).
三氯氧磷(POCl3)常温下为无色液体,有广泛应用,近年来,三氯氧磷的工业生产由三氧化磷的“氯气直接氧化法”代替传统的三氯化磷“氯化水解法”(由氯气、三氯化磷和水为原料反应得到). (4)间甲基苯甲醛 (5)CH2=CHCH2CH3(6)
(4)间甲基苯甲醛 (5)CH2=CHCH2CH3(6)