题目内容
9. 三氯氧磷(POCl3)常温下为无色液体,有广泛应用,近年来,三氯氧磷的工业生产由三氧化磷的“氯气直接氧化法”代替传统的三氯化磷“氯化水解法”(由氯气、三氯化磷和水为原料反应得到).
三氯氧磷(POCl3)常温下为无色液体,有广泛应用,近年来,三氯氧磷的工业生产由三氧化磷的“氯气直接氧化法”代替传统的三氯化磷“氯化水解法”(由氯气、三氯化磷和水为原料反应得到).(1)氧气直接氧化法生产三氯氧磷的化学方程式是2PCl3+O2=2POCl3,从原理上看,与氯化水解法比,其优点是原子利用率高或无副产物,对环境污染小等.
(2)氯化水解法生产三氯氧磷会产生含磷(主要为H3PO4、H3PO3等)废水,在废水中先国入适量漂白粉,再加入生石灰将磷元素转化为磷酸的钙盐沉淀并回收.
①漂白粉的主要作用是将H3PO3氧化为H3PO4;
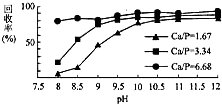
②如图表示不同条件对磷的沉淀回收率的影响(“Ca/”表示钙磷比,即溶液中Ca 2+与PO43-的浓度比).则回收时加入生石灰的目的是增大钙磷比和废水的pH,从而提高磷的回收.
(3)下述方法可以测定三氯氧磷产品中氯元素含量,实验步骤如下:
Ⅰ.先向一定量产品中加入足量NaOH溶液,使产品中的氯元素完全转化为Cl-
Ⅱ.用硝酸酸化后,加入过量的AgNO3溶液,使Cl-完全沉淀,记录AgNO3用量;
Ⅲ.再加入少量硝基苯并振荡,使其覆盖沉淀,避免沉淀与水溶液接触;
Ⅳ.最终加入几滴NH4Fe(SO4)2溶液后,用NH4SCN溶液沉淀中过量的Ag+,并记录NH4SCN的用量.
已知相同条件下的溶解度:AgSCN<AgCl
①步骤Ⅳ中当溶液颜色变为红色时,即表明溶液中Ag+恰好沉淀完全.
②若取消步骤Ⅲ,会使步骤Ⅳ中增加一个化学反应,该反应的离子方程式是AgCl+SCN-═AgSCN+Cl-;该反应使测定结果偏低,运用平衡原理解释其原因:AgCl在溶液中存在沉淀溶解平衡,加入NH4SCN溶液后,生成AgSCN沉淀使AgCl的溶解平衡向右移动,NH4SCN消耗量增大,由此计算出Ⅱ中消耗的Ag+的量减少.
分析 (1)依据题干要求,PCl3和O2反应生成三氯氧磷;因该反应无副产物,原子利用率高;
(2)①在该废水中加入漂白粉,可以将+3价的磷氧化为+5价;
②加入生石灰是为了增大钙磷比和废水的pH,有利于将磷元素转化为磷酸的钙盐沉淀,从而提高磷的回收率;
(3)①滴定完全时,Ag+全部生成AgSCN沉淀,过量的SCN-和Fe3+结合,溶液变为红色;
②因AgCl在溶液中存在平衡:AgCl(s)?Ag+(aq)+Cl-(aq),加入NH4SCN溶液时,AgCl会和SCN-结合,生成更难溶的AgSCN,平衡向右移动,导致NH4SCN消耗量增大.
解答 解:(1)依据题干要求,PCl3和O2反应生成三氯氧磷的方程式为:2PCl3+O2=2POCl3;因该反应无副产物,原子利用率高,且对环境污染小,故比氯化水解法要好;
故答案为:2PCl3+O2=2POCl3;原子利用率高或无副产物,对环境污染小等;
(2)①在该废水中加入漂白粉,可以将+3价的磷氧化为+5价;
故答案为:将H3PO3氧化为H3PO4;
②加入生石灰是为了增大钙磷比和废水的pH,有利于将磷元素转化为磷酸的钙盐沉淀,从而提高磷的回收率;
故答案为:增大钙磷比和废水的pH,从而提高磷的回收;
(3)①滴定完全时,Ag+全部生成AgSCN沉淀,过量的SCN-和Fe3+结合,溶液变为红色;
故答案为:红;
②因AgCl在溶液中存在平衡:AgCl(s)?Ag+(aq)+Cl-(aq),加入NH4SCN溶液时,AgCl会和SCN-结合,生成更难溶的AgSCN,即:AgCl+SCN-=AgSCN+Cl-生成AgSCN沉淀使AgCl的溶解平衡向右移动,导致NH4SCN消耗量增大;
故答案为:AgCl+SCN-═AgSCN+Cl-;AgCl在溶液中存在沉淀溶解平衡,加入NH4SCN溶液后,生成AgSCN沉淀使AgCl的溶解平衡向右移动,NH4SCN消耗量增大.
点评 本题考查了物质的制备方案设计,题目涉及化学方程式的书写、图象分析以及难溶电解质的溶度积常数的应用等,题目综合性较强,难度中等,侧重于考查学生的分析能力和对基础知识的综合应用能力.

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案| A. | 乙烯中 C=C 的键能是乙烷中 C-C 的键能的 2 倍 | |
| B. | 同一原子中,2p,3p,4p 能级的轨道数目依次增多 | |
| C. | C-O 键的极性比 N-O 键的极性大 | |
| D. | 根据能量最低原理,原子的核外电子排布先填满离核近的轨道,再填充离核远的轨道 |
| A. | 油脂的水解反应又叫皂化反应 | |
| B. | 分子式为C5H12O的醇类有5种结构 | |
| C. | 乙醇发生氧化反应生成乙酸,乙酸和乙醇发生取代反应生成乙酸乙酯 | |
| D. | 有机物甲的分子式为C3H6,则甲与乙烯(C2H4)互为同系物 |
| A. | 葡萄糖变为葡萄糖酸 | B. | 植物油变成硬化油 | ||
| C. | 蛋白质变为氨基酸 | D. | 油脂变质(酸败) |

若要求产品尽量不含杂质,而且生产成本较低,根据以下资料,填写空白:
已知:
1、25℃,Ksp[Fe(OH)3]=1.0×10-38,Ksp[Fe(OH)2]=8.0×10-16,
Ksp[Mg(OH)2]=1.8×10-11,Ksp[Mn(OH)2]=4.0×10-14.
2、Fe2+氢氧化物呈絮状,不易从溶液中除去,常将它氧化为Fe3+,生成Fe(OH)3沉淀除去.
3、原料价格表
| 物质 | 价格/元?吨-1 |
| 漂液(含25.2%NaClO) | 450 |
| 双氧水(含30%H2O2) | 2400 |
| 烧碱(含98%NaOH) | 2100 |
| 纯碱(含99.5%Na2CO3) | 600 |
明卤块中含铁离子,往另一份溶液中滴加酸性高锰酸钾溶液,若酸性高锰酸钾溶液褪色,则说明含亚铁离子.
(2)在步骤②中加入的试剂X,最佳的选择是漂液(NaClO),其作用是使溶液中Fe2+氧化成为Fe3+,便于除去.
(3)在步骤③中加入的试剂Y应是烧碱(NaOH),步骤⑥中发生的反应是Mg(OH)2$\frac{\underline{\;\;△\;\;}}{\;}$H2O+MgO.
(4)请写出氧化镁的一种用途:耐火材料、食品添加剂、抗酸剂、催化剂、制造镁盐的原料等,步骤⑥如在实验室进行,应选用在坩埚(填仪器名称)中灼烧.
(5)25℃,往卤块对应的水溶液中,加入一定量的烧碱达到沉淀溶液平衡,当pH=3,c(Fe3+)沉淀完全.测得pH=4.00,则此温度下残留在溶液中的c(Fe3+)=1×10-8mol/L.
| A. | 白酒 | B. | 纯碱溶液 | C. | 食盐溶液 | D. | 柠檬酸 |
| A. | 1mol任何物质都含有约6.02×1023个原子 | |
| B. | 气体摩尔体积在非标准状况下也有可能是22.4L/mol | |
| C. | 在使用摩尔表示物质的量的单位时,应用化学式指明粒子的种类 | |
| D. | 物质的量是国际单位制中七个基本物理量之一 |
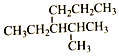 的命名正确的是( )
的命名正确的是( )| A. | 2-甲基-3-乙基己烷 | B. | 2-甲基-3-丙基戊烷 | ||
| C. | 3-异丙基己烷 | D. | 4-甲基-3-丙基戊烷 |
| 实验序号 | 甲 | 乙 | 丙 |
| 合金质量/mg | 255 | 385 | 459 |
| 生成气体体积/mL | 280 | 336 | 336 |
(1)要算出盐酸的物质的量浓度,题中作为计算依据的数据是乙或丙,求得的盐酸的物质的量浓度为1.5mol/L.
(2)求合金中Mg、Al的物质的量之比,题中可作为计算依据的数据是甲,求得的Mg、Al物质的量之比为1:1.