题目内容
钡在氧气中燃烧时的得到一种钡的氧化物晶体,起结构如图所示,有关说法正确的是( )

| A、该晶体属于离子晶体 |
| B、晶体的化学式为Ba2O2 |
| C、该晶体晶胞结构与CsCl相似 |
| D、与每个Ba2+距离相等且最近的Ba2+共有12个 |
考点:晶胞的计算
专题:化学键与晶体结构
分析:A.由阴阳离子构成的晶体为离子晶体,离子晶体中可能含有共价键;
B.该晶胞中Ba离子个数=8×
+6×
=4,过氧根离子个数=1+12×
=4,则钡离子和过氧根离子个数之比为4:4=1:1,据此确定化学式;
C.该晶胞中钡离子配位数是6,过氧根离子配位数是6,氯化铯中离子配位数是8,NaCl中离子配位数是6;
D.与每个Ba2+距离相等且最近的Ba2+个数=3×8×
.
B.该晶胞中Ba离子个数=8×
| 1 |
| 8 |
| 1 |
| 2 |
| 1 |
| 4 |
C.该晶胞中钡离子配位数是6,过氧根离子配位数是6,氯化铯中离子配位数是8,NaCl中离子配位数是6;
D.与每个Ba2+距离相等且最近的Ba2+个数=3×8×
| 1 |
| 2 |
解答:
解:A.该晶胞是由金属阳离子钡离子和阴离子过氧根离子构成的,为离子晶体,故A正确;
B.该晶胞中Ba离子个数=8×
+6×
=4,过氧根离子个数=1+12×
=4,则钡离子和过氧根离子个数之比为4:4=1:1,其化学式为BaO2,故B错误;
C.该晶胞中钡离子配位数是6,过氧根离子配位数是6,氯化铯中离子配位数是8,NaCl中离子配位数是6,该晶胞结构和氯化钠结构相似,故C错误;
D.与每个Ba2+距离相等且最近的Ba2+个数=3×8×
=12,故D正确;
故选AD.
B.该晶胞中Ba离子个数=8×
| 1 |
| 8 |
| 1 |
| 2 |
| 1 |
| 4 |
C.该晶胞中钡离子配位数是6,过氧根离子配位数是6,氯化铯中离子配位数是8,NaCl中离子配位数是6,该晶胞结构和氯化钠结构相似,故C错误;
D.与每个Ba2+距离相等且最近的Ba2+个数=3×8×
| 1 |
| 2 |
故选AD.
点评:本题考查晶胞计算,侧重考查分析、计算、空间想象能力,以教材中氯化钠、氯化铯为例采用知识迁移方法解答离子晶体晶胞有关计算,难点是配位数的计算方法.

练习册系列答案
相关题目
在2KMnO4+16HCl═2KCl+2MnCl2+5Cl2↑+8H2O反应中,氧化产物是( )
| A、KCl |
| B、MnCl2 |
| C、H2O |
| D、Cl2 |
设NA表示阿伏加德罗常数,下列说法不正确的是( )
| A、甲烷的摩尔质量与NA个甲烷分子的质量在数值上相等 |
| B、NA个氧气分子和NA个氢气分子的质量比等于16:1 |
| C、28 g氮气所含的原子数目为NA |
| D、17克NH3所含的原子数目为4NA,所含电子数目为10NA |
下列各化合物的命名不正确的是( )
| A、CH2═CH-CH═CH2 1,4-二丁烯 |
B、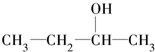 2-丁醇 2-丁醇 |
C、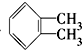 邻二甲苯 邻二甲苯 |
D、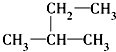 2-甲基丁烷 2-甲基丁烷 |
 某溶液中可能含有OH-,CO32-,AlO2-,SiO32-,SO42-,K+,Na+,Fe3+,Mg2+,Al3+等离子,当向溶液中逐滴加入一定物质的量的盐酸时,生成沉淀物质的量与加入盐酸体积的关系如图所示.下列判断正确的是( )
某溶液中可能含有OH-,CO32-,AlO2-,SiO32-,SO42-,K+,Na+,Fe3+,Mg2+,Al3+等离子,当向溶液中逐滴加入一定物质的量的盐酸时,生成沉淀物质的量与加入盐酸体积的关系如图所示.下列判断正确的是( )| A、原溶液中一定含有Na2SO4 |
| B、反应后形成的溶液溶质为NaCl |
| C、原溶液中含有CO32-与AlO2-的物质的量比为3:4 |
| D、原溶液中一定含有的离子是OH-,CO32-,SiO32-,AlO2-,K+ |

 如图是某化学学习小组用来探究钠与水反应的实验装置.该装置可以集反应、收集、检验气体于一体.图中钠块是用大头针叉住的.请填空:
如图是某化学学习小组用来探究钠与水反应的实验装置.该装置可以集反应、收集、检验气体于一体.图中钠块是用大头针叉住的.请填空: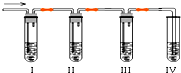 化学课外兴趣小组学生在实验室里制取的乙烯中常混有少量的二氧化硫,老师启发他们并由他们自己设计了下列实验图以确认上述混合气体中有C2H4和SO2.回答下列问题:
化学课外兴趣小组学生在实验室里制取的乙烯中常混有少量的二氧化硫,老师启发他们并由他们自己设计了下列实验图以确认上述混合气体中有C2H4和SO2.回答下列问题: