题目内容
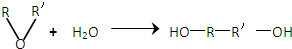
(1)在相同的条件下CO2、SO2在水中的溶解度较大的是 (写分子式),理由是 .
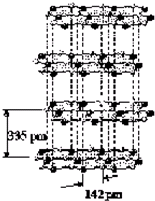
(2)AlN的晶体结构与晶体硅相似,在AlN晶体中,每个Al原子与 个N原子相连,与N元素同主族的元素As位于元素周期表的第一个长周期,其原子结构示意图为 .
(3)已知几种元素之间形成的化学键的键能如下:
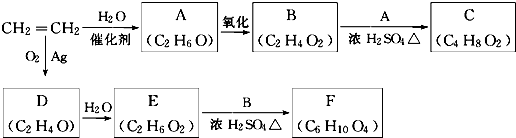
工业上用SiCl4在高温下与H2反应来得到高纯度的晶体Si,请写出该反应的热化学方程式: .
(2)AlN的晶体结构与晶体硅相似,在AlN晶体中,每个Al原子与
(3)已知几种元素之间形成的化学键的键能如下:
| 化学键 | H-H | H-Cl | C-Si | Si-Si | Si-Cl |
| 键能(kJ/mol) | 436 | 431 | 347 | 176 | 360 |
考点:不同晶体的结构微粒及微粒间作用力的区别,热化学方程式
专题:化学反应中的能量变化,化学键与晶体结构
分析:(1)水是极性分子,根据相似相溶原理判断;
(2)AlN的晶体结构与晶体硅相似,根据硅的晶体结构分析;As核外有33个电子,分4层排布,最外层5个;
(3)△H=反应物的总键能-生成物的总键能,再写出反应的热化学方程式.
(2)AlN的晶体结构与晶体硅相似,根据硅的晶体结构分析;As核外有33个电子,分4层排布,最外层5个;
(3)△H=反应物的总键能-生成物的总键能,再写出反应的热化学方程式.
解答:
解:(1)在相同的条件下CO2、SO2在水中的溶解度较大的是,SO2;SO2是极性分子,CO2是非极性分子,水是极性分子,根据相似相溶原理:极性分子易溶于极性溶剂中,所以SO2在水中的溶解度比CO2的大;
故答案为:SO2;SO2是极性分子,CO2是非极性分子,水是极性分子,根据相似相溶原理,SO2在水中的溶解度比CO2的大;
(2)AlN的晶体结构与晶体硅相似,硅的晶体为空间网状结构,每个硅原子形成4个共价键,则AlN的晶体中每个Al原子与4个N原子相连;As核外有33个电子,分4层排布,最外层5个,其电子排布式为: ;
;
故答案为:4; ;
;
(3)△H=反应物的总键能-生成物的总键能=360×4+436×2-176×2-431×4=236kJ/mol,
则SiCl4(g)+2H2(g)=Si(s)+4HCl(g)△H=+236kJ/mol;
故答案为:SiCl4(g)+2H2(g)=Si(s)+4HCl(g)△H=+236kJ/mol.
故答案为:SO2;SO2是极性分子,CO2是非极性分子,水是极性分子,根据相似相溶原理,SO2在水中的溶解度比CO2的大;
(2)AlN的晶体结构与晶体硅相似,硅的晶体为空间网状结构,每个硅原子形成4个共价键,则AlN的晶体中每个Al原子与4个N原子相连;As核外有33个电子,分4层排布,最外层5个,其电子排布式为:
 ;
;故答案为:4;
 ;
;(3)△H=反应物的总键能-生成物的总键能=360×4+436×2-176×2-431×4=236kJ/mol,
则SiCl4(g)+2H2(g)=Si(s)+4HCl(g)△H=+236kJ/mol;
故答案为:SiCl4(g)+2H2(g)=Si(s)+4HCl(g)△H=+236kJ/mol.
点评:本题考查了相似相溶原理、晶体结构、原子结构示意图、反应热的计算和热化学方程式的书写,题目涉及的知识点较多,侧重于基础知识的应用的考查,题目难度中等.

练习册系列答案
相关题目
下列说法不正确的是( )
| A、生铁、不锈钢和黄金都属于合金 |
| B、水泥、玻璃、陶瓷均属于无机非金属材料 |
| C、淀粉、油脂、蛋白质都属于天然高分子化合物 |
| D、天然气、石油液化气和汽油的主要成分都属于烃类 |
一些微生物在代谢过程中会产生硫化物.科学家设计出利用一种菌种生成的硫化物,与氧气构成微生物燃料电池,电解质溶液呈酸性.下列关于该电池的说法不正确的是( )
| A、将化学能转化为电能电池 |
| B、放电时,H+向正极移动 |
| C、正极反应式为:O2+2H2O+4e-═4OH- |
| D、负极反应式可能为:S2-+4H2O-8e-═SO42-+8H+ |
短周期元素W、X、Y的原子序数依次增大,其中W的阴离子的核外电子数与X、Y、原子的核外内层电子数相同.X的一种核素在考古时常用来鉴定一些文物的年代,工业上采用液态空气分馏方法来生产Y的单质.根据以上叙述,下列说法中一定正确的是( )
| A、上述四种元素的原子半径大小为Y<X<W |
| B、W、X、Y原子的核外最外层电子数的总和为10 |
| C、由W与X组成的化合物的沸点总低于由W与Y组成的化合物的沸点 |
| D、W与Y可形成既含极性共价键又含非极性共价键的化合物 |
用NA表示阿伏加德罗常数的值.下列叙述中,正确的是( )
| A、在NA个NO2分子与水的反应中,转移电子数为2NA |
| B、0.1NA个Cu与含0.2mol溶质的浓硫酸共热,被还原的硫酸为0.1mol |
| C、19.2gCu与足量稀硝酸反应,生成0.2NA个NO分子 |
| D、标准状况下11.2LNH3溶解于1000 mL水中,所得溶液的物质的量浓度为0.5 mol?L-1 |
 太阳能电池的发展已经进入了第三代.第一代为单晶硅太阳能电池,第二代为多晶硅、非晶硅等太阳能电池,第三代就是铜铟镓硒CIGs(CIS中掺入Ga)等化合物薄膜太阳能电池以及薄膜Si系太阳能电池.
太阳能电池的发展已经进入了第三代.第一代为单晶硅太阳能电池,第二代为多晶硅、非晶硅等太阳能电池,第三代就是铜铟镓硒CIGs(CIS中掺入Ga)等化合物薄膜太阳能电池以及薄膜Si系太阳能电池.