题目内容
10.已知FeSO4•7H2O的溶解度曲线如图所示,则从溶液中提取绿矾晶体采用的操作是蒸发浓缩、冷却结晶.
分析 由图象可知硫酸亚铁的溶解度随温度升高而增大,如析出晶体,应将饱和溶液降温,以此解答该题.
解答 解:由图象可知硫酸亚铁的溶解度随温度升高而增大,则从溶液中提取绿矾晶体,应采取蒸发浓缩、冷却结晶的方法,故答案为:蒸发浓缩、冷却结晶.
点评 本题考查物质的分离,提纯,为高频考点,侧重于学生的分析能力和实验能力的考查,注意把握物质的性质,难度不大.

练习册系列答案
 超能学典应用题题卡系列答案
超能学典应用题题卡系列答案
相关题目
1.质量分数不同的两种硫酸溶液,以相同质量混合时,所得混合溶液的密度为ρ1;以相同体积混合时,所得混合溶液的密度为ρ2,两种浓度不同的乙醇(密度小于水)溶液,以相同质量混合时,所得混合溶液的密度为ρ3;以相同体积混合时,所得溶液密度为ρ4,则ρ1、ρ2、ρ3、ρ4大小之间关系为( )
| A. | ρ1>ρ2>ρ3>ρ4 | B. | ρ1>ρ2>ρ4>ρ3 | C. | ρ2>ρ1>ρ3>ρ4 | D. | ρ2>ρ1>ρ4>ρ3 |
18.在一定条件下,对于密闭容器中进行的可逆反应:2HI(g) $\stackrel{△}{?}$H2(g)+I2(g),下列说法中可以充分说明这一反应已经达到化学平衡状态的是( )
| A. | HI、H2、I2的浓度相等 | B. | HI、H2、I2的浓度不再发生变化 | ||
| C. | HI、H2、I2在密闭容器中共存 | D. | 容器内气体的颜色不再发生变化 |
5.有如图所示装置,下列有关说法正确的是( )
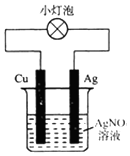

| A. | 该装置外电路中电流由Cu棒转移到Ag棒 | |
| B. | 该装置中正极是Cu、负极是Ag | |
| C. | 该装置可以将电能转化为化学能 | |
| D. | 该装置中正极上的电极反应为Ag++e-=Ag |
15.下列反应中必须加入还原剂才能进行的是( )
| A. | MnO4-→Mn2+ | B. | H2O2→H2O | C. | H2→H2O | D. | Zn→Zn2+ |
19.从物质分类的角度进行下列判断,正确的是( )
| A. | 根据是否具有丁达尔效应,可将分散系分为溶液、浊液和胶体 | |
| B. | SiO2既能与NaOH溶液反应,又能与氢氟酸反应,但SiO2不属于两性氧化物 | |
| C. | AgCl的水溶液不易导电,故AgCl是弱电解质 | |
| D. | 烧碱、纯碱、熟石灰均属于碱 |
20.甲醇是重要的工业原料.煤化工可以利用煤炭制取水煤气从而合成甲醇:CO(g)+2H2(g)?CH3OH(g).已知常温常压下反应的能量变化如图1所示: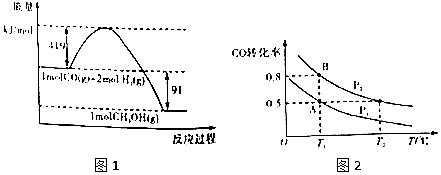
②
(3)CO(g)+$\frac{1}{2}$O2(g)=CO2(g)△H=-280kJ/mol
H2(g)+$\frac{1}{2}$O2(g)=H2O(I)△H=-284kJ/mol
H2O(I)=H2O(g)△H=+44kJ/mol
请回答下列问题:
(1)甲醇气体分解为CO和H2两种气体这一反应的活化能为510kj/mol;
(2)请写出表示气态甲醇燃烧热的热化学方程式CH3OH(g)+$\frac{3}{2}$O2(g)=CO2(g)+2H2O(l)△H=-757kJ•mol-1;
(3)H-O的键能x值为462;
(4)如图2:在一容积可变的密闭容器中充入10molCO气体和30molH2气体,当达到平衡状态A时,容器的体积为20L.如反应开始时仍充入10molCO和30molH2,则在平衡状态B时容器的体积V(B)=7L;
(5)在甲、乙、丙三个不同密闭容器中按不同方式投料,一定条件下发生该反应(起始温度和起始体积相同,反应物和生成物反应前后均为气态).相关数据如表所示:
则下列说法正确的是BC.
A.V(甲)>V(丙)B.K(乙)>K(丙)
C.c(乙)>c(甲) D.v(甲)=v(丙)

②
| 化学键 | H-H | H-O | O=O |
| 键能kj/mol | 436 | x | 496 |
H2(g)+$\frac{1}{2}$O2(g)=H2O(I)△H=-284kJ/mol
H2O(I)=H2O(g)△H=+44kJ/mol
请回答下列问题:
(1)甲醇气体分解为CO和H2两种气体这一反应的活化能为510kj/mol;
(2)请写出表示气态甲醇燃烧热的热化学方程式CH3OH(g)+$\frac{3}{2}$O2(g)=CO2(g)+2H2O(l)△H=-757kJ•mol-1;
(3)H-O的键能x值为462;
(4)如图2:在一容积可变的密闭容器中充入10molCO气体和30molH2气体,当达到平衡状态A时,容器的体积为20L.如反应开始时仍充入10molCO和30molH2,则在平衡状态B时容器的体积V(B)=7L;
(5)在甲、乙、丙三个不同密闭容器中按不同方式投料,一定条件下发生该反应(起始温度和起始体积相同,反应物和生成物反应前后均为气态).相关数据如表所示:
| 容器 | 甲 | 乙 | 丙 |
| 相关条件 | 恒温恒容 | 绝热恒容 | 恒温恒压 |
| 反应物投料 | 1molCO、2molH2 | 1molCH3OH | 1molCH3OH |
| 平衡时容器体积 | V(甲) | V(乙) | V(丙) |
| 反应的平衡常数K | K(甲) | K(乙) | K(丙) |
| 平衡时CH3OH的浓度/mol•L-1 | C(甲) | C(乙) | C(丙) |
| 平衡时CH3OH的反应速率/mol•L-1•min-1 | v(甲) | v(乙) | v(丙) |
A.V(甲)>V(丙)B.K(乙)>K(丙)
C.c(乙)>c(甲) D.v(甲)=v(丙)