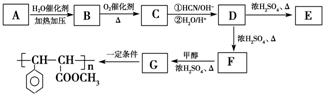
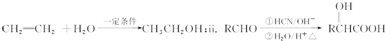题目内容
同温同压下,mg A气体与ng B气体的分子数相等,下列说法不正确的是( )
| A、同体积的A和B的质量比为m:n |
| B、等质量的A和B的分子数为n:m |
| C、同温同压下A和B的密度比为n:m |
| D、同温同压下等质量的A和B的体积比为n:m |
考点:阿伏加德罗定律及推论
专题:
分析:同温同压下,气体摩尔体积相等,mg A气体与ng B气体的分子数相等,说明二者的物质的量相等,根据n=
知,A、B的摩尔质量之比为m:n,结合m=
M、N=
NA、ρ=
、V=
Vm进行计算.
| m |
| M |
| V |
| Vm |
| m |
| M |
| M |
| Vm |
| m |
| M |
解答:
解:同温同压下,气体摩尔体积相等,mg A气体与ng B气体的分子数相等,说明二者的物质的量相等,根据n=
知,A、B的摩尔质量之比为m:n,
A.相同条件下,根据m=
M知,气体体积相等时,气体的质量与摩尔质量成正比,所以A、B的质量之比=m:n,故A正确;
B.根据N=
NA知,相同质量时气体分子数之比等于摩尔质量反比=n:m,故B正确;
C.根据ρ=
知,气体摩尔体积相等时,气体的密度之比等于其摩尔质量之比=m:n,故C错误;
D.根据V=
Vm知,相同条件下,质量相等时气体体积之比等于摩尔质量反比=n:m,故D正确;
故选C.
| m |
| M |
A.相同条件下,根据m=
| V |
| Vm |
B.根据N=
| m |
| M |
C.根据ρ=
| M |
| Vm |
D.根据V=
| m |
| M |
故选C.
点评:本题考查阿伏伽德罗定律及其推论,侧重考查公式灵活运用,明确物质的量公式中各个物理量的关系是解本题关键,会根据基本公式进行推导,题目难度中等.

练习册系列答案
相关题目
0.5mol Na2SO4中所含的Na+的数目为( )
| A、NA |
| B、2NA |
| C、3.01×1023 |
| D、6.02×1024 |
下列关于药物的使用说法正确的是( )
| A、虽然药物能治病,但大部分药物有毒副作用 |
| B、使用青霉素时,直接静脉注射可以不用进行皮肤敏感试验 |
| C、长期大量使用阿司匹林可预防疾病,没有副作用 |
| D、麻黄碱有镇静催眠的效果 |
用分液漏斗可以分离的一组液体混合物是( )
| A、硝基苯和水 | B、溴和四氯化碳 |
| C、苯和溴苯 | D、己烷和苯 |

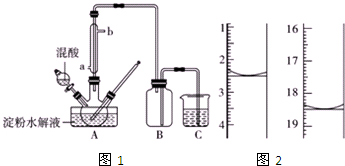 淀粉水解的产物(C6H12O6)用硝酸氧化可以制备草酸,装置如图1所示(加热,搅拌和仪器固定装置均已略去)
淀粉水解的产物(C6H12O6)用硝酸氧化可以制备草酸,装置如图1所示(加热,搅拌和仪器固定装置均已略去)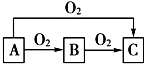 ABC是中学化学中常见的三种物质,它们之间的相互转化关系如图(部分反应条件及产物略去),回答下列问题:
ABC是中学化学中常见的三种物质,它们之间的相互转化关系如图(部分反应条件及产物略去),回答下列问题: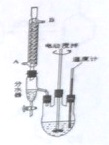 邻苯二甲酸二异癸酯为无色粘稠液体,密度约为0.966g?cm-3,不溶于水,易溶于有机溶剂,常用作耐热塑料增塑剂,某实验小组用如图所示装置制取少量邻苯二甲酸二异癸酯(图中夹持和加热装置已略去).主要操作步骤如下:
邻苯二甲酸二异癸酯为无色粘稠液体,密度约为0.966g?cm-3,不溶于水,易溶于有机溶剂,常用作耐热塑料增塑剂,某实验小组用如图所示装置制取少量邻苯二甲酸二异癸酯(图中夹持和加热装置已略去).主要操作步骤如下: