题目内容
7.质量分数为a的某物质的溶液m g与质量分数为b的该物质的溶液n g混合后,蒸发掉p g水,得到的溶液每毫升质量为q g,物质的量浓度为c.则溶质的分子量(相对分子质量)为( )| A. | $\frac{q(am+bn)}{c(m+n-p)}$ | B. | $\frac{c(m+n-p)}{q(am+bn)}$ | ||
| C. | $\frac{1000q(am+bn)}{c(m+n-p)}$ | D. | $\frac{c(m+n-p)}{1000q(am+bn)}$ |
分析 蒸发掉p g水后溶质质量分数为:$\frac{ma+nb}{m+n-p}$,再根据c=$\frac{1000ρω}{M}$的计算溶质的相对分子质量.
解答 解:蒸发掉p g水后溶质质量分数为:$\frac{ma+nb}{m+n-p}$,
根据c=$\frac{1000ρω}{M}$可知,溶质的摩尔质量M=$\frac{1000ρω}{c}$=$\frac{1000×q×\frac{ma+nb}{m+n-p}}{c}$g/mol=$\frac{1000q(am+bn)}{c(m+n-p)}$g/mol,
所以溶质的相对分子质量为 $\frac{1000q(am+bn)}{c(m+n-p)}$,
故选:C.
点评 本题考查溶液浓度有关计算,涉及物质的量浓度度、质量分数,属于字母型计算,为易错题目,掌握物质的量浓度与质量分数关系,注意公式的灵活运用.

练习册系列答案
 名师伴你成长课时同步学练测系列答案
名师伴你成长课时同步学练测系列答案
相关题目
17.化合物C是制备液晶材料的中间体之一,它可由A和B在一定条件下制得下列说法正确的是( )


| A. | 可用FeCl3溶液检验C中是否含有B | |
| B. | 1molC分子最多可与4molH2发生加成反应 | |
| C. | 可以用酸性KMnO4溶液检验B中是否含有-CHO | |
| D. | 1molC与NaOH溶液反应时最多消耗1molNaOH |
15.向密度为d g•cm-3的盐酸中逐滴加入硝酸银溶液到过量,生成沉淀的质量与原盐酸的质量相等,原盐酸的物质的量浓度为( )
| A. | 25.4d mol•L-1 | B. | 12.7d mol•L-1 | C. | 6.97d mol•L-1 | D. | 6.35d mol•L-1 |
2.下列物质中与其他三组不同的是( )
| A. | 金刚石、石墨、C60 | B. | 红磷、白磷 | ||
| C. | 一氧化碳、二氧化碳 | D. | 氧气、臭氧 |
12.某烃的结构简式为 ,它可能具有的性质是( )
,它可能具有的性质是( )
 ,它可能具有的性质是( )
,它可能具有的性质是( )| A. | 易溶于水,也易溶于有机溶剂 | |
| B. | 1 mol该烃含有4 mol碳碳双键 | |
| C. | 能发生聚合反应,其产物可表示为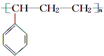 | |
| D. | 既能使溴水褪色,又能使酸性KMnO4溶液褪色 |
19.下列离子方程式书写错误的是( )
| A. | 在NaHSO4溶液中加Ba(OH)2至中性:Ba2++2OH-+2H++SO${\;}_{4}^{2-}$=BaSO4↓+2H2O | |
| B. | 向硫酸铜溶液中通入H2S气体:Cu2++H2S═CuS↓+2H+ | |
| C. | SO2气体通入Ba(OH)2溶液中:SO2+2OH-═SO${\;}_{3}^{2-}$ | |
| D. | 用稀硫酸酸化硫化钠和亚硫酸钠的混合溶液:SO${\;}_{3}^{2-}$+2S2-+6H+═3S↓+3H2O |
16.下列物质中,发生消去反应生成的烯烃只有一种的是( )
①2丁醇
②2甲基2丙醇
③1丁醇
④2甲基2丁醇.
①2丁醇
②2甲基2丙醇
③1丁醇
④2甲基2丁醇.
| A. | ①② | B. | ②③ | C. | ②④ | D. | ③④ |
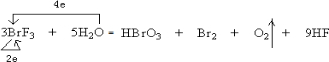 ,还原剂是H2O和BrF3,氧化剂是BrF3.氧化产物是HBrO3、O2. 还原产物是Br2(以上均填化学式)
,还原剂是H2O和BrF3,氧化剂是BrF3.氧化产物是HBrO3、O2. 还原产物是Br2(以上均填化学式)