题目内容
17.根据反应3BrF3+5H2O═HBrO3+Br2+O2↑+9HF回答下列问题:(1)用单线桥法标明电子转移方向和数目
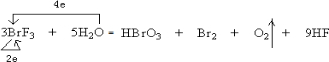 ,还原剂是H2O和BrF3,氧化剂是BrF3.氧化产物是HBrO3、O2. 还原产物是Br2(以上均填化学式)
,还原剂是H2O和BrF3,氧化剂是BrF3.氧化产物是HBrO3、O2. 还原产物是Br2(以上均填化学式)(2)当有5mol水参加反应,则被还原的BrF3物质的量为2mol.
(3)当有5mol水参加反应,则被水还原的BrF3物质的量为$\frac{4}{3}$mol.
(4)已知生成的Br2与 NaI溶液发生置换反应,请写出该反应的离子方程式Br2+2I-=2Br-+I2.
分析 3BrF3+5H2O→HBrO3+Br2+O2+9HF中,溴元素的化合价由+3价变为0价和+5价,氧元素的化合价由-2价变为0价,所以氧化剂是BrF3,还原剂是BrF3和H2O,氧化产物是HBrO3、O2,还原产物是Br2,被还原的元素是+3价的溴,该反应中,部分溴失电子部分得电子,水中氧元素失电子,转移电子数是6,以此来解答.
解答 解:(1)3BrF3+5H2O→HBrO3+Br2+O2+9HF中,溴元素的化合价由+3价变为0价和+5价,氧元素的化合价由-2价变为0价,所以氧化剂是BrF3,还原剂是BrF3和H2O,氧化产物是HBrO3、O2,还原产物是Br2,被还原的元素是+3价的溴,该反应中,部分溴失电子部分得电子,水中氧元素失电子,转移电子数是6,用单线桥法标明电子转移方向和数目为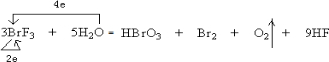 ,
,
故答案为: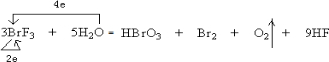 ;H2O 和BrF3;BrF3;HBrO3、O2;Br2;
;H2O 和BrF3;BrF3;HBrO3、O2;Br2;
(2)当有5mol水参加反应,由反应可知,3molBrF3中2mol作氧化剂,则被还原的BrF3物质的量为2mol,故答案为:2mol;
(3)当有5mol水参加反应,2mol作还原剂,由电子守恒可知,则被水还原的BrF3物质的量为$\frac{2mol×(2-0)}{(3-0)}$=$\frac{4}{3}$mol,故答案为:$\frac{4}{3}$mol;
(4)Br2与 NaI溶液发生置换反应,离子反应为Br2+2I-=2Br-+I2,故答案为:Br2+2I-=2Br-+I2.
点评 本题考查氧化还原反应及计算,为高频考点,把握反应中元素的化合价变化为解答的关键,侧重氧化还原反应转移电子的考查,注意从元素的化合价角度分析,题目难度不大.

练习册系列答案
相关题目
7.质量分数为a的某物质的溶液m g与质量分数为b的该物质的溶液n g混合后,蒸发掉p g水,得到的溶液每毫升质量为q g,物质的量浓度为c.则溶质的分子量(相对分子质量)为( )
| A. | $\frac{q(am+bn)}{c(m+n-p)}$ | B. | $\frac{c(m+n-p)}{q(am+bn)}$ | ||
| C. | $\frac{1000q(am+bn)}{c(m+n-p)}$ | D. | $\frac{c(m+n-p)}{1000q(am+bn)}$ |
5.下列有关金属钠的说法中,错误的是( )
| A. | 钠应保存在煤油中 | |
| B. | 钠与氧气反应的产物与反应条件有关 | |
| C. | 钠在反应中易失去电子,表现出还原性 | |
| D. | 钠只有在加热条件下才能与氯气反 |
12.通过对实验现象的观察、分析推理得出正确的结论是化学学习的方法之一.对下列实验事实的解释正确的是( )
| 现象 | 解释 | |
| A | KI淀粉溶液中通入Cl2,溶液变蓝 | Cl2能与淀粉发生显色反应 |
| B | 浓HNO3在光照条件下变黄 | 浓HNO3不稳定,生成有色产物能溶于浓硝酸 |
| C | 某溶液中加入硝酸酸化的氯化钡溶液,有白色沉淀生成 | 说明该溶液中含有SO42- |
| D | 铜片放入浓硫酸中,无明显变化 | 说明铜在冷的浓硫酸中发生钝化 |
| A. | A | B. | B | C. | C | D. | D |
6.已知:CH4、C2H6的一氯代物都只有一种,则50个碳原子以内,且一氯代物只有一种的烷烃共有( )
| A. | 6种 | B. | 7种 | C. | 8种 | D. | 9种 |
