题目内容
根据如图,下列判断中正确的是( )
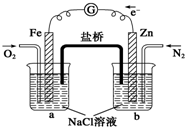

| A、烧杯a中的溶液pH不变 |
| B、烧杯a中发生氧化反应 |
| C、烧杯b中发生的反应为Zn-2e-=Zn2+ |
| D、烧杯a中发生的反应为2H2O+2e-=H2↑+2OH- |
考点:原电池和电解池的工作原理
专题:电化学专题
分析:装置图为原电池反应,b中电极锌做负极失电子发生氧化反应,a中电极上氧气得到电子发生还原反应生成氢氧根离子,溶液pH升高.
解答:
解:A、烧杯a中发生的氧气得到电子生成氢氧根离子的反应,电极反应为:O2+2H2O+4e-=4OH-,氢氧根离子浓度增大,溶液pH增大,故A错误;
B、烧杯a中发生的氧气得到电子生成氢氧根离子的反应,属于还原反应,故B错误;
C、烧杯b中电极上是锌失电子发生氧化反应,电极反应为Zn-2e-=Zn2+,故C正确;
D、杯a中发生的氧气得到电子生成氢氧根离子的反应,电极反应为O2+2H2O+4e-=4OH-,故D错误;
故选C.
B、烧杯a中发生的氧气得到电子生成氢氧根离子的反应,属于还原反应,故B错误;
C、烧杯b中电极上是锌失电子发生氧化反应,电极反应为Zn-2e-=Zn2+,故C正确;
D、杯a中发生的氧气得到电子生成氢氧根离子的反应,电极反应为O2+2H2O+4e-=4OH-,故D错误;
故选C.
点评:本题考查了原电池原理的分析应用,电极判断和电极反应是解题关键,题目较简单.

练习册系列答案
相关题目
下列物质中,不属于合金的是( )
| A、硬铝 | B、水银 | C、黄铜 | D、钢铁 |
下列各组物质全部是弱电解质的是( )
| A、H2O、NH3?H2O、H3PO4、HF |
| B、Cu(OH)2、CH3COOH、C2H5OH、CH3COONa |
| C、H2SO3、Ba(OH)2、BaSO4 AgCl |
| D、H2SiO3、H2S、CO2 |
在固定容积的密闭容器中,可逆反应2X+Y(g)?Z(s)已达到平衡,此时升高温度则气体混合物的密度增大.下列叙述正确的是( )
| A、若X为非气态,则正反应为吸热反应 |
| B、正反应为放热反应,X一定为气态 |
| C、正反应为放热反应,X可能是气态、液态或固态 |
| D、若加入少量的Z,该平衡向左移动 |
下面关于电解质的叙述中错误的是( )
| A、在水溶液中或熔融状态下均不导电的化合物叫非电解质 |
| B、电解质、非电解质都指化合物而言,单质不属于此范畴 |
| C、电解质在水中一定能导电,在水中导电的化合物一定是电解质 |
| D、BaSO4不溶于水,但BaSO4是电解质 |
设NA表示阿伏加德罗常数的值,下列叙述中正确的是( )
| A、常温常压下,20 g D2O和足量的金属钠反应产生气体的分子数为0.5NA |
| B、0.1 mol?L-1的Na2CO3溶液中Na+数为0.1NA |
| C、若一筒120g的墨粉能打a个字,则平均每个字约含有10NA个碳原子 |
| D、0.5mol的甲基(-CH3)与氢氧根(OH-)所含电子数都为5NA |