题目内容
8.下列有关实验的说法中正确的是( )| A. | 在利用重结晶的方法制备KNO3的过程中,可在漏斗中加入酒精来洗涤 | |
| B. | 在石油的分馏实验中,冷凝管中冷水应从上口进入,热水从下口流出 | |
| C. | 粗盐提纯中,在溶解粗盐时,应用大量的水来溶解,以防止食盐不完全溶解 | |
| D. | 在分液实验中,待液体静置分层后,上、下层液体都应分别从分液漏斗下端的活塞放出 |
分析 A.硝酸钾在酒精中的溶解性较小且酒精易挥发;
B.分馏时,冷凝管中水应该从下口流入上口流出;
C.溶解食盐时需要加适量水;
D.分液时,上层液体从上口倒出,下层液体从下口倒出.
解答 解:A.硝酸钾在酒精中的溶解性较小且酒精易挥发,所以在利用重结晶的方法制备KNO3的过程中,可在漏斗中加入酒精来洗涤,减少硝酸钾损失,故A正确;
B.分馏时,冷凝管中水应该从下口流入上口流出,否则易炸裂冷凝管,故B错误;
C.溶解食盐时需要加适量水,如果溶液太稀,蒸发时耗时太长,故C错误;
D.分液时,上层液体从上口倒出,下层液体从下口倒出,否则易产生杂质,故D错误;
故选A.
点评 本题考查化学实验方案评价,为高频考点,涉及实验基本操作为重结晶、分馏、蒸发、分液,明确实验操作规范性及实验安全、实验原理是解本题关键,注意冷凝管中水流方向,为易错点.

练习册系列答案
 中考利剑中考试卷汇编系列答案
中考利剑中考试卷汇编系列答案 教育世家状元卷系列答案
教育世家状元卷系列答案 黄冈课堂作业本系列答案
黄冈课堂作业本系列答案 单元加期末复习先锋大考卷系列答案
单元加期末复习先锋大考卷系列答案
相关题目
19.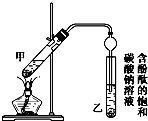 已知下列数据:
已知下列数据:
某学生在实验室制取乙酸乙酯的主要步骤如下:
①配制2mL浓硫酸、3mL乙醇(含18O)和2mL乙酸的混合溶液.
②按如图所示连接好装置(装置气密性良好)并加入混合液,用小火均匀加热3~5min.
③待试管乙收集到一定量产物后停止加热,撤出试管乙并用力振荡,然后静置分层.
④分离出乙酸乙酯,洗涤、干燥.
(1)配制①中混合溶液的方法为应先加入乙醇,然后边摇动试管边慢慢加入浓硫酸,最后加入冰醋酸;
反应中浓硫酸的作用是催化剂 吸水剂;写出制取乙酸乙酯的化学方程式:CH3COOH+C2H5OH$?_{△}^{浓H_{2}SO_{4}}$CH3COOC2H5+H2O.
(2)上述实验中饱和碳酸钠溶液的作用是BC(填字母).
A.中和乙酸和乙醇 B.中和乙酸并吸收乙醇 C.减少乙酸乙酯的溶解 D.加速酯的生成,提高其产率
(3)步骤②中需要小火均匀加热,其主要理由是减少乙酸乙醇的挥发,减少副反应的发生;步骤③所观察到的现象是试管乙中的液体分成上下两层,上层无色,下层为红色液体,振荡后下层液体的红色变浅;
欲将乙试管中的物质分离以得到乙酸乙酯,必须使用的仪器有分液漏斗;分离时,乙酸乙酯应从仪器上口倒(填“下口放”或“上口倒”)出.
(4)该同学反复实验,得出乙醇与乙酸的用量和得到的乙酸乙酯生成量如表:
表中数据x的范围是1.57<X<1.76;实验①②⑤探究的是增加乙醇或乙酸的用量对酯产量的影响.
 已知下列数据:
已知下列数据:| 物质 | 熔点(℃) | 沸点(℃) | 密度(g•cm-3) |
| 乙醇 | -117.0 | 78.0 | 0.79 |
| 乙酸 | 16.6 | 117.9 | 1.05 |
| 乙酸乙酯 | -83.6 | 77.5 | 0.90 |
①配制2mL浓硫酸、3mL乙醇(含18O)和2mL乙酸的混合溶液.
②按如图所示连接好装置(装置气密性良好)并加入混合液,用小火均匀加热3~5min.
③待试管乙收集到一定量产物后停止加热,撤出试管乙并用力振荡,然后静置分层.
④分离出乙酸乙酯,洗涤、干燥.
(1)配制①中混合溶液的方法为应先加入乙醇,然后边摇动试管边慢慢加入浓硫酸,最后加入冰醋酸;
反应中浓硫酸的作用是催化剂 吸水剂;写出制取乙酸乙酯的化学方程式:CH3COOH+C2H5OH$?_{△}^{浓H_{2}SO_{4}}$CH3COOC2H5+H2O.
(2)上述实验中饱和碳酸钠溶液的作用是BC(填字母).
A.中和乙酸和乙醇 B.中和乙酸并吸收乙醇 C.减少乙酸乙酯的溶解 D.加速酯的生成,提高其产率
(3)步骤②中需要小火均匀加热,其主要理由是减少乙酸乙醇的挥发,减少副反应的发生;步骤③所观察到的现象是试管乙中的液体分成上下两层,上层无色,下层为红色液体,振荡后下层液体的红色变浅;
欲将乙试管中的物质分离以得到乙酸乙酯,必须使用的仪器有分液漏斗;分离时,乙酸乙酯应从仪器上口倒(填“下口放”或“上口倒”)出.
(4)该同学反复实验,得出乙醇与乙酸的用量和得到的乙酸乙酯生成量如表:
| 实验 | 乙醇(mL) | 乙酸(mL) | 乙酸乙酯(mL) |
| ① | 2 | 2 | 1.33 |
| ② | 3 | 2 | 1.57 |
| ③ | 4 | 2 | x |
| ④ | 5 | 2 | 1.76 |
| ⑤ | 2 | 3 | 1.55 |
16. 用甲烷和二氧化碳可以制备化工原料.
用甲烷和二氧化碳可以制备化工原料.
(1)一定温度下,向容积恒为2L的密闭容器中通入3mol CO2,3mol CH4,发生如下反应:
CO2(g)+CH4(g)?2CO(g)+2H2(g)
反应在2min末达到平衡状态,此时测得CO2和CO的体积分数相等.清回答下列问题:
①2min内,用H2来表示的反应速率v(H2)=0.5mol/(L•min);
②此温度下该反应的平衡常数K=1;
③下列叙述可以作为该反应达到平衡状态的标志的是BC;(填选项字母)
A.v正(CH4)=v逆(H2)
B.容器内压强保持恒定不变
C.反应中断裂2mol C-H键同时消耗1mol H2
D.容器内混合气体的密度保持恒定不变
④已知:
则反应CO2(g)+CH4(g)?2CO(g)+2H2(g)△H=248kJ/mol.
⑤为提高CH4的转化率,可以采取的措施是减小反应压强、增大CO2的浓度.(写两点)
(2)在催化作用下,甲烷和二氧化碳还可以直接转化成乙酸.
①在不同温度下乙酸的生成速率如图所示:
在250-400℃范围内,乙酸的生成速率随温度变化的原因是温度超过250℃时,催化剂的催化效率降低.
②250℃与400℃时乙酸的生成速率相近,清分析判断实际生产选择的最佳温度是250℃.
 用甲烷和二氧化碳可以制备化工原料.
用甲烷和二氧化碳可以制备化工原料.(1)一定温度下,向容积恒为2L的密闭容器中通入3mol CO2,3mol CH4,发生如下反应:
CO2(g)+CH4(g)?2CO(g)+2H2(g)
反应在2min末达到平衡状态,此时测得CO2和CO的体积分数相等.清回答下列问题:
①2min内,用H2来表示的反应速率v(H2)=0.5mol/(L•min);
②此温度下该反应的平衡常数K=1;
③下列叙述可以作为该反应达到平衡状态的标志的是BC;(填选项字母)
A.v正(CH4)=v逆(H2)
B.容器内压强保持恒定不变
C.反应中断裂2mol C-H键同时消耗1mol H2
D.容器内混合气体的密度保持恒定不变
④已知:
| 物质 | H2 | CO | CH4 | CH3COOH |
| 燃烧热(kJ/mol) | 286 | 283 | 890 | 874 |
⑤为提高CH4的转化率,可以采取的措施是减小反应压强、增大CO2的浓度.(写两点)
(2)在催化作用下,甲烷和二氧化碳还可以直接转化成乙酸.
①在不同温度下乙酸的生成速率如图所示:
在250-400℃范围内,乙酸的生成速率随温度变化的原因是温度超过250℃时,催化剂的催化效率降低.
②250℃与400℃时乙酸的生成速率相近,清分析判断实际生产选择的最佳温度是250℃.
3.根据反应(1)→(4),可以判断下列4个物质的氧化性由强到弱的正确顺序是( )
(1)Cl2+2KI=2KCl+I2;
(2)2FeCl2+Cl2=2FeCl3;
(3)2FeCl3+2HI=2FeCl2+2HCl+I2,
(4)H2S+I2=S+2HI.
(1)Cl2+2KI=2KCl+I2;
(2)2FeCl2+Cl2=2FeCl3;
(3)2FeCl3+2HI=2FeCl2+2HCl+I2,
(4)H2S+I2=S+2HI.
| A. | S>I2>Fe3+>Cl2 | B. | Cl2>Fe3+>I2>S | C. | Fe3+>Cl2>S>I2 | D. | Cl2>I2>Fe3+>S |
13.有A、B、C、D、E五种短周期元素,其元素特征信息如下表:
回答下列问题:
(1)写出B的氢化物的结构式H-O-H
(2)①写出E单质与A、B、C形成的化合物反应的化学方程式:Cl2+2NaOH═NaCl+NaClO+H2O
②D的氧化物与A、B、C形成的化合物的水溶液反应的离子方程式:Al2O3+2 OH-═AlO2-+H2O.
| 元素编号 | 元素特征信息 |
| A | 其单质是密度最小的物质. |
| B | 阴离子带两个单位负电荷,单质是空气的主要成分之一. |
| C | 其阳离子与B的阴离子有相同的电子层结构,且与B可以形成两种离子化合物. |
| D | 其氢氧化物和氧化物都有两性,与C同周期 |
| E | 与C同周期,原子半径在该周期最小 |
(1)写出B的氢化物的结构式H-O-H
(2)①写出E单质与A、B、C形成的化合物反应的化学方程式:Cl2+2NaOH═NaCl+NaClO+H2O
②D的氧化物与A、B、C形成的化合物的水溶液反应的离子方程式:Al2O3+2 OH-═AlO2-+H2O.
20.下列属于同系物的是( )
①金刚石与“足球烯”C60
②D与T
③16O、17O和18O
④氧气(O2)与臭氧(O3)
⑤CH4和CH3CH2CH3
⑥乙醇(CH3CH2OH)和甲醚(CH3OCH3)
⑦ 和
和
⑧ 和
和
①金刚石与“足球烯”C60
②D与T
③16O、17O和18O
④氧气(O2)与臭氧(O3)
⑤CH4和CH3CH2CH3
⑥乙醇(CH3CH2OH)和甲醚(CH3OCH3)
⑦
 和
和
⑧
 和
和
| A. | ①④ | B. | ⑤⑦ | C. | ⑥⑧ | D. | ②③ |
18.海水是巨大的资源宝库.如图是人类从海水资源获取某些重要化工原料的流程示意图.

回答下列问题:
(1)操作A是蒸发结晶(填实验基本操作名称).要知道海水晒盐的过程中溶液里食盐含量在逐渐提高的简易方法是b.
a.分析氯化钠含量 b.测定溶液密度 c.观察是否有沉淀析出
(2)操作B需加入下列试剂中的一种,最合适的是c(选填编号).
a.氢氧化钠溶液 b.澄清石灰水 c.石灰乳d.碳酸钠溶液
(3)操作C是热空气吹出;上图中虚线框内流程的主要作用是富集Br2.
(4)图中虚线框内流程也可用 替代,请将Br2与Na2CO3,反应的化学方程式补充完整:3Br2+3Na2CO3═1NaBrO3+5NaBr+3CO2
替代,请将Br2与Na2CO3,反应的化学方程式补充完整:3Br2+3Na2CO3═1NaBrO3+5NaBr+3CO2
(5)已知苦卤的主要成分如表:
理论上,1L苦卤最多可得到Mg(OH)2的质量为69.6g.

回答下列问题:
(1)操作A是蒸发结晶(填实验基本操作名称).要知道海水晒盐的过程中溶液里食盐含量在逐渐提高的简易方法是b.
a.分析氯化钠含量 b.测定溶液密度 c.观察是否有沉淀析出
(2)操作B需加入下列试剂中的一种,最合适的是c(选填编号).
a.氢氧化钠溶液 b.澄清石灰水 c.石灰乳d.碳酸钠溶液
(3)操作C是热空气吹出;上图中虚线框内流程的主要作用是富集Br2.
(4)图中虚线框内流程也可用
 替代,请将Br2与Na2CO3,反应的化学方程式补充完整:3Br2+3Na2CO3═1NaBrO3+5NaBr+3CO2
替代,请将Br2与Na2CO3,反应的化学方程式补充完整:3Br2+3Na2CO3═1NaBrO3+5NaBr+3CO2(5)已知苦卤的主要成分如表:
| 离子 | Na+ | Mg2+ | Cl- | SO${\;}_{4}^{2-}$ |
| 浓度/(g•L-1) | 63.7 | 28.8 | 144.6 | 46.4 |
