题目内容
一元强酸和一元强碱恰好完全中和时,两者一定相等的是( )
| A、质量 |
| B、溶液的体积 |
| C、物质的量浓度 |
| D、H+和OH-的物质的量 |
考点:物质的量的相关计算
专题:
分析:一元强酸和一元强碱恰好完全中和时,H+和OH-的物质的量,强酸与强碱的摩尔质量不一定相等,二者质量不一定相等,溶液体积不一定相等,物质的量浓度也不一定相等.
解答:
解:一元强酸和一元强碱恰好完全中和时,反应反应:H++OH-=H2O,故H+和OH-的物质的量,
A.强酸与强碱的摩尔质量不一定相等,二者质量不一定相等,溶液体积不一定相等,故A错误;
B.溶液物质的量浓度相等,则溶液体积相等,二者浓度不一定相等,故溶液体积不一定相等,故B错误;
C.若溶液体积相等,则溶液物质的量浓度相等,二者溶液体积不一定相等,故溶液物质的量浓度不一定相等,故C错误;
D.一元强酸和一元强碱恰好完全中和时,反应反应:H++OH-=H2O,故H+和OH-的物质的量,故D正确,
故选D.
A.强酸与强碱的摩尔质量不一定相等,二者质量不一定相等,溶液体积不一定相等,故A错误;
B.溶液物质的量浓度相等,则溶液体积相等,二者浓度不一定相等,故溶液体积不一定相等,故B错误;
C.若溶液体积相等,则溶液物质的量浓度相等,二者溶液体积不一定相等,故溶液物质的量浓度不一定相等,故C错误;
D.一元强酸和一元强碱恰好完全中和时,反应反应:H++OH-=H2O,故H+和OH-的物质的量,故D正确,
故选D.
点评:本题以酸碱中和为载体,考查物质的量浓度有关计算,比较基础,有利于基础知识的巩固.

练习册系列答案
相关题目
已知:25℃时,Ksp[Mg(OH)2]=5.61×10-12,Ksp[MgF2]=7.42×10-11.下列说法正确的是( )
| A、25℃时,饱和Mg(OH)2溶液与饱和MgF2溶液相比,前者的c(Mg2+)大 |
| B、25℃时,Mg(OH)2的悬浊液加入少量的NH4Cl固体,c(Mg2+)增大 |
| C、25℃时,Mg(OH)2固体在20 mL 0.01 mol?L-1氨水中的Ksp比在20 mL 0.01 mol?L-1NH4Cl溶液中的Ksp小 |
| D、25℃时,在Mg(OH)2的悬浊液中加入NaF溶液后,Mg(OH)2不可能转化成为MgF2 |
下列实验过程正确的是( )
| A、用酒精萃取碘水中的碘 |
| B、用稀硫酸清洗做焰色反应的铂丝 |
| C、用加热法分离氯化钠和碳酸钙的固体混合物 |
| D、分液操作时分液漏斗中下层液体从下口放出,上层液体从上口倒出 |
在2A+B?3C+4D反应中,表示该反应速率最快的是( )
| A、v(A)=0.5 mol?L-1?min-1 |
| B、v(B)=0.01 mol?L-1?s-1 |
| C、v(C)=0.8 mol?L-1?min-1 |
| D、v(D)=1 mol?L-1?min-1 |
铍元素性质与铝元素性质相似,下列方法能证明氯化铍是分子晶体的是( )
| A、溶于硝酸银溶液,观察是否有白色沉淀生成 |
| B、溶于水做导电实验,观察是否导电 |
| C、熔融状态,做导电实验,观察是否导电 |
| D、测定氯化铍熔点 |
用NA表示阿伏加德罗常数,下列说法中错误的是( )
| A、在一定温度压强下,14 gN2所含的体积可能为11.2 L |
| B、标准状况下,足量NaOH溶液与2.24 LCl2反应,转移电子数目为0.1NA |
| C、标准状况下,11.2 LH2O中含有的电子数为5NA |
| D、加热条件下,足量Cl2与1 molFe粉充分反应,转移的电子数为3NA |
纳米科技是21世纪经济发展的发动机.人们会利用纳米级(1~100nm,1nm=10-9 m)粒子物质制造出更加优秀的材料和器件,使化学在材料、能、环境和生命科学等领域发挥越越重要的作用.下列分散系中分散质颗粒与纳米级粒子在直径上具有相同数量级的是( )
| A、溶液 | B、悬浊液 |
| C、胶体 | D、乳浊液 |
短周期主族元素X、Y、Z、W在元素周期表中的相对位置如表所示.已知X的最低负价与Y的最高正价代数和为零,下列说法正确的是( )
| X | ||||
| Y | Z | W |
| A、原子半径的大小顺序:r(Y)>r(Z)>r(W)>r(X) |
| B、Z的最高价氧化物的水化物酸性比W的强 |
| C、X的简单气态氢化物的稳定性比W的弱 |
| D、X分别与Y、Z形成的化合物中化学键类型相同 |
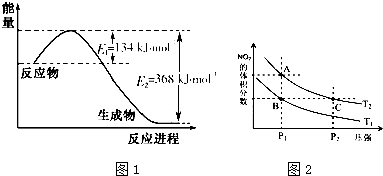 氮是地球上含量丰富的一种元素,氮及其化合物在生产、生活中有着重要作用.
氮是地球上含量丰富的一种元素,氮及其化合物在生产、生活中有着重要作用.