题目内容
已知化合物X和Y的化学式的组成相似,经测定X中各元素的质量分数分别为:钾-a%,硫-b%,其余是氧元素;化合物Y中各元素的质量分数分别为:钾-c%,硒-d%,其余是氧元素,硫的相对原子质量是32,试求硒的相对原子质量.
考点:物质的量的相关计算
专题:计算题
分析:根据题意:化合物X和Y的化学式的组成相似,即构成物质的各个元素原子的数目是相等的,根据氧元素的含量相等来计算.
解答:
设硒的相对原子质量为x,那么两种化合物的氧有如下关系(组成相似,氧原子数相等):
×(1-a%-b%)=
×(1-c%-d%),解得x=
.
答:硒的相对原子质量是
.
| 32 |
| b% |
| x |
| d% |
| 32d(1-a%-b%) |
| b(1-c%-d%) |
答:硒的相对原子质量是
| 32d(1-a%-b%) |
| b(1-c%-d%) |
点评:本题目是一道信息的迁移应用题,考查学生分析和解决问题的能力,难度不大.

练习册系列答案
相关题目
某溶液中只可能含有下列离子中的几种(不考虑溶液中含的较少的H+和OH-):Na+、NH4+、SO42-、CO32-、NO3-.取200mL该溶液,分为等体积的两份分别做下列实验.实验1:第一份加入足量的烧碱并加热,产生的气体在标准状况下为224mL.实验2:第二份先加入足量的盐酸,无现象,再加入足量的BaCl2溶液,得固体2.33g.下列说法正确的是( )
| A、该溶液中一定含有Na+,且c(Na+)≥0.1 mol?L-1 |
| B、该溶液中可能含有Na+ |
| C、该溶液中一定不含NO3- |
| D、该溶液中肯定含有NH4+、SO42-、CO32-、NO3- |
NA表示阿伏伽德罗常数.下列叙述正确的是( )
| A、1mol CH4所含原子总数是5NA |
| B、32g硫与足量铜完全反应转移的电子数为2NA |
| C、2L 1mol/L的盐酸溶液中,所含氯化氢分子个数是2NA |
| D、2mol SO2和1mol O2混合后,在V2O5存在的条件下密闭容器中加热反应后,容器内分子总数是2NA |

 100mL某无色溶液由H+、Na+、Mg2+、Al3+、Fe3+、CO32-、Cl-等离子中的几种混合组成(不考虑水电离出的离子),向溶液中逐滴加0.5mol/L氢氧化钠溶液直到过量,产生沉淀的情况如图所示.
100mL某无色溶液由H+、Na+、Mg2+、Al3+、Fe3+、CO32-、Cl-等离子中的几种混合组成(不考虑水电离出的离子),向溶液中逐滴加0.5mol/L氢氧化钠溶液直到过量,产生沉淀的情况如图所示.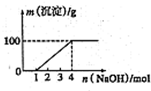 某澄清透明溶液中只可能含有①Al3+;②Mg2+;③Fe3+;④Fe2+;⑤H+;⑥CO32-;⑦NO3-中的几种,向该溶液中逐滴加入NaOH溶液至过量,生成沉淀的质量与NaOH的物质的量的关系如图所示.则该溶液中一定含有的离子是( )
某澄清透明溶液中只可能含有①Al3+;②Mg2+;③Fe3+;④Fe2+;⑤H+;⑥CO32-;⑦NO3-中的几种,向该溶液中逐滴加入NaOH溶液至过量,生成沉淀的质量与NaOH的物质的量的关系如图所示.则该溶液中一定含有的离子是( )