题目内容
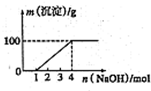 某澄清透明溶液中只可能含有①Al3+;②Mg2+;③Fe3+;④Fe2+;⑤H+;⑥CO32-;⑦NO3-中的几种,向该溶液中逐滴加入NaOH溶液至过量,生成沉淀的质量与NaOH的物质的量的关系如图所示.则该溶液中一定含有的离子是( )
某澄清透明溶液中只可能含有①Al3+;②Mg2+;③Fe3+;④Fe2+;⑤H+;⑥CO32-;⑦NO3-中的几种,向该溶液中逐滴加入NaOH溶液至过量,生成沉淀的质量与NaOH的物质的量的关系如图所示.则该溶液中一定含有的离子是( )| A、③⑤⑦ | B、②③⑤⑦ |
| C、①②③⑥⑦ | D、①②③④⑤⑦ |
考点:镁、铝的重要化合物
专题:
分析:向该溶液中加入一定量NaOH溶液的过程中,开始没有沉淀,说明溶液呈酸性,则一定含有大量的H+离子,在酸性溶液中CO32-离子因发生反应生成挥发性气体而不能存在,而后会有沉淀,能够生成沉淀的是①Al3+,②Mg2+,③Fe3+,④Fe2+中的一种或几种,但是氢氧化铝能溶于过量的碱中,所以一定没有铝离子,结合溶液的电中性和Fe2+离子的还原性以及NO3-离子的氧化性做进一步的推断.
解答:
解:向该溶液中加入一定量 NaOH溶液的过程中,开始没有沉淀,说明溶液呈酸性,则一定含有大量的H+离子,在酸性溶液中CO32-离子分别与H+离子反应生成CO2气体而不能存在,根据溶液的电中性可知一定含有阴离子,则只有NO3-离子符合,含硝酸根离子、氢离子,即相当于硝酸存在,亚铁离子因为和硝酸之间发生氧化还原反应一定不能存在,而后随着氢氧化钠的加入会有沉淀,能够生成沉淀的是①Al3+,②Mg2+,③Fe3+中的一种或几种,但是氢氧化铝能溶于过量的碱中,沉淀量会出现减小的迹象,但是没有出现,所以一定没有Al3+,根据沉淀量达到最大消耗氢氧化钠的量是4mol,1mol铁离子能消耗3mol氢氧化钠,可以知道一定含有镁离子,综上可知一定含有的离子是:②Mg2+,③Fe3+,⑤H+,⑦NO3-.
故选B.
故选B.
点评:本题考查常见离子的检验,注意从反应的现象推断离子的存在性,把握物质的性质和离子的检验方法是做本题的关键,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
可以用来检验酒精中是否含有水的试剂是( )
| A、胆矾 | B、无水硫酸铜 |
| C、金属钠 | D、生石灰 |
生活中常常碰到涉及化学知识的某些问题,下列叙述正确的是( )
①不法商贩运输白菜时用甲醛溶液喷洒保鲜
②蜂蚁叮咬人的皮肤时将分泌物甲酸注入人体,此时可在患处涂抹小苏打或稀氨水
③变质的油脂有难闻的特殊气味,是由于油脂发生了水解反应
④所有的糖类都有甜味,所以糖类是生活中最常见的甜味剂.
⑤人的皮肤在强紫外线的照射下将会失去生理活性.
①不法商贩运输白菜时用甲醛溶液喷洒保鲜
②蜂蚁叮咬人的皮肤时将分泌物甲酸注入人体,此时可在患处涂抹小苏打或稀氨水
③变质的油脂有难闻的特殊气味,是由于油脂发生了水解反应
④所有的糖类都有甜味,所以糖类是生活中最常见的甜味剂.
⑤人的皮肤在强紫外线的照射下将会失去生理活性.
| A、①④⑤ | B、②③④ |
| C、②⑤ | D、全部 |
垃圾无害化处理有利于保护生态环境.下列有关生活垃圾的处理合理的是( )
| A、用厨余垃圾生产沼气 |
| B、废旧塑料露天焚烧防止产生白色污染 |
| C、废旧电池就地填埋 |
| D、用医疗垃圾中的废塑料生产一次性水杯 |
 甲、乙、丙为三种单质,A、B、C 是三种常见化合物,A为淡黄色固体.它们之间的
甲、乙、丙为三种单质,A、B、C 是三种常见化合物,A为淡黄色固体.它们之间的 Na2O2是常见的氧化剂.某化学小组的同学欲通过以下实验确定炭粉与Na2O2反应的产物.
Na2O2是常见的氧化剂.某化学小组的同学欲通过以下实验确定炭粉与Na2O2反应的产物.