题目内容
下列表示对应化学反应的离子方程式正确的是( )
| A、漂白粉露置在空气中失效:ClO-+CO2+H2O=HClO+HCO3- |
| B、向NaAlO2溶液中通入过量CO2:AlO2-+CO2+2H2O=Al(OH)3↓+HCO3- |
| C、向Na2S2O3溶液中通入足量氯气:S2O32-+2Cl2+3H2O=2SO32-+4Cl-+6H+ |
| D、在强碱溶液中次氯酸钠与Fe(OH)3反应生成Na2FeO4:3ClO-+Fe(OH)3=FeO42-+3Cl-+H2O+4H+ |
考点:离子方程式的书写
专题:离子反应专题
分析:A.漂白粉在空气中变质是因为其有效成分次氯酸钙与空气中的二氧化碳反应生成了次氯酸,并且次氯酸见光、受热分解,从而使漂白粉失效;
B.NaAlO2溶液通入过量的二氧化碳,由于碳酸酸性比氢氧化铝强,所以生成氢氧化铝白色沉淀和碳酸氢钠;
C.Na2S2O3中S的化合价为+2,Na2S2O3和氯气反应,可将氯气完全转化为Cl-,生成了硫酸、氯化钠和氯化氢;
D.在强碱溶液中次氯酸钠与Fe(OH)3反应生成Na2FeO4,方程式左右电荷不守恒,且不能由碱生成酸;
B.NaAlO2溶液通入过量的二氧化碳,由于碳酸酸性比氢氧化铝强,所以生成氢氧化铝白色沉淀和碳酸氢钠;
C.Na2S2O3中S的化合价为+2,Na2S2O3和氯气反应,可将氯气完全转化为Cl-,生成了硫酸、氯化钠和氯化氢;
D.在强碱溶液中次氯酸钠与Fe(OH)3反应生成Na2FeO4,方程式左右电荷不守恒,且不能由碱生成酸;
解答:
解:A.Ca(ClO)2是漂白粉中有效成分,漂白粉置于空气中易失效的原因是发生Ca(ClO)2+H2O+CO2=CaCO3↓+2HClO,2HClO
2HCl+O2↑反应,离子方程式为:Ca2++2ClO-+H2O+CO2=CaCO3↓+2HClO,故A错误;
B.向NaAlO2溶液中通入过量CO2,反应生成的是碳酸氢根离子,离子方程式为:AlO2-+CO2+2H2O═Al(OH)3↓+HCO3-,故B正确;
C.硫代硫酸钠与氯气反应生成硫酸、氯化钠和盐酸,反应的化学方程式为:Na2S2O3+4Cl2+5H2O═2NaCl+6HCl+2H2SO4,离子方程式为:S2O32-+4Cl2+5H2O=2SO42-+8Cl-+10H+,故C错误;
D.在强碱溶液中次氯酸钠与Fe(OH)3反应生成Na2FeO4的离子反应为3ClO-+2Fe(OH)3+4OH-=2FeO42-+3Cl-+5H2O,故D错误;
故选B.
| ||
B.向NaAlO2溶液中通入过量CO2,反应生成的是碳酸氢根离子,离子方程式为:AlO2-+CO2+2H2O═Al(OH)3↓+HCO3-,故B正确;
C.硫代硫酸钠与氯气反应生成硫酸、氯化钠和盐酸,反应的化学方程式为:Na2S2O3+4Cl2+5H2O═2NaCl+6HCl+2H2SO4,离子方程式为:S2O32-+4Cl2+5H2O=2SO42-+8Cl-+10H+,故C错误;
D.在强碱溶液中次氯酸钠与Fe(OH)3反应生成Na2FeO4的离子反应为3ClO-+2Fe(OH)3+4OH-=2FeO42-+3Cl-+5H2O,故D错误;
故选B.
点评:本题考查了离子方程式的正误判断,明确判断离子方程式常用方法(1)检查反应能否发生;(2)检查反应物、生成物是否正确;(3)检查各物质拆分是否正确;(4)检查是否符合守恒关系(如:质量守恒和电荷守恒等);(5)检查是否符合原化学方程式,B选项反应生成的是碳酸氢根离子为易错点,题目难度中等.

练习册系列答案
相关题目
下列离子方程式中书写正确的是( )
| A、过氧化钠固体与水反应:2O2-+2H2O=4OH-+O2↑ | ||
B、在H2O2中加入酸性KMnO4溶液:2M
| ||
| C、醋酸溶液与大理石反应:CaCO3+2H+=Ca2++H2O+CO2↑ | ||
| D、次氯酸钙溶液中通入过量二氧化碳:Ca2++2ClO-+H2O+CO2=CaCO3↓+2HClO |
阿佛加德罗常数约为6.02×1023mol-1,下列说法中一定正确的是( )
| A、60gSiO2晶体中含有2×6.02×1023个Si-O键 |
| B、18gD2O(重水)完全电解,转移2×6.02×1023个电子 |
C、720gC60晶体(如图)中含有6.02×1023个晶胞结构单元 |
| D、14g两种烯烃CnH2n和CmH2m混合物,含有共用电子对数目为3×6.02×1023 |
下列离子方程式正确的是( )
| A、钠与水的反应:Na+2H2O=Na++2OH-+H2↑ |
| B、过量的NaHSO4与Ba(OH)2溶液反应:Ba2++2OH-+2H++SO42-═BaSO4↓+2H2O |
| C、硫酸镁溶液跟氢氧化钡溶液反应:SO42-+Ba2+=BaSO4↓ |
| D、碳酸钙溶于醋酸中 CaCO3+2H+=Ca2++H2O+CO2↑ |
下列各组离子可以大量共存,加入括号中试剂,整体可能形成无色澄清溶液的是( )
| A、Na+、NH4+、Fe2+、NO3-(稀硫酸) |
| B、Al3+、K+、HCO3-、NO3-(NaOH溶液) |
| C、NH4+、Ag+、K+、NO3-(NaOH溶液) |
| D、Na+、K+、AlO2-、SiO32-(稀硝酸) |
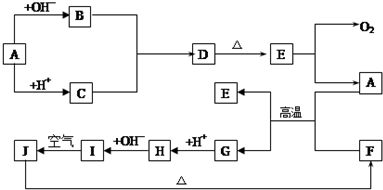

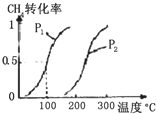 甲醇被称为21世纪的新型燃料,工业上用CH4和H2O为原料通过下列反应①和②,来制备甲醇.
甲醇被称为21世纪的新型燃料,工业上用CH4和H2O为原料通过下列反应①和②,来制备甲醇.