题目内容
设NA为阿伏伽德罗常数的值,下列叙述正确的是( )
| A、11gT2O含有的中子数为6NA |
| B、1molNa2O2与CO2完全反应转移的电子数为2NA |
| C、常温下,0.2L0.5mol/LNH4NO3溶液的氮原子数小于0.2NA |
| D、标准状况下,2.24LH2S全部溶于水所得溶液中HS-和S2-离子数之和为0.1NA |
考点:阿伏加德罗常数
专题:阿伏加德罗常数和阿伏加德罗定律
分析:A、依据n=
计算物质的量,结合质子数+中子数=质量数计算中子数;
B、过氧化钠和二氧化碳反应,过氧化钠中氧元素化合价-1价变化为0价和-2价;
C、溶液中铵根离子水解,但溶液中氮元素守恒;
D、依据溶液中物料守恒分析判断;
| m |
| M |
B、过氧化钠和二氧化碳反应,过氧化钠中氧元素化合价-1价变化为0价和-2价;
C、溶液中铵根离子水解,但溶液中氮元素守恒;
D、依据溶液中物料守恒分析判断;
解答:
解:A、11gT2O物质的量=
=0.5mol,含有的中子数=0.5mol(2×2+8)×NA=6NA,故A正确;
B、1molNa2O2与CO2完全反应,过氧化钠中氧元素化合价-1价变化为0价和-2价,转移的电子数为NA,故B错误;
C、0.2L0.5mol/LNH4NO3溶液中溶质物质的量=0.2L×0.5mol/L=0.1mol,含有的氮原子数等于0.2NA,故C错误;
D、标准状况下,2.24LH2S物质的量=
=0.1mol,全部溶于水所得溶液中H2S、HS-和S2-离子数之和为0.1NA,故D错误;
故选A.
| 11g |
| 22g/mol |
B、1molNa2O2与CO2完全反应,过氧化钠中氧元素化合价-1价变化为0价和-2价,转移的电子数为NA,故B错误;
C、0.2L0.5mol/LNH4NO3溶液中溶质物质的量=0.2L×0.5mol/L=0.1mol,含有的氮原子数等于0.2NA,故C错误;
D、标准状况下,2.24LH2S物质的量=
| 2.24L |
| 22.4L/mol |
故选A.
点评:本题考查了阿伏伽德罗常数的分析应用,主要是氧化还原反应电子转移计算,溶液中元素守恒的分析判断,原子结构中质子数中子数的计算,掌握基础是关键,题目较简单.

练习册系列答案
相关题目
下列化学用语不正确的是( )
A、二氧化碳的电子式: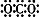 | ||
B、S2-的粒子结构示意图: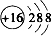 | ||
C、甲烷分子的结构式: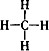 | ||
D、R2+离子核外有a个电子,b个中子,R原子克表示为
|
可逆反应3A(g)?3B+C;△H>0,随着温度的升高,气体的平均相对分子质量有变小的趋势.下列关于B、C两种物质的聚集状态的判断不正确的是( )
| A、B和C可能都是气体 |
| B、B和C一定都是气体 |
| C、若C为固体,则B一定是气体 |
| D、不可能B为固体,C为气体 |
将铝粉和Fe2O3粉末均匀混合,再分成两等份.一份在高温下恰好完全反应后,再溶于1mol?L-1的盐酸中;另一份直接溶于1mol?L-1的盐酸中.前后两种情况下消耗盐酸体积的关系为( )
| A、一样多 |
| B、前者大于后者 |
| C、后者大于前者 |
| D、数据不完整,无法确定 |
某位同学配制一定物质的量浓度的NaOH溶液时,造成所配溶液浓度偏高的原因是( )
| A、所用NaOH已经潮解 |
| B、容量瓶中原有少量蒸馏水 |
| C、加水定容时俯视刻度线 |
| D、用带游码的托盘天平称2.4g NaOH时误用了“左码右物”方法 |
室温下向10mLpH=3的醋酸溶液中加水稀释后,下列说法正确的是( )
| A、溶液中导电粒子的数目减少 | ||
B、溶液中
| ||
| C、醋酸的电离程度变大,c(H+)也增大 | ||
D、溶液中
|
依据元素周期表及元素周期律,下列推断中正确的是( )
| A、同一周期元素的原子,半径越小越容易失去电子 |
| B、ⅠA族元素的金属性比ⅡA族元素的金属性强 |
| C、向氢硫酸溶液中滴入氯水有单质硫生成,可以验证硫元素的非金属性比氯元素弱 |
| D、主族元素的最高正化合价等于该元素原子的核外电子数 |
有关化学用语正确的是( )
| A、乙烯的结构简式:CH2 CH2 |
| B、乙醇的化学式:C2H6O |
C、CCl4的电子式 |
| D、乙酸的结构简式C2H4O2 |
X、Y、Z、W均为短周期元素,它们在元素周期表中的位置如图所示.若Y原子的最外层电子数是次外层电子数的3倍,下列说法正确的是( )
| X | Y | |
| Z | W |
| A、原子半径:W>Z>Y>X |
| B、最高价氧化物对应水化物的酸性:Z>W>X |
| C、Z和W的氢化物中,W的氢化物最稳定 |
| D、X的最高价氧化物对应的水化物能与其气态氢化物发生反应 |