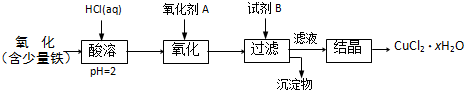
��Ŀ����
��1����ʢ������ͭˮ��Һ���Թ�����백ˮ�������γ�������������Ӱ�ˮ���������ܽ�õ�����ɫ������Һ�����жԴ������˵����ȷ����
A����Ӧ����Һ�в������κγ��������Է�Ӧǰ��Cu2+��Ũ�Ȳ���
B�������ܽ����������ɫ���������[Cu��NH3��4] 2+
C����[Cu��NH3��4] 2+�У���Cu2+�����¶Ե��ӣ�NH3�ṩ�չ��
D����Ӧ�����Һ�м����Ҵ�����Һû�з����仯����Ϊ[Cu��NH3��4] 2+�������Ҵ�������Ӧ
��2��д����1�������е����ӷ���ʽ �� ��
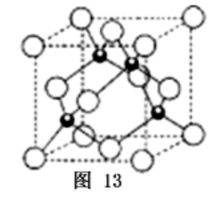
��3��CuԪ����ClԪ���γɵ�һ�����Ӿ���ľ����ṹ��ͼ13��ʾ�����Ȼ���Ļ�ѧʽ�� ______ �����û����ᄃ����ܶ�Ϊ�� g/cm3��NA��ʾ����٤����������þ���������� _cm3��
A����Ӧ����Һ�в������κγ��������Է�Ӧǰ��Cu2+��Ũ�Ȳ���
B�������ܽ����������ɫ���������[Cu��NH3��4] 2+
C����[Cu��NH3��4] 2+�У���Cu2+�����¶Ե��ӣ�NH3�ṩ�չ��
D����Ӧ�����Һ�м����Ҵ�����Һû�з����仯����Ϊ[Cu��NH3��4] 2+�������Ҵ�������Ӧ
��2��д����1�������е����ӷ���ʽ �� ��
��3��CuԪ����ClԪ���γɵ�һ�����Ӿ���ľ����ṹ��ͼ13��ʾ�����Ȼ���Ļ�ѧʽ�� ______ �����û����ᄃ����ܶ�Ϊ�� g/cm3��NA��ʾ����٤����������þ���������� _cm3��
��1��B
��2��Cu2++2NH3��H2O=Cu(OH)2��+2NH4+
Cu(OH)2+4NH3=[Cu(NH3)4]2++2OH-
��3��CuCl 398/��NA
��2��Cu2++2NH3��H2O=Cu(OH)2��+2NH4+
Cu(OH)2+4NH3=[Cu(NH3)4]2++2OH-
��3��CuCl 398/��NA

��ϰ��ϵ�д�
�����Ŀ
 ��1����ͼ��ʾΪ����ʯ����ѧʽΪNa3AlF6���ľ�����ͼ�С�λ�ڴ������嶥������ģ���λ�ڴ��������12������е��8��С����������ģ�����ͼ�С��е�һ�֣�ͼ�С�ֱ�ָ����������
��1����ͼ��ʾΪ����ʯ����ѧʽΪNa3AlF6���ľ�����ͼ�С�λ�ڴ������嶥������ģ���λ�ڴ��������12������е��8��С����������ģ�����ͼ�С��е�һ�֣�ͼ�С�ֱ�ָ����������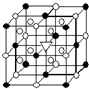 A����1����ͼ��ʾΪ����ʯ����ѧʽΪNa3AlF6���ľ�����ͼ�С�λ�ڴ������嶥������ģ���λ�ڴ��������12������е��8��С����������ģ���ͼ�С��е�һ�֣�ͼ�С�ֱ�ָ����������
A����1����ͼ��ʾΪ����ʯ����ѧʽΪNa3AlF6���ľ�����ͼ�С�λ�ڴ������嶥������ģ���λ�ڴ��������12������е��8��С����������ģ���ͼ�С��е�һ�֣�ͼ�С�ֱ�ָ����������