��Ŀ����
12��ʵ���ҿ��������᳧¯������Ҫ�ɷ�Ϊ���������P����FeS��SiO2�ȣ��Ʊ��������̷���FeSO4•7H2O���������Ļ�ѧʽΪ[Fe2��OH��n��SO4��3-0.5n]m���Ʊ�������ͼ��ʾ������˵������ȷ���ǣ�������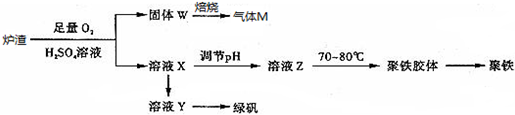
| A�� | ¯����FeS������������ķ�Ӧ�����ӷ���ʽΪ��4FeS+3O2+12H+�T4Fe3++4S��+6H2O | |
| B�� | ��ҺZ��pHӰ�������������������������pHƫС�������¾�����������������ƫ�� | |
| C�� | ����M�ijɷ���SO2��ͨ��˫��ˮ�õ����ᣬ��ѭ��ʹ�� | |
| D�� | ����ҺX�м���������ۣ���ַ�Ӧ����˵õ���ҺY���پ�����Ũ������ȴ�ᾧ�����˵Ȳ���õ��̷� |
���� �����м���ϡ���ᡢͬʱͨ�����������˺õ�����W�к���S��SiO2�������պ�β���к��ж���������ҺX����Fe2��SO4��3��δ��Ӧ�����ᣬ��ҺX�м���Fe�ۣ���Ӧ��ϣ����˵õ���ҺYΪFeSO4��Һ���پ�������Ũ������ȴ�ᾧ�����ˡ�ϴ�ӵȵõ��̷�����ҺX����pH�õ���ҺZ�����ȴٽ�Fe3+��ˮ��õ��������壬�پ�������۳��õ�������ͨ������pH���Կ��������������������ı�����ϵ���Դ˽����⣮
��� �⣺¯������������Һͬʱͨ�������õ�����WΪ������ԭ��Ӧ���ɵ����ʺ�SiO2�ȣ����յõ�����Ϊ����������ҺXΪ����Fe3+���ӵ���Һ��������ҺPH�õ���ҺZ���ȵõ���������ҺX�м�������Ӧ��������������ҺY�������ᾧ�õ������������壬
A��¯����FeS�������������Ӧ����������������ˮ����Ӧ�����ӷ���ʽΪ4FeS+3O2+12H+�T4Fe3++4S��+6H2O����A��ȷ��
B������ҺZ��PHƫС������������ɵ��������ĺ������٣���������ӵĺ���ƫ����ʹ���ĺ������٣���B����
C��¯������������Һͬʱͨ�������õ�����WΪ������ԭ��Ӧ���ɵ����ʺ�SiO2�ȣ�����W���յõ�����Ϊ��������C��ȷ��
D����ҺX�м���������ۣ�������������Һ��Ӧ��������������ͨ������Ũ������ȴ�ᾧ�����������õ��̷������Ͼ����������裬��D��ȷ��
��ѡB��
���� ���⿼���Ϊ�ۺϣ��漰���ʺ����IJⶨ���Ʊ�ʵ�鷽������Ƶ�֪ʶ��������ѧ���ķ�����ʵ�������Ŀ��飬�Ƕ�ѧ���ۺ������Ŀ��飬��Ҫѧ���߱���ʵ�Ļ������ѶȲ���

| A�� | �����ǿ����ڲ���ҩ��ĺϳ� | |
| B�� | ����������Һ�����ڻ���������ɱ�� | |
| C�� | ����ϩ������Ʒ������ʳƷ�İ�װ | |
| D�� | ��ʯ�ҿ�����ʳƷ������ |
| A�� | 2.8g | B�� | 5.6g | C�� | 8.4g | D�� | 11.2g |
| A�� | 3�� | B�� | 4�� | C�� | 5�� | D�� | 6�� |
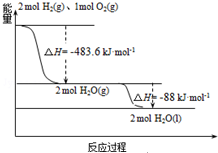 �����õ����ػ��ʹ�õ�����Һ��Ϊȼ�ռ���Һ��Ϊ�������ĸ��ܵ����ƽ�������֪��
�����õ����ػ��ʹ�õ�����Һ��Ϊȼ�ռ���Һ��Ϊ�������ĸ��ܵ����ƽ�������֪����1��H2��g���TH2��l����H1=-0.92kJ•mol-1
��2��O2��g���TO2��l����H2=-6.84kJ•mol-1
����˵����ȷ���ǣ�������
| A�� | H2��g����O2��g����Ӧ����H2O��g������483.6kJ•mol-1 | |
| B�� | ������ȼ����Ϊ��H=-241.8 kJ•mol-1 | |
| C�� | �����Һ��ȼ�յ��Ȼ�ѧ����ʽΪ��2H2��l��+O2��l���T2H2O��g����H=-474.92kJ•mol-1 | |
| D�� | H2O��g��=H2O��l����H=-88kJ•mol-1 |
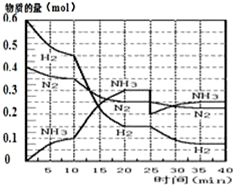 ���ĺϳ�ԭ��Ϊ��N2��g��+3H2��g��?2NH3��g������H=-92.4KJ•mol-1������500�桢20MPaʱ����N2��H2����һ���ݻ�Ϊ2L���ܱ������з�����Ӧ����Ӧ�����и����ʵ����ʵ����仯��ͼ��
���ĺϳ�ԭ��Ϊ��N2��g��+3H2��g��?2NH3��g������H=-92.4KJ•mol-1������500�桢20MPaʱ����N2��H2����һ���ݻ�Ϊ2L���ܱ������з�����Ӧ����Ӧ�����и����ʵ����ʵ����仯��ͼ���ش��������⣺
��1��10min����NH3��ʾ��ƽ����Ӧ����0.005mol/��L��min����
��2����10��20min�ڣ�NH3Ũ�ȱ仯��ԭ�������A��
A�����˴��� B����С�������
C�������¶� D������NH3���ʵ���
��3����1��ƽ���ʱ�䷶ΧΪ��20-25min����1��ƽ�⣺ƽ�ⳣ��K1=$\frac{��\frac{0.3mol}{2L}��^{2}}{��\frac{0.25mol}{2L}����\frac{0.15mol}{2L}��^{3}}$�������ݵı���ʽ����
��4���ڷ�Ӧ������25minʱ��
�����߷����仯��ԭ�����0.1molNH3
�ڴ�ڶ���ƽ��ʱ����ƽ���ƽ�ⳣ��K2����K1������ڡ��������ڡ�����С�ڡ�����
��5���������¡��˹��̵������о��������ڳ��¡���ѹ�����������£�N2�ڴ�������������Fe2O3��TiO2��������ˮ�������з�Ӧ��
N2��g��+3H2O��1��?2NH3��g��+$\frac{3}{2}$O2��g������H=a kJ•mol-1
��һ���о�NH3���������¶ȵĹ�ϵ����ѹ�´ﵽƽ��ʱ��ò���ʵ���������±���
| T/K | 303 | 313 | 323 |
| NH3������/��10-6mol�� | 4.8 | 5.9 | 6.0 |
����֪��N2��g��+3H2��g��?2NH3��g����H=-92.4kJ•mol-1
2H2��g��+O2��g���T2H2O��l����H=-571.6kJ•mol-1
�����µ�����ˮ��Ӧ���ɰ������������Ȼ�ѧ����ʽΪ��2N2��g��+6H2O��l��=4NH3��g��+3O2��g����H=+1530kJ•mol-1��
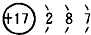 ��
�� ��
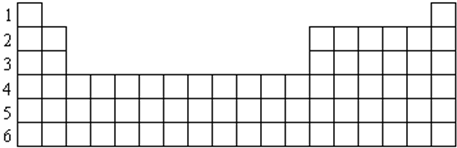
��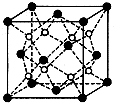 ��A��B��C��D��E����ԭ���������������Ԫ�أ�ԭ��������С��30����A�Ļ�̬ԭ��2p�ܼ���3�������ӣ�C�Ļ�̬ԭ��2p�ܼ���1�������ӣ�E��ԭ�Ӹ��ڲ����������������гɵ����ӣ�D��Eͬ���ڣ��۵�����Ϊ2����
��A��B��C��D��E����ԭ���������������Ԫ�أ�ԭ��������С��30����A�Ļ�̬ԭ��2p�ܼ���3�������ӣ�C�Ļ�̬ԭ��2p�ܼ���1�������ӣ�E��ԭ�Ӹ��ڲ����������������гɵ����ӣ�D��Eͬ���ڣ��۵�����Ϊ2����