题目内容
11.汽车尾气中CO、NOx 以及燃煤废弃中的SO2都是大气污染物,对它们的治理具有重要意义.吸收SO2和NO,获得Na2S2O4和NH4NO3产品的流程图如图1(Ce为铈元素):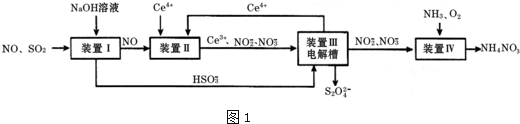
(1)装置Ⅰ中,NaOH溶液吸收SO2也可生成Na2SO3和NaHSO3的混合溶液
①写出NaOH溶液吸收SO2生成等物质的量的Na2SO3和NaHSO3混合溶液时总反应的离子方程式2SO2+3OH-=HSO3-+SO32-+H2O
②已知混合液pH随n(SO32-):n(HSO3-)变化关系如表:
| n(SO32-):n(HSO3-) | 91:9 | 1:1 | 9:91 |
| pH | 8.2 | 7.2 | 6.2 |
(2)装置Ⅱ中,酸性条件下,NO被Ce4+氧化的产物主要是NO3-、NO2-,写出只生成NO2-的离子方程式NO+2H2O+3Ce4+=3Ce3++NO3-+4H+
(3)装置Ⅲ的作用之一是再生Ce4+,其原理如图所示.

①生成的Ce4+从电解槽的a(填字母序号)口流出;
②生成S2O42-的电极反应式为2HSO3-+2H++2e-=S2O42-+2H2O;
(4)已知进入装置Ⅳ的溶液中,NO2-的浓度为a g•L-1,要使1m3该溶液中的NO2-完全转化为NO3-,至少需向装置Ⅳ中通入标准状况下的O2$\frac{5600a}{23}$ L.(用含a代数式表示)
分析 (1)①NaOH溶液吸收SO2生成等物质的量的Na2SO3和NaHSO3混合溶液时,由原子守恒可知NaOH与二氧化硫的物质的量比为3:2;
②当混合液中n(SO32-):n(HSO3-)=1:1时,由表格中pH=7.2可知,溶液为碱性,结合电荷守恒分析;
(2)NO被氧化为硝酸根,Ce4+被还原为Ce3+,酸性环境,缺氧补水,缺氢补氢离子完成方程式;
(3)①生成Ce4+为氧化反应,发生在阳极上,连接电源正极,因此从a口流出;
②反应物是HSO3-被还原成S2O42-,得到电子;
(4)NO2-的浓度为a g•L-1,要使1m3该溶液中的NO2-完全转化为NH4NO3,则失去电子数目是:1000×(5-3)a/46,设消耗标况下氧气的体积是V,则得电子数目是:V÷22.4×2×(2-0),根据电子守恒进行计算.
解答 解:(1)①NaOH溶液吸收SO2生成等物质的量的Na2SO3和NaHSO3混合溶液时,由原子守恒可知NaOH与二氧化硫的物质的量比为3:2,离子反应为2SO2+3OH-=HSO3-+SO32-+H2O,
故答案为:2SO2+3OH-=HSO3-+SO32-+H2O;
②当混合液中n(SO32-):n(HSO3-)=1:1时,由表格中pH=7.2可知,溶液为碱性,c(OH-)>c(H+),由电荷守恒可知,c(H+)+c(Na+)=c(HSO3-)+2c(SO32-)+c(OH-),则(Na+)>c(HSO3-)+2c(SO32-),故答案为:>;
(2)NO被氧化为硝酸根,Ce4+被还原为Ce3+,酸性环境,缺氧补水,缺氢补氢离子,所以离子方程式为NO+2H2O+3Ce4+=3Ce3++NO3-+4H+,
故答案为:NO+2H2O+3Ce4+=3Ce3++NO3-+4H+;
(3)①生成Ce4+为氧化反应,发生在阳极上,连接电源正极,因此从a口流出,故答案为:a;
②反应物是HSO3-被还原成S2O42-,得到电子,电极反应式为2HSO3-+2H++2e-=S2O42-+2H2O,
故答案为:2HSO3-+2H++2e-=S2O42-+2H2O;
(4)NO2-的浓度为a g•L-1,要使1m3该溶液中的NO2-完全转化为NH4NO3,则失去电子为$\frac{1000a×(5-3)}{46}$
mol,设消耗标况下氧气的体积是V,则得电子为$\frac{V}{22.4}$mol×2×(2-0),根据电子守恒可知$\frac{1000a×(5-3)}{46}$=$\frac{V}{22.4}$mol×2×(2-0),解得V=$\frac{5600a}{23}$L,故答案为:$\frac{5600a}{23}$.
点评 本题考查较综合,涉及离子浓度比较、离子反应及电化学、氧化还原反应计算等,注重高频考点的考查,综合考查化学反应原理,把握习题中的信息守恒法应用为解答的关键,注意知识的迁移应用,题目难度中等.

 超能学典应用题题卡系列答案
超能学典应用题题卡系列答案| A. | 10℃时pH=12的Na0H溶液与40℃时pH=12的Na0H溶液中:c(OH-)相等 | |
| B. | 25℃时pH=10的NaOH溶液与pH=10的氨水中:c(Na+)═c(NH4+) | |
| C. | 物质的量浓度相等的CH3COOH和CH3COONa溶液等体积混合:c(CH3COO-)+2c(OH-)═2c(H+)+c(CH3COOH) | |
| D. | 向10mLpH=12的Na0H溶液中滴加pH=2的HA溶液达中性:则混合液体积V总≥20mL |
| A. | 氯化钡 | B. | 盐酸 | C. | 氯化钡和盐酸 | D. | 氯化钡和硫酸 |
①H2O2+2KI+H2SO4═I2+K2SO4+2H2O;
②H2O2+I2═2HIO;
③H2O2+2HIO═I2+O2↑+2H2O.
下列有关该反应的说法正确的是( )
| A. | 反应速率与SO42-浓度有关 | |
| B. | 催化剂能加快化学反应速率,但反应物所需活化能不变 | |
| C. | 碘单质是过氧化氢分解的催化剂 | |
| D. | 与一定量H2O2反应的KI溶液浓度越大,反应速率越慢 |
 .
.
 .
. .
.