题目内容
(1)化学实验操作的“先”与“后”,对化学实验结果、师生安全等具有十分重要的意义.我们在进行化学实验时,若遇到下列情况,应如何操作.
①给试管中的药品加热,必须先 ,后集中加热.
②点燃可燃性气体(如H2、CO等)时,都要先 ,后点燃.
③H2还原CuO实验结束时,要先 ,后移去导气管.
(2)要分离下列四组混合物:a.饱和食盐水与沙子 b.从KNO3和NaCl的混合溶液中获得KNO3 c.水和汽油的混合物 d.CCl4液体与甲苯液体的混合物(已知CCl4与甲苯互溶,沸点分别为76.75℃和110.6℃)
①分离a、b的操作分别为 、 .
②上述四组分离时需使用酒精灯的有 和 (填序号).
③分离c时所使用仪器中有一种在其他组分分离时无需使用,这种仪器是 .
①给试管中的药品加热,必须先
②点燃可燃性气体(如H2、CO等)时,都要先
③H2还原CuO实验结束时,要先
(2)要分离下列四组混合物:a.饱和食盐水与沙子 b.从KNO3和NaCl的混合溶液中获得KNO3 c.水和汽油的混合物 d.CCl4液体与甲苯液体的混合物(已知CCl4与甲苯互溶,沸点分别为76.75℃和110.6℃)
①分离a、b的操作分别为
②上述四组分离时需使用酒精灯的有
③分离c时所使用仪器中有一种在其他组分分离时无需使用,这种仪器是
考点:化学实验操作的先后顺序,物质的分离、提纯和除杂
专题:化学实验基本操作
分析:(1)①给试管中的药品加热要先预热再集中加热,防止试管炸裂;
②可燃性气体与空气的浓度存在爆炸极限,点燃之前定要验纯;
③H2还原CuO实验步骤、注意事项进行分析判断;
(2)①沙子不溶于水,而食盐溶于水;NaCl的溶解度受温度影响不大,而KNO3的溶解度受温度影响大;
②结晶法、蒸馏法分离混合物需要酒精灯;
③水和汽油的混合物分层,利用分液操作分离.
②可燃性气体与空气的浓度存在爆炸极限,点燃之前定要验纯;
③H2还原CuO实验步骤、注意事项进行分析判断;
(2)①沙子不溶于水,而食盐溶于水;NaCl的溶解度受温度影响不大,而KNO3的溶解度受温度影响大;
②结晶法、蒸馏法分离混合物需要酒精灯;
③水和汽油的混合物分层,利用分液操作分离.
解答:
解:(1)①给试管中的药品加热时,为防止试管底部受热不均匀造成试管炸裂,应先进行预热,后集中加热;
故答案为:预热;
②点燃可燃性气体(如H2、CO等)时,要先检验气体的纯度,后点燃,以防止发生爆炸;
故答案为:检验气体纯度;
③H2还原CuO实验结束时,为防止生成的铜被氧化,实验结束时要先停止加热,再撤去通H2的导管;
故答案为:移去酒精灯;
(2)a.饱和食盐水与沙子,沙子不溶于水,则利用过滤分离,不需要加热;
b.NaCl的溶解度受温度影响不大,而KNO3的溶解度受温度影响大,则利用冷却结晶法分离,溶解时需要加热得到热饱和溶液;
c.水和汽油的混合物,分层,利用分液法分离,需要分液漏斗;
d.CCl4液体与甲苯液体的混合物,混溶,但沸点不同,利用蒸馏法分离,需要酒精灯加热,
①由上述分析可知,分离a、b的操作分别为过滤、结晶、
故答案为:过滤;结晶;
②由上述分析可知,分离时需使用酒精灯的有b、d;
故答案为:b;d;
③由上述分析可知,分离c时使用的主要仪器是分液漏斗;
故答案为:分液漏斗.
故答案为:预热;
②点燃可燃性气体(如H2、CO等)时,要先检验气体的纯度,后点燃,以防止发生爆炸;
故答案为:检验气体纯度;
③H2还原CuO实验结束时,为防止生成的铜被氧化,实验结束时要先停止加热,再撤去通H2的导管;
故答案为:移去酒精灯;
(2)a.饱和食盐水与沙子,沙子不溶于水,则利用过滤分离,不需要加热;
b.NaCl的溶解度受温度影响不大,而KNO3的溶解度受温度影响大,则利用冷却结晶法分离,溶解时需要加热得到热饱和溶液;
c.水和汽油的混合物,分层,利用分液法分离,需要分液漏斗;
d.CCl4液体与甲苯液体的混合物,混溶,但沸点不同,利用蒸馏法分离,需要酒精灯加热,
①由上述分析可知,分离a、b的操作分别为过滤、结晶、
故答案为:过滤;结晶;
②由上述分析可知,分离时需使用酒精灯的有b、d;
故答案为:b;d;
③由上述分析可知,分离c时使用的主要仪器是分液漏斗;
故答案为:分液漏斗.
点评:可燃性气体点燃前一定要检验纯度,可防止爆炸;注意物质分离、提纯方法的选择和应用,题目难度不大.

练习册系列答案
 全优点练单元计划系列答案
全优点练单元计划系列答案
相关题目
实验室中配制250mL 0.10mo1?L-1 NaOH溶液时,必须使用到的玻璃仪器是( )
A、 锥形瓶 |
B、 试管 |
C、 分液漏斗 |
D、 容量瓶 |
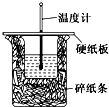 50mL 0.50mol/L盐酸与50mL 0.55mol/L NaOH溶液在如图所示的装置中进行中和反应.通过测定反应过程中所放出的热量可计算中和热.回答下列问题:
50mL 0.50mol/L盐酸与50mL 0.55mol/L NaOH溶液在如图所示的装置中进行中和反应.通过测定反应过程中所放出的热量可计算中和热.回答下列问题: