题目内容
9.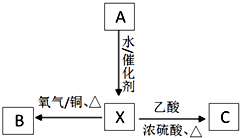 A为标准状况下密度为1.25g•L-1的常见气态烃.有关物质的转化关系如图:请回答:
A为标准状况下密度为1.25g•L-1的常见气态烃.有关物质的转化关系如图:请回答:(1)X分子中官能团的名称是羟基.
(2)向装有银氨溶液的试管中加入3滴B溶液,振荡后水浴加热.写出加热后观察到的现象试管内壁析出光亮的银镜.
(3)X转化为C的化学方程式是CH3COOH+CH3CH2OH$→_{△}^{浓硫酸}$CH3COOCH2CH3+H2O.
分析 A在标准状况下的密度为1.25g/L,其摩尔质量为1.25g/L×22.4L/mol=28g/mol,故A为CH2=CH2,乙烯能与水反应生成X为乙醇,乙醇能与氧气反应生成乙醛,乙醇能与乙酸反应生成乙酸乙酯.
(1)X为乙醇;
(2)醛基能发生银镜反应;
(3)乙醇能与乙酸反应生成乙酸乙酯.
解答 解:A在标准状况下的密度为1.25g/L,其摩尔质量为1.25g/L×22.4L/mol=28g/mol,故A为CH2=CH2,乙烯能与水反应生成X为乙醇,乙醇能与氧气反应生成乙醛,乙醇能与乙酸反应生成乙酸乙酯.
(1)X为乙醇,官能团为羟基,故答案为:羟基;
(2)醛基能发生银镜反应,生成银镜,故答案为:试管内壁析出光亮的银镜;
(3)乙醇能与乙酸反应生成乙酸乙酯,化学方程式是CH3COOH+CH3CH2O$→_{△}^{浓硫酸}$CH3COOCH2CH3+H2O,故答案为:CH3COOH+CH3CH2OH$→_{△}^{浓硫酸}$CH3COOCH2CH3+H2O.
点评 本题考查有机物的推断与合成,涉及醇、醛、羧酸、酯、烯烃的性质等,难度不大,推断A为乙烯是关键,注意掌握官能团的性质与转化.

练习册系列答案
相关题目
19.根据下列热化学方程式:
(1)C(s)+O2(g)═CO2(g)△H1=-393.5kJ•mol-1;
(2)H2(g)+$\frac{1}{2}$O2(g)═H2O(l)△H2=-285.8kJ•mol-1;
(3)CH3COOH(l)+2O2(g)═2CO2(g)+2H2O(l)△H3=-870.3kJ•mol-1
可以计算出2C(s)+2H2(g)+O2(g)═CH3COOH(l)的反应热为( )
(1)C(s)+O2(g)═CO2(g)△H1=-393.5kJ•mol-1;
(2)H2(g)+$\frac{1}{2}$O2(g)═H2O(l)△H2=-285.8kJ•mol-1;
(3)CH3COOH(l)+2O2(g)═2CO2(g)+2H2O(l)△H3=-870.3kJ•mol-1
可以计算出2C(s)+2H2(g)+O2(g)═CH3COOH(l)的反应热为( )
| A. | △H=244.1 kJ•mol-1 | B. | △H=-488.3 kJ•mol-1 | ||
| C. | △H=-996.6 kJ•mol-1 | D. | △H=996.6 kJ•mol-1 |
20. 制备纯净的液态无水四氯化锡(SnCl4易挥发形成气体,极易发生水解)的反应为:Sn+2Cl2$\frac{\underline{\;\;△\;\;}}{\;}$SnCl4,Sn也可与HCl反应生成SnCl2,已知:
制备纯净的液态无水四氯化锡(SnCl4易挥发形成气体,极易发生水解)的反应为:Sn+2Cl2$\frac{\underline{\;\;△\;\;}}{\;}$SnCl4,Sn也可与HCl反应生成SnCl2,已知:
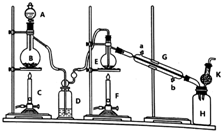
某同学设计的相关实验装置图如图:
(l)A中浓盐酸与B中物质进行反应,化学方程式为MnO2+4HCl(浓)$\frac{\underline{\;\;△\;\;}}{\;}$MnCl2+Cl2↑+2H2O.
(2)D中的试剂为浓硫酸,目的是除去H2O.
(3)G中冷却水的进水位置为b(填字母).
(4)为避免E中副反应的发生,对装置需要改进的措施是BD间增加盛饱和食盐水的洗气瓶.
(5)K中固体物质的作用为防止空气中水分进入.
(6)当要结束实验时,不能首先进行的操作是③.①关闭A的活塞 ②停止F的加热 ③停止G的通水.
(7)若将B中的固体换成Sn,并将除A和B以外的器皿去掉,反应可制备SnCl2.
(8)实验结束后,若得到的SnCl4为13.05g,至少消耗8.70g MnO2.为了避免尾气污染,需要改进的措施是在K后面加尾气吸收装置.
 制备纯净的液态无水四氯化锡(SnCl4易挥发形成气体,极易发生水解)的反应为:Sn+2Cl2$\frac{\underline{\;\;△\;\;}}{\;}$SnCl4,Sn也可与HCl反应生成SnCl2,已知:
制备纯净的液态无水四氯化锡(SnCl4易挥发形成气体,极易发生水解)的反应为:Sn+2Cl2$\frac{\underline{\;\;△\;\;}}{\;}$SnCl4,Sn也可与HCl反应生成SnCl2,已知:| 物质 | 摩尔质量/(g•mol-1) | 熔点/℃ | 沸点/℃ |
| Sn | 119 | 232 | 2260 |
| SnCl2 | 190 | 246.8 | 623 |
| SnCl4 | 261 | -30.2 | 114.1 |
| MnO2 | 87 | 535(分解) | - |
(l)A中浓盐酸与B中物质进行反应,化学方程式为MnO2+4HCl(浓)$\frac{\underline{\;\;△\;\;}}{\;}$MnCl2+Cl2↑+2H2O.
(2)D中的试剂为浓硫酸,目的是除去H2O.
(3)G中冷却水的进水位置为b(填字母).
(4)为避免E中副反应的发生,对装置需要改进的措施是BD间增加盛饱和食盐水的洗气瓶.
(5)K中固体物质的作用为防止空气中水分进入.
(6)当要结束实验时,不能首先进行的操作是③.①关闭A的活塞 ②停止F的加热 ③停止G的通水.
(7)若将B中的固体换成Sn,并将除A和B以外的器皿去掉,反应可制备SnCl2.
(8)实验结束后,若得到的SnCl4为13.05g,至少消耗8.70g MnO2.为了避免尾气污染,需要改进的措施是在K后面加尾气吸收装置.
17.下列说法不正确的是( )
| A. | Cl2能使湿润的有色布条褪色,所以Cl2具有漂白性 | |
| B. | 红热的铁丝在Cl2中剧烈燃烧,反应生成FeCl3 | |
| C. | 利用溴单质的氧化性可以把碘离子转化为碘单质 | |
| D. | 实验室常用NaOH溶液吸收多余的Cl2以避免污染 |
4.下列说法不正确的是( )
| A. | 石油的裂解可以提高汽油等轻质油的质量和产量 | |
| B. | 在一定条件下煤和氢气作用得到液体燃料的过程是煤的液化途径之一 | |
| C. | 葡萄糖、淀粉、油脂在一定条件下都能发生水解反应 | |
| D. | 往蛋白质溶液中加入饱和硫酸铵溶液,产生的沉淀再加水又可溶解 |
1.可以用AG来表示溶液的酸度.AG与pH的关系如图:则下列说法正确的是( )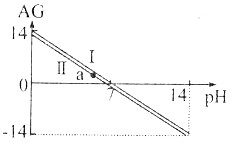

| A. | AG与pH的关系一定是AG=14-2pH | |
| B. | 直线Ⅰ和Ⅱ是因溶液的温度不同引起的,且T(Ⅰ)>T(Ⅱ) | |
| C. | AG=0时,溶液一定呈中性 | |
| D. | a点的溶液中可以有大量Na+、Cl-、Fe3+存在 |
16.下列叙述正确的是( )
| A. | 加入稀盐酸产生无色气体,该气体能使澄清石灰水变浑浊,则原溶液中一定有CO32- | |
| B. | 鉴别碳酸钠溶液和碳酸氢钠溶液,可以用稀CaCl2 溶液 | |
| C. | 做焰色反应时,每次实验要将铂丝用水洗干净,再蘸取其他物质在灯焰上灼烧 | |
| D. | 加入氯化钡溶液有白色沉淀产生,再加盐酸,沉淀不消失,则原溶液中一定有SO42- |