题目内容
下列有关主族元素形成的离子的叙述正确的是( )
| A、单核阳离子的电子层结构(除氢外)一定与上一周期稀有气体原子相同 |
| B、单核阳离子的电子层数一定比其他原子的电子层数少 |
| C、单核阴离子的半径一定比其原子半径大 |
| D、单核阴离子最外层一定是八电子结构 |
考点:元素周期表的结构及其应用
专题:
分析:主族元素形成的离子中
A、单核阳离子的电子层结构(除氢外)一定与上一周期稀有气体原子相同,例如第ⅣA族中的Pb2+离子;
B、单核阳离子的电子层数不一定比其原子的电子层数少,也可能相等,例如第ⅣA族中的Pb2+离子;
C、在电子层数和核电荷数相等时,最外层电子数越多,判断越大;
D、H-的最外层只有两个电子;
A、单核阳离子的电子层结构(除氢外)一定与上一周期稀有气体原子相同,例如第ⅣA族中的Pb2+离子;
B、单核阳离子的电子层数不一定比其原子的电子层数少,也可能相等,例如第ⅣA族中的Pb2+离子;
C、在电子层数和核电荷数相等时,最外层电子数越多,判断越大;
D、H-的最外层只有两个电子;
解答:
解:A、单核阳离子的电子层结构(除氢外)一定与上一周期稀有气体原子相同,例如过渡元素中的部分离子,故A错误;
B、单核阳离子的电子层数不一定比其原子的电子层数少,也可能相等,故B错误;
C、在电子层数和核电荷数相等时,最外层电子数越多,判断越大,故C正确;
D、H-的最外层只有两个电子,故D错误;
故选C.
B、单核阳离子的电子层数不一定比其原子的电子层数少,也可能相等,故B错误;
C、在电子层数和核电荷数相等时,最外层电子数越多,判断越大,故C正确;
D、H-的最外层只有两个电子,故D错误;
故选C.
点评:本题主考查了元素原子结构的有关知识,熟练掌握主族元素的离子结构是解本题关键,题目难度不大.

练习册系列答案
相关题目
2014年6月5日为世界环境日,主题为“提高你的呼声而不是海平面”,提倡节能减排,以下措施中不能体现这一思想的是( )
| A、在电解铝工业中添加冰晶石 |
| B、大力发展火电,缓解用电紧张 |
| C、开发太阳能、风能、氢能等清洁能源 |
| D、研制出性能优良的催化剂,降低反应所需温度 |
25℃时,水的电离达到平衡:H2O?H++OH-,下列叙述正确的是( )
A、 表示的粒子不会对水的电离平衡产生影响 表示的粒子不会对水的电离平衡产生影响 |
B、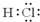 表示的物质加入水中,促进水的电离,c(H+)增大 表示的物质加入水中,促进水的电离,c(H+)增大 |
C、25℃时, 表示的微粒加入水中,促进水的电离,Kw不变 表示的微粒加入水中,促进水的电离,Kw不变 |
| D、水的电离程度只与温度有关,温度越高,电离程度越大 |
下列叙述正确的是( )
| A、用简易量热计能粗略测量稀盐酸和烧碱稀溶液中和反应的反应热 |
| B、pH<7的溶液不可能呈中性 |
| C、所有化学反应的反应热均可通过实验直接测定 |
| D、铅酸蓄电池充电和放电时的所发生的反应互为可逆反应 |
钠元素与硅元素最本质的区别是( )
| A、质子数不同 |
| B、相对原子质量不同 |
| C、中子数不同 |
| D、最外层电子数不同 |
下列化学用语正确的是( )
| A、乙酸的结构简式:C2H4O2 |
| B、氮气的结构式:N≡N |
C、硫化氢的电子式: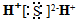 |
D、氯原子的结构示意图: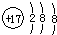 |
下列反应能用CO32-+2H+═CO2↑+H2O表示的是( )
| A、Na2CO3+H2SO4═Na2SO4+CO2↑+H2O |
| B、CaCO3+2HCl═CaCl2+CO2↑+H2O |
| C、KHCO3+HCl═KCl+CO2↑+H2O |
| D、BaCO3+2HNO3═Ba(NO3 )2+CO2↑+H2O |