题目内容
15.NH3在与酸反应、与盐溶液反应时体现出碱性外,还有其它性质.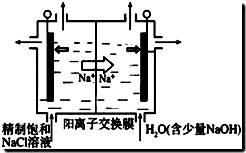
( I)(1)同学甲在百度中查阅工业制硝酸的原理:硝酸工业与合成氨工业密接相关,氨氧化法是工业生产中制取硝酸的主要途径,其主要流程是将氨和空气的混合气(氧:氮≈2:1)通入灼热(760~840℃)的铂铑合金网,在合金网的催化下,氨被氧化成一氧化氮(NO).生成的一氧化氮利用反应后残余的氧气继续氧化为二氧化氮,随后将二氧化氮通入水中制取硝酸.稀硝酸、浓硝酸、发烟硝酸的制取在工艺上各不相同.反应在高温高压条件下进行.同学乙认为只要增大氧气的含量,就可以直接氧化得到NO2,再制备硝酸.请结合你所学习的化学知识,谈谈实际生产中的合理性.已知:2NO与O2反应生成2NO2是可逆反应.氨和空气的混合气在合金网的催化下,氨被氧化成一氧化氮(NO),氧气继续氧化为二氧化氮,反应增大氧气的含量,可以促使化学反应正向移动,从而提高硝酸的产率
(2)工业上,NaNH2用于制取靛青染料;LiNH2主要用于有机合成和药物制造,是具有良好前景的储氢材料.科学家在液氨中加入金属钠或金属锂制备NaNH2和LiNH2,试写出制备LiNH2反应方程式:Li+2NH3=LiNH2+2H2,NH3表现氧化性.
(3)已知NH3与Cl2在一定条件下能发生反应,其中N元素被氧化为游离态,实际反应中其产物随着n(NH3):n(Cl2)的比发生变化,经测定,产物中n(HCl):n(NH4Cl)=1:1时,则n(NH3):n(Cl2)=5:3,整个反应过程被氧化的N与未被氧化的N物质的量之比为2:3结合以上信息,请写出工业上检验氯气管道是否漏气的方法及现象:取浓氨水洒于管道口,产生白烟,证明此处漏气
( II)二氧化氯(ClO2)为一种黄绿色气体,是国际上公认的高效、广谱、快速、安全的杀菌消毒剂.
(1)目前已开发出用电解法制取ClO2的新工艺.
①如图示意用石墨做电极,在一定条件下电解饱和食盐水制取ClO2.写出阳极产生ClO2的电极反应式:Cl--5e-+2H2O=ClO2↑+4H+.
②电解一段时间,当阴极产生的气体体积为112mL(标准状况)时,停止电解.通过阳离子交换膜的阳离子的物质的量为0.01mol;用平衡移动原理解释阴极区pH增大的原因在阴极发生2H++2e-=H2↑,H+浓度减小,使得H2O?OH-+H+的平衡向右移动,OH-浓度增大,pH增大.
(2)ClO2对污水中CN-有明显的去除效果.某工厂污水中含CN- a mg/L,现用ClO2将CN-氧化,只生成两种常见气体,其离子反应方程式为2ClO2+2CN-=N2↑+2CO2↑+2Cl-;处理100m3这种污水,至少需要ClO2$\frac{50a}{13}$mol.
分析 ( I)、(1)根据化学平衡移动原理:增加反应物的浓度可以促使化学平衡正向移动,从而增加反应产物的量;
(2)根据信息:在液氨中加入金属钠或金属锂可以制备NaNH2和LiNH2来书写化学方程式,据元素的化合价确定物质的性质;
(3)根据反应物是氨气和氯气,产物是等物质的量的氯化氢和氯化铵,结合元素守恒、质量守恒来书写方程式即可;被氧化的元素化合价升高,被还原的元素化合价降低,根据产物确定现象;
( II)、(1)①由题意可知,氯离子放电生成ClO2,由元素守恒可知,有水参加反应,同时生成氢离子;
②在阴极发生2H++2e-=H2↑,通过阳离子交换膜的阳离子为+1价离子,根据n=$\frac{V}{Vm}$计算氢气的物质的量,根据电子转移守恒计算阳离子的物质的量,电解中H+浓度减小,使得H2O?OH-+H+的平衡向右移动;
(2)ClO2将CN-氧化,只生成两种气体,应生成氮气与二氧化碳,同时生成氯离子;根据方程式计算需要ClO2的物质的量.
解答 解:(1)氨和空气的混合气在合金网的催化下,氨被氧化成一氧化氮(NO),增加氧气的量,氧气继续氧化NO为二氧化氮,同时2NO与O2反应生成2NO2是可逆反应反应,所以增大氧气的含量,可以促使化学反应正向移动,从而提高硝酸的产率,
故答案为:氨和空气的混合气在合金网的催化下,氨被氧化成一氧化氮(NO),氧气继续氧化为二氧化氮,反应增大氧气的含量,可以促使化学反应正向移动,从而提高硝酸的产率.
(2)在液氨中加入金属锂,会发生反应:Li+2NH3=LiNH2+2H2,据此制备制备LiNH2,氨气中氢元素的化合价降低,所以是氧化剂,故答案为:Li+2NH3=LiNH2+2H2;
氧化;
(3)NH3与Cl2在一定条件下能发生反应,产物中n(HCl):n(NH4Cl)=1:时,根据电子守恒,得到发生的反应为:5NH3+3Cl2=3HCl+3NH4Cl+N2,则n(NH3):n(Cl2)=5:3,整个反应过程被氧化的N与未被氧化的N物质的量之比,2:3,工业上检验氯气管道是否漏气的方法及现象:取浓氨水洒于管道口,产生白烟,证明此处漏气,故答案为:5:3;2:3;取浓氨水洒于管道口,产生白烟,证明此处漏气;
( II)、(1)①由题意可知,氯离子放电生成ClO2,由元素守恒可知,有水参加反应,同时生成氢离子,电极反应式为:Cl--5e-+2H2O=ClO2↑+4H+,
故答案为:Cl--5e-+2H2O=ClO2↑+4H+;
②在阴极发生2H++2e-=H2↑,氢气的物质的量为$\frac{0.112L}{22.4L/mol}$=0.005mol,通过阳离子交换膜的阳离子为+1价离子,故交换膜的阳离子的物质的量为0.005mol×2=0.01mol,电解中阴极H+浓度减小,使得H2O?OH-+H+的平衡向右移动,溶液的pH增大,
故答案为:0.01;在阴极发生2H++2e-=H2↑,H+浓度减小,使得H2O?OH-+H+的平衡向右移动,OH-浓度增大,pH增大;
(2)ClO2将CN-氧化,只生成两种气体,应生成氮气与二氧化碳,同时生成氯离子,反应离子方程式为:2ClO2+2CN-=N2↑+2CO2↑+2Cl-,
100m3废水中CN-质量=100m3×ag/m3=100ag,CN-的物质的量为$\frac{100ag}{26g/mol}$=$\frac{50a}{13}$mol,由方程式可知,至少需要ClO2的物质的量=$\frac{50a}{13}$mol,
故答案为:2ClO2+2CN-=N2↑+2CO2↑+2Cl-;$\frac{50a}{13}$mol.
点评 本题考查氧化还原反应、常用化学用语、电解原理、化学计算等,题目难度中等,电解反应是难点、易错点,是对学生综合能力的考查,需要学生具有扎实的基础与分析解决问题的能力.

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
| A. | 产物B的状态只能为固态或液态 | |
| B. | 平衡时,单位时间内n(A)消耗:n(C)消耗=1:1 | |
| C. | 保持体积不变,向平衡体系中加入A,平衡向正反应方向移动 | |
| D. | 若开始时向容器中加入1 mol B和1 mol C,达到平衡时放出热量Q |
 合成它的单体可能有( )
合成它的单体可能有( )①邻苯二甲酸(
 ) ②丙烯醇(CH2═CH-CH2OH)
) ②丙烯醇(CH2═CH-CH2OH) ③丙烯 ④乙烯 ⑤邻苯二甲酸甲酯 ⑥甲醛.
| A. | ①② | B. | ③④ | C. | ④⑤ | D. | ④⑤⑥ |
| 选项 | 实验操作 | 现象 | 结论 |
| A | 在酒精灯上加热铝箔 | 铝箔熔化但不滴落 | 熔点:铝>氧化铝 |
| B | 某酸雨试样中加入Ba(OH)2溶液 | 产生白色沉淀 | 酸雨试样中只含SO42- |
| C | 用玻璃棒蘸取浓硫酸点到蓝色石蕊试纸上 | 试纸变黑 | 浓硫酸具有脱水性 |
| D | 食用加碘盐加入食醋和KI溶液,再加入CCl4振荡,静置 | 下层呈紫红色 | 该食用加碘盐含有KIO3 |
| A. | A | B. | B | C. | C | D. | D |
| A. | 高温下二氧化硅与碳酸钠反应放出二氧化碳,说明硅酸(H2SiO3)的酸性比碳酸强 | |
| B. | 陶瓷、玻璃、水泥容器都能贮存氢氟酸 | |
| C. | 石灰抹墙、水泥砌墙的硬化过程原理不相同 | |
| D. | 硫酸钠溶液、烧碱溶液、硝酸溶液、浓硫酸四种溶液均能用带玻璃塞的试剂瓶保存 |
 .
.
 .
.