题目内容
6.DAP是电器部件和仪表部件中常用的一种高分子化合物,它的结构简式为: 合成它的单体可能有( )
合成它的单体可能有( )①邻苯二甲酸(
 ) ②丙烯醇(CH2═CH-CH2OH)
) ②丙烯醇(CH2═CH-CH2OH) ③丙烯 ④乙烯 ⑤邻苯二甲酸甲酯 ⑥甲醛.
| A. | ①② | B. | ③④ | C. | ④⑤ | D. | ④⑤⑥ |
分析 凡链节中主碳链为2个碳原子,分别将两个半键闭合即得单体,然后根据获得该高分子化合物的单体找出合成该单体的有机物的结构简式.
解答 解:高分子材料DAP的结构简式为: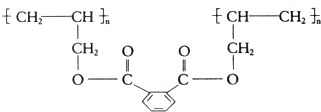 ,将两个半键闭合可得其单体结构简式为:
,将两个半键闭合可得其单体结构简式为: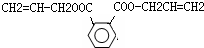 ,合成
,合成 需要用
需要用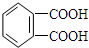 (①邻苯二甲酸)和CH2=CH-CH2-OH(②丙烯醇)发生酯化反应即可,
(①邻苯二甲酸)和CH2=CH-CH2-OH(②丙烯醇)发生酯化反应即可,
故选A.
点评 本题考查加聚产物找单体的方法和酯化反应,题目难度中等,注意凡链节中主碳链为2个碳原子,分别将两个半键闭合即得单体.

练习册系列答案
相关题目
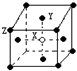
17.下列物质分子的几何构型为正四面体的是( )
| A. | CH4 | B. | NH3 | C. | H2O | D. | CO2 |
14.下列叙述中,不属于核外电子的特点的是( )
| A. | 质量很小 | B. | 运动范围很小 | ||
| C. | 运动速率很快 | D. | 有确定的运动轨道 |
11.人类利用无机物合成的第一种有机物是( )
| A. | 电石气 | B. | 甲烷 | C. | 尿素 | D. | 醋酸 |