题目内容
14. 某温度时,在2L的密闭容器中,X、Y、Z三种物质的量随时间的变化曲线如图所示.
某温度时,在2L的密闭容器中,X、Y、Z三种物质的量随时间的变化曲线如图所示.(1)由图中所给数据进行分析,该反应的化学方程式为3X+Y?2Z;
(2)X的转化率是30%
(3)当反应进行到第2min,该反应达到平衡
(4)反应从开始至2分钟末,用Z的浓度变化表示的平均反应速率为v(Z)=0.05mol/(L.min).
分析 根据图象知,随着反应进行,X、Y的物质的量减少而Z物质的量增大,说明X、Y是反应物而Z是生成物,
(1)达到平衡状态时,参加反应的△n(X)=(1.0-0.7)mol=0.3mol、△n(Y)=(1.0-0.9)mol=0.1mol、△n(Z)=(0.2-0)mol=0.2mol,同一反应中同一时间段内参加反应的各物质的物质的量之比等于其计量数之比,所以X、Y、Z的计量数之比=0.3mol:0.1mol:0.2mol=3:1:2,据此书写方程式;
(2)转化率=$\frac{消耗量}{起始量}$×100%;
(3)反应到2min后XYZ物质的量不随时间变化,反应达到平衡状态;
(4)Z的平均反应速率=$\frac{\frac{△n}{V}}{△t}$.
解答 解:根据图象知,随着反应进行,X、Y的物质的量减少而Z物质的量增大,说明X、Y是反应物而Z是生成物,
(1)达到平衡状态时,参加反应的△n(X)=(1.0-0.7)mol=0.3mol、△n(Y)=(1.0-0.9)mol=0.1mol、△n(Z)=(0.2-0)mol=0.2mol,同一反应中同一时间段内参加反应的各物质的物质的量之比等于其计量数之比,所以X、Y、Z的计量数之比=0.3mol:0.1mol:0.2mol=3:1:2,所以该反应方程式为3X+Y?2Z,
故答案为:3X+Y?2Z;
(2)X的转化率=$\frac{0.3mol}{1mol}$×100%=30%,故答案为;30%;
(3)图象可知,反应到2min后XYZ物质的量不随时间变化,反应达到平衡状态,故答案为:2;
(4)Z的平均反应速率=$\frac{\frac{△n}{V}}{△t}$=$\frac{\frac{0.2mol}{2L}}{2min}$=0.05mol/(L.min),故答案为:0.05mol/(L.min).
点评 本题考查图象分析,侧重考查学生分析及计算能力,明确曲线变化趋势含义、物质的量变化量与其计量数的关系即可解答,题目难度中等.

 新思维寒假作业系列答案
新思维寒假作业系列答案| A. | S2- | B. | AlO2- | C. | HCO3- | D. | NH4+ |
| A. | 它们互为同分异构体 | B. | 丙酸分子之间存在氢键 | ||
| C. | 它们可用核磁共振氢谱法鉴别 | D. | 它们可用KMnO4(H+)溶液鉴别 |

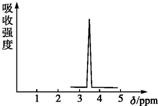 在有机物分子中,不同氢原子的核磁共振谱中给出的峰值(信号)也不同,根据峰值可以确定有机物分子中氢原子的种类和数目.
在有机物分子中,不同氢原子的核磁共振谱中给出的峰值(信号)也不同,根据峰值可以确定有机物分子中氢原子的种类和数目.