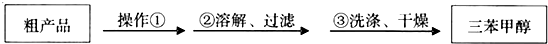题目内容
用已知浓度的盐酸溶液滴定未知浓度的烧碱溶液,下列错误操作将对c(碱)
有何影响?(填写:偏大、偏小或无影响)
A、盛标准酸的滴定管尖嘴部分有气泡未排除就开始滴定
B、振荡时液体飞溅出来
C、开始读标准酸时用仰视
D、终点读标准酸时用俯视
E、滴定前盛放氢氧化钠溶液的锥形瓶用蒸馏水洗净后没有干燥 .
有何影响?(填写:偏大、偏小或无影响)
A、盛标准酸的滴定管尖嘴部分有气泡未排除就开始滴定
B、振荡时液体飞溅出来
C、开始读标准酸时用仰视
D、终点读标准酸时用俯视
E、滴定前盛放氢氧化钠溶液的锥形瓶用蒸馏水洗净后没有干燥
考点:中和滴定
专题:实验题
分析:根据c(待测)=
分析不当操作对V(标准)的影响,以此判断浓度的误差.
| c(标注)×V(标准) |
| V(待测) |
解答:
解:A.盛标准酸的滴定管尖嘴部分有气泡未排除就开始滴定,造成V(标准)偏大,根据c(待测)=
分析,c(待测)偏大;
B.振荡时液体飞溅出来,待测液的物质的量偏小,造成V(标准)偏小,根据c(待测)=
分析,c(待测)偏小;
C.开始读标准酸时用仰视,造成V(标准)偏小,根据c(待测)=
分析,c(待测)偏小;
D.终点读标准酸时用俯视,造成V(标准)偏小,根据c(待测)=
分析,c(待测)偏小;
E.滴定前盛放氢氧化钠溶液的锥形瓶用蒸馏水洗净后没有干燥,待测液的物质的量不变,标准液的体积不变,c(待测)无影响;
故答案为:偏大;偏小;偏小;偏小;无影响.
| c(标注)×V(标准) |
| V(待测) |
B.振荡时液体飞溅出来,待测液的物质的量偏小,造成V(标准)偏小,根据c(待测)=
| c(标注)×V(标准) |
| V(待测) |
C.开始读标准酸时用仰视,造成V(标准)偏小,根据c(待测)=
| c(标注)×V(标准) |
| V(待测) |
D.终点读标准酸时用俯视,造成V(标准)偏小,根据c(待测)=
| c(标注)×V(标准) |
| V(待测) |
E.滴定前盛放氢氧化钠溶液的锥形瓶用蒸馏水洗净后没有干燥,待测液的物质的量不变,标准液的体积不变,c(待测)无影响;
故答案为:偏大;偏小;偏小;偏小;无影响.
点评:本题主要考查了中和滴定操作的误差分析,根据c(待测)=
分析是解答的关键,题目难度不大.
| c(标注)×V(标准) |
| V(待测) |

练习册系列答案
 53随堂测系列答案
53随堂测系列答案
相关题目
用铂丝做焰色反应实验,每次做完后都需要( )
| A、用水洗涤2~3次后再使用 |
| B、用盐酸洗涤,再灼烧至跟酒精灯火焰颜色相同再使用 |
| C、用盐酸洗涤,再用自来水洗净后使用 |
| D、用滤纸擦干净即可使用 |
在一定温度下的恒容容器中,当下列物理量不再发生变化时,表明反应:A(固)+3B(气)?2C(气)+D(气)已达平衡状态的是(其中只有B气体有颜色)( )
| A、混合气体的压强 |
| B、混合气体的密度 |
| C、气体的平均分子量 |
| D、气体的颜色 |
在密闭容器中发生反应:aX(g)+bY(g)?cZ(g)+dW(g)当反应达到平衡后,保持温度不变,将气体压缩到原来的
体积,当再次达到平衡时,W的浓度为原平衡的1.8倍.下列叙述中不正确的是( )
| 1 |
| 2 |
| A、平衡向逆反应方向移动 |
| B、a+b>c+d |
| C、Z的体积分数减小 |
| D、X的转化率减小 |
在标准状况下,将aLNH3完全溶于水得到VmL氨水,所得溶质的物质的量浓度为c mol/L.下列叙述中不正确的是( )
A、C=
| ||
B、已知常温下,氨水的电离常数为Ka,则pH约等于14+lg
| ||
| C、上述溶液中再加入0.5VmL同浓度稀盐酸,充分反应后c(Cl-)=c(NH4+)+c(NH3?H2O) | ||
| D、上述溶液中再加入VmL同浓度稀盐酸,充分反应后溶液中离子浓度大小关系为:c(Cl-)>c(NH4+)>c(H+)>c(OH-) |
下列关于电化学知识说法正确的是( )
| A、电解AlCl3溶液,在阴极上析出金属Al |
| B、氢氧燃料电池中,氧气是正极反应物 |
| C、用惰性电极电解CuSO4溶液一段时间,溶液酸性不变 |
| D、铅蓄电池在充电时,连接电源正极的电极反应为:PbSO4+2e-═Pb+SO42- |

 (其它试剂自选),请写出合成路线(合成路线的书写请仿照本题流程图,在箭头上标出自选试剂):
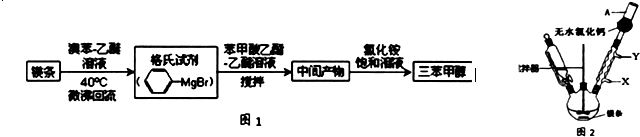
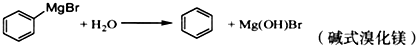
(其它试剂自选),请写出合成路线(合成路线的书写请仿照本题流程图,在箭头上标出自选试剂): )是一种重要的化工原料和医药中间体,实验室合成三苯甲醇的合成流程如图1所示.
)是一种重要的化工原料和医药中间体,实验室合成三苯甲醇的合成流程如图1所示.