题目内容
用NA代表阿伏加德罗常数,下列说法正确的是( )
| A、标准状况下,22.4LCl2和HCl的混合气体所含分子总数为2 NA |
| B、标准状况下,11.2L 乙醇所含的分子数为0.5NA |
| C、0.1molCH4所含的电子数一定为NA |
| D、22.4 L N2中所含的分子数一定为NA |
考点:阿伏加德罗常数
专题:阿伏加德罗常数和阿伏加德罗定律
分析:A、依据标准状况n=
=
计算物质的量,得到分子数;
B、标准状况乙醇不是气体;
C、甲烷为10电子微粒;
D、依据气体摩尔体积的应用条件分析判断,标准状况气体摩尔体积为2.4L/mol;
| V |
| 22.4 |
| N |
| NA |
B、标准状况乙醇不是气体;
C、甲烷为10电子微粒;
D、依据气体摩尔体积的应用条件分析判断,标准状况气体摩尔体积为2.4L/mol;
解答:
解:A、依据标准状况n=
计算物质的量=
=1mol,得到分子数 NA,故A错误;
B、标准状况乙醇不是气体,11.2L 乙醇物质的量不是0.5mol,故B错误;
C、甲烷为10电子微粒,0.1molCH4所含的电子数一定为NA,故C正确;
D、标准状况气体摩尔体积为2.4L/mol,22.4 L N2中所含的分子数不一定为NA,故D错误;
故选C.
| V |
| 22.4 |
| 22.4L |
| 22.4L/mol |
B、标准状况乙醇不是气体,11.2L 乙醇物质的量不是0.5mol,故B错误;
C、甲烷为10电子微粒,0.1molCH4所含的电子数一定为NA,故C正确;
D、标准状况气体摩尔体积为2.4L/mol,22.4 L N2中所含的分子数不一定为NA,故D错误;
故选C.
点评:本题考查了阿伏伽德罗常数的分析应用,主要是气体摩尔体积条件分析,微粒结构的理解应用,掌握基础是关键,题目较简单.

练习册系列答案
相关题目
下列物质中不能发生水解反应的是( )
| A、乙酸乙酯 | B、淀粉 |
| C、蛋白质 | D、果糖 |
“雷雨发庄稼”是一句俗语,它包涵有一定的科学道理.从化学的角度来看,下列的方程式在这个过程中不会发生的是( )
A、N2+O2
| ||||
| B、2NO+O2═2NO2 | ||||
C、N2+2O2
| ||||
| D、2NO2+H2O═2HNO3+N0 |
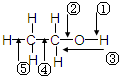 乙醇分子中各化学键如图所示,对乙醇在各种反应中应断裂的键说明正确的是( )
乙醇分子中各化学键如图所示,对乙醇在各种反应中应断裂的键说明正确的是( )| A、和金属钠作用时,键②断裂 |
| B、和浓硫酸共热至170℃时,②键和⑤断裂 |
| C、在铜催化下和氧气反应时,键①和③断裂 |
| D、与氢卤酸反应时,键①断裂 |
下列反应的离子方程式不正确的是( )
| A、Ba(OH)2溶液中加入过量Al2(SO4)3溶液:3Ba2++6OH-+2Al3++3SO42-→3 BaSO4↓+2Al(OH)3↓ |
| B、FeCl3溶液中加入过量Na2S溶液:2Fe3++S2-→2Fe2++S↓ |
| C、将适量CO2通入Ca(ClO)2溶液中(已知:次氯酸的Ki为2.95×10-8、碳酸的Ki2为5.6×10-11):2ClO-+CO2+H2O→CO32-+2HClO |
| D、向Ca(OH)2溶液中加入过量的NaHCO3溶液:Ca2++2HCO3-+2OH-→CO32-+CaCO3↓+2H2O |
在含有0.1mol氢氧化钙的溶液中,通入二氧化碳气体,当产生的沉淀为5.0g时,将该液体低温下蒸干,得到固体的质量为( )
| A、0.43g |
| B、0.87g |
| C、13.1g |
| D、16.2g |
微量元素是指人体内总含量不到万分之一,重量总和不到人体重量的千分之一的20多种元素,下列各组元素中,全部是微量元素的是( )
| A、Na、K、Cl、S |
| B、F、I、Fe、Zn、 |
| C、N、H、O、P |
| D、Ge、Se、Cu、Al、 |
下列说法正确的是( )
| A、N2的摩尔质量是14g |
| B、1mol H2O的质量是18g |
| C、氢气的摩尔质量是1g?mol |
| D、1mol H2O 中含有1molH2和1mol0 |