题目内容
分类是化学学习与研究的常用方法,下列分类正确的是( )
| A、Na2O、MgO、Al2O3均属于碱性氧化物 |
| B、石灰石、生石灰、熟石灰均属于碱 |
| C、根据是否具有丁达尔效应,将分散系分为溶液、浊液和胶体 |
| D、根据电解质在水溶液中电离的程度,将电解质分为强电解质和弱电解质 |
考点:酸、碱、盐、氧化物的概念及其相互联系,分散系、胶体与溶液的概念及关系,电解质与非电解质
专题:物质的分类专题
分析:A、依据和酸反应生成盐和水的氧化物为碱性氧化物分析;
B、水溶液中电离出的阴离子全部是氢氧根离子的化合物为碱;
C、分散系的本质区别是分散质微粒直径大小;
D、水溶液中电解质部分电离为弱电解质,全部电离为强电解质.
B、水溶液中电离出的阴离子全部是氢氧根离子的化合物为碱;
C、分散系的本质区别是分散质微粒直径大小;
D、水溶液中电解质部分电离为弱电解质,全部电离为强电解质.
解答:
解:A、依据和酸反应生成盐和水的氧化物为碱性氧化物分析,Na2O、MgO均属于碱性氧化物,Al2O3和强酸强碱反应属于两性氧化物,故A错误;
B、水溶液中电离出的阴离子全部是氢氧根离子的化合物为碱,石灰石主要成分是CaCO3属于盐、生石灰是CaO属于氧化物、熟石灰是Ca(OH)2属于碱,故B错误;
C、分散系的本质区别是分散质微粒直径大小,根据分散质微粒直径,将分散系分为:分散质小于1nm的分散系为溶液、分散质直径大于100nm的分散系为浊液,分散质微粒直径1nm-100nm的分散系为胶体,故C错误;
D、水溶液中电解质部分电离为弱电解质,全部电离为强电解质,根据电解质在水溶液中电离的程度,将电解质分为强电解质和弱电解质,故D正确;
故选D.
B、水溶液中电离出的阴离子全部是氢氧根离子的化合物为碱,石灰石主要成分是CaCO3属于盐、生石灰是CaO属于氧化物、熟石灰是Ca(OH)2属于碱,故B错误;
C、分散系的本质区别是分散质微粒直径大小,根据分散质微粒直径,将分散系分为:分散质小于1nm的分散系为溶液、分散质直径大于100nm的分散系为浊液,分散质微粒直径1nm-100nm的分散系为胶体,故C错误;
D、水溶液中电解质部分电离为弱电解质,全部电离为强电解质,根据电解质在水溶液中电离的程度,将电解质分为强电解质和弱电解质,故D正确;
故选D.
点评:本题考查了物质分类方法,物质组成分析,分散系本质区别,掌握基础是关键,题目较简单.

练习册系列答案
相关题目
下列各组固体物质中,在加水或加热的条件下,都能放出CO2的是( )
| A、NaHCO3和Al2(SO4)3 |
| B、NaHCO3和Na2CO3 |
| C、MgSO4和CaCO3 |
| D、Na2CO3和Al(NO3)3 |
下列物质既能跟硫酸反应,又能跟氢氧化钠溶液反应的是( )
①NaHCO3 ②Al2O3 ③Al(OH)3 ④Al.
①NaHCO3 ②Al2O3 ③Al(OH)3 ④Al.
| A、①②③④ | B、①和③ |
| C、③和④ | D、①和④ |
m克焦炭与x克氧气置于密闭容器中,在一定条件下充分反应后恢复到原来的温度,容器中反应物均无剩余.设反应前后压强分别为P1、P2,以下说法正确的是( )
| A、如果P1=P2,m≥3x/8 |
| B、如果2P1=P2,m≤3x/4 |
| C、如果P1<P2<2P1,3x/4>m>3x/8 |
| D、无论前后压强如何变化,m=3x/8 |
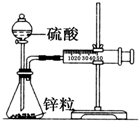 按如图安装好实验装置(装置气密性良好),在锥形瓶内盛6.5g锌粒(相对原子质量Zn-65),通过分液漏斗加入40mL2.5mol/L的硫酸溶液,将产生的H2收集在一个注射器中,用时10s时恰好收集到标准状况下的H244.8mL.下列说法不正确的是( )
按如图安装好实验装置(装置气密性良好),在锥形瓶内盛6.5g锌粒(相对原子质量Zn-65),通过分液漏斗加入40mL2.5mol/L的硫酸溶液,将产生的H2收集在一个注射器中,用时10s时恰好收集到标准状况下的H244.8mL.下列说法不正确的是( )| A、忽略锥形瓶内溶液体积的变化,用H+来表示10s内该反应的速率0.01mol/(L?s) |
| B、忽略锥形瓶内溶液体积的变化,用Zn2+来表示10s内该反应的速率0.01mol/(L?s) |
| C、用锌粒来表示10s内该反应的速率为0.013g/s |
| D、用H2来表示10s内该反应的速率为0.0002mol/s |
下列说法不正确的是( )
| A、温度相同、体积相同的O2(g)和N2(g)分子数相同 |
| B、等温等压下,SO2气体与CO2气体的密度之比等于16:11 |
| C、温度和容积相同的两气罐中分别盛有5molO2(g)和2mol N2(g),两容积中的压强之比等于5:2 |
| D、等温等压条件下,5molO2(g)和2molH2(g)的体积之比等于5:2 |
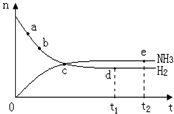 合成氨工业对国民经济和社会发展具有重要的意义,对密闭容器中的反应:
合成氨工业对国民经济和社会发展具有重要的意义,对密闭容器中的反应:N2(g)+3H2(g)
| 催化剂 |
| 高温高压 |
| A、点a的正反应速率比b点的大 |
| B、反应达到平衡时,v(N2)正=2v(NH3)逆 |
| C、点d(t1时刻)和点e(t2时刻)处n(N2)不一样 |
| D、其他条件不变,500℃下反应至t1时刻,n(H2)比图中d点值大 |
固体碘在受热时发生升华现象,有关叙述正确的是( )
| A、碘受热升华,破坏的是分子间作用力,未破坏I-I共价键,因此未发生吸热反应 |
| B、碘受热升华,吸收热量,发生了吸热反应 |
| C、碘升华,未破坏共价键,不供应热量也能发生 |
| D、碘升华过程中,热能转变为化学能 |