题目内容
信息时代产生的大量电子垃圾对环境造成了极大的威胁.某“变废为宝”学生探究小组将一批废弃的线路板简单处理后,得到含70%Cu、25%Al、4%Fe及少量Au、Pt等金属的混合物,并设计出如下制备硫酸铜晶体的路线:
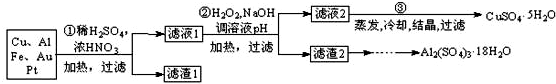
回答下列问题:
(1)第①步Cu与酸反应的离子方程式为 ;得到滤渣1的主要成分为 .
(2)第②步加入H2O2的作用是 ,使用H2O2的优点是 ;调节pH的目的是使 生成沉淀.
(3)用第③步所得CuSO4?5H2O制备无水CuSO4的方法是 .
(4)由滤渣2制取Al2(SO4)3?18H2O,探究小组设计了三种方案:
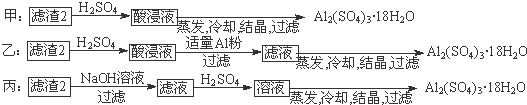
上述三种方案中, 方案不可行;三种方案中均采用了蒸发,进行该操作时注意 时停止加热.
(5)探究小组用滴定法测定CuSO4?5H2O(Mr=250)含量.取a g 试样配成100mL溶液,每次取20.00mL,消除干扰离子后,用c mol/L EDTA(H2Y2-)标准溶液滴定至终点,平均消耗EDTA溶液b mL.滴定反应如下:Cu2++H2Y2-═CuY2-+2H+.(EDTA:乙二胺四乙酸白色结晶粉末状固体,呈酸性.)
配制EDTA(H2Y2-)标准溶液时,下列仪器不必要用到的有 (用编号表示).
①电子天平 ②烧杯 ③量筒 ④玻璃棒 ⑤容量瓶 ⑥胶头滴管 ⑦移液管
写出计算CuSO4?5H2O质量分数的表达式ω= ;下列操作会导致CuSO4?5H2O含量测定结果偏高的是 .
a.未干燥锥形瓶
b.滴定终点时滴定管尖嘴中产生气泡
c.未除静可与EDTA反应的干扰离子.

回答下列问题:
(1)第①步Cu与酸反应的离子方程式为
(2)第②步加入H2O2的作用是
(3)用第③步所得CuSO4?5H2O制备无水CuSO4的方法是
(4)由滤渣2制取Al2(SO4)3?18H2O,探究小组设计了三种方案:

上述三种方案中,
(5)探究小组用滴定法测定CuSO4?5H2O(Mr=250)含量.取a g 试样配成100mL溶液,每次取20.00mL,消除干扰离子后,用c mol/L EDTA(H2Y2-)标准溶液滴定至终点,平均消耗EDTA溶液b mL.滴定反应如下:Cu2++H2Y2-═CuY2-+2H+.(EDTA:乙二胺四乙酸白色结晶粉末状固体,呈酸性.)
配制EDTA(H2Y2-)标准溶液时,下列仪器不必要用到的有
①电子天平 ②烧杯 ③量筒 ④玻璃棒 ⑤容量瓶 ⑥胶头滴管 ⑦移液管
写出计算CuSO4?5H2O质量分数的表达式ω=
a.未干燥锥形瓶
b.滴定终点时滴定管尖嘴中产生气泡
c.未除静可与EDTA反应的干扰离子.
考点:制备实验方案的设计
专题:实验设计题
分析:(1)稀硫酸、浓硝酸混合酸后加热,Cu、Al、Fe发生反应生成Cu2+、Al3+、Fe2+;所以滤渣1的成分是Pt和Au,滤液1中的离子是Cu2+、Al3+、Fe2+;
(2)过氧化氢具有氧化性且被还原为水,无杂质无污染;可以氧化亚铁离子为铁离子易于沉淀除去,调节溶液PH目的是铁离子和铝离子全部沉淀;第②步加H2O2的作用是把Fe2+氧化为Fe3+,该氧化剂的优点是不引入杂质,产物对环境物污染.调溶液PH的目的是使Fe3+和Al3+形成沉淀.所以滤液2的成分是Cu2+,滤渣2的成分为氢氧化铁和氢氧化铝;
(3)第③步由五水硫酸铜制备硫酸铜的方法应是在坩埚中加热脱水;
(4)依据实验方案过程分析制备晶体中是否含有杂质,使用的试剂作用,原料的利用率,原子利用率因素分析判断;加热蒸发时不能直接蒸干,否则容易导致固体飞溅;
(5)根据配制一定物质的量浓度的溶液步骤判断使用仪器;依据滴定实验和反应离子方程式计算得到;滴定实验误差分析依据标准溶液消耗的多少进行分析判断.
(2)过氧化氢具有氧化性且被还原为水,无杂质无污染;可以氧化亚铁离子为铁离子易于沉淀除去,调节溶液PH目的是铁离子和铝离子全部沉淀;第②步加H2O2的作用是把Fe2+氧化为Fe3+,该氧化剂的优点是不引入杂质,产物对环境物污染.调溶液PH的目的是使Fe3+和Al3+形成沉淀.所以滤液2的成分是Cu2+,滤渣2的成分为氢氧化铁和氢氧化铝;
(3)第③步由五水硫酸铜制备硫酸铜的方法应是在坩埚中加热脱水;
(4)依据实验方案过程分析制备晶体中是否含有杂质,使用的试剂作用,原料的利用率,原子利用率因素分析判断;加热蒸发时不能直接蒸干,否则容易导致固体飞溅;
(5)根据配制一定物质的量浓度的溶液步骤判断使用仪器;依据滴定实验和反应离子方程式计算得到;滴定实验误差分析依据标准溶液消耗的多少进行分析判断.
解答:
解:(1)稀硫酸、浓硝酸混合酸后加热,Cu、Al、Fe发生反应生成Cu2+、Al3+、Fe2+;所以滤渣1的成分是Pt和Au,滤液1中的离子是Cu2+、Al3+、Fe2+;第①步Cu与酸反应的离子方程式为:3Cu+8H++2NO3-
3Cu2++2NO↑+4H2O,
故答案为:3Cu+8H++2NO3-
3Cu2++2NO↑+4H2O;Au、Pt;
(2)第②步加H2O2的作用是将Fe2+氧化为Fe3+;过氧化氢做氧化剂不引入杂质,对环境无污染;调节溶液pH使Fe3+、Al3+全部沉淀后过滤得到氢氧化铁、氢氧化铝沉淀和滤液硫酸铜,
故答案为:将Fe2+氧化为Fe3+;不引入杂质,对环境无污染;Fe3+、Al3+;
(3)第③步由五水硫酸铜制备硫酸铜的方法应是在坩埚中加热脱水;
故答案为:在坩埚中加热脱水;
(4)制备硫酸铝晶体的甲、乙、丙三种方法中,甲方案在滤渣中只加硫酸会生成硫酸铁和硫酸铝,冷却、结晶、过滤得到的硫酸铝晶体中混有大量硫酸铁杂质,方法不可行;乙和丙方法均可行;乙方案先在滤渣中加H2SO4,生成Fe2(SO4)3和Al2(SO4)3,再加Al粉和Fe2(SO4)3生成Al2(SO4)3,蒸发、冷却、结晶、过滤可得硫酸铝晶体;
丙方案先在滤渣中加NaOH和Al(OH)3反应生成NaAlO2,再在滤液中加H2SO4生成Al2(SO4)3,蒸发、冷却、结晶、过滤可得硫酸铝晶体;
蒸发过程中,当蒸发浓缩至溶液表面出晶膜时停止加热,避免造成固体飞溅现象,
故答案为:甲;蒸发浓缩至溶液表面出晶膜;
(5)配制c mol/L EDTA(H2Y2-)标准溶液过程中使用的仪器有:电子天平、容量瓶、玻璃棒、胶头滴管、烧杯,不需要的仪器为:③量筒、⑦移液管;
滴定反应为:Cu2++H2Y2-=CuY2-+2H+,铜离子物质的量和标准液物质的量相同:cmol/L×b×10-3L=bc×10-3mol;依据元素守恒可得:
20ml溶液中含有的CuSO4?5H2O物质的量为:bc×10-3mol,
则100ml溶液中含硫酸铜晶体的物质的量为:bc×10-3mol×
=5bc×10-3mol,
所以CuSO4?5H2O质量分数的表达式为:
×100%;
a.未干燥锥形瓶对实验结果无影响,故a错误;
b.滴定终点时滴定管尖嘴中产生气泡说明消耗标准液读数偏小,结果偏低,故b错误;
c.未除净可与EDTA反应的干扰离子,消耗标准液多,结果偏高,故c正确;
故答案为:③⑦;
×100%;c.
| ||
故答案为:3Cu+8H++2NO3-
| ||
(2)第②步加H2O2的作用是将Fe2+氧化为Fe3+;过氧化氢做氧化剂不引入杂质,对环境无污染;调节溶液pH使Fe3+、Al3+全部沉淀后过滤得到氢氧化铁、氢氧化铝沉淀和滤液硫酸铜,
故答案为:将Fe2+氧化为Fe3+;不引入杂质,对环境无污染;Fe3+、Al3+;
(3)第③步由五水硫酸铜制备硫酸铜的方法应是在坩埚中加热脱水;
故答案为:在坩埚中加热脱水;
(4)制备硫酸铝晶体的甲、乙、丙三种方法中,甲方案在滤渣中只加硫酸会生成硫酸铁和硫酸铝,冷却、结晶、过滤得到的硫酸铝晶体中混有大量硫酸铁杂质,方法不可行;乙和丙方法均可行;乙方案先在滤渣中加H2SO4,生成Fe2(SO4)3和Al2(SO4)3,再加Al粉和Fe2(SO4)3生成Al2(SO4)3,蒸发、冷却、结晶、过滤可得硫酸铝晶体;
丙方案先在滤渣中加NaOH和Al(OH)3反应生成NaAlO2,再在滤液中加H2SO4生成Al2(SO4)3,蒸发、冷却、结晶、过滤可得硫酸铝晶体;
蒸发过程中,当蒸发浓缩至溶液表面出晶膜时停止加热,避免造成固体飞溅现象,
故答案为:甲;蒸发浓缩至溶液表面出晶膜;
(5)配制c mol/L EDTA(H2Y2-)标准溶液过程中使用的仪器有:电子天平、容量瓶、玻璃棒、胶头滴管、烧杯,不需要的仪器为:③量筒、⑦移液管;
滴定反应为:Cu2++H2Y2-=CuY2-+2H+,铜离子物质的量和标准液物质的量相同:cmol/L×b×10-3L=bc×10-3mol;依据元素守恒可得:
20ml溶液中含有的CuSO4?5H2O物质的量为:bc×10-3mol,
则100ml溶液中含硫酸铜晶体的物质的量为:bc×10-3mol×
| 100mL |
| 20mL |
所以CuSO4?5H2O质量分数的表达式为:
| cmol/L×b×10-3L×250g/mol×5 |
| ag |
a.未干燥锥形瓶对实验结果无影响,故a错误;
b.滴定终点时滴定管尖嘴中产生气泡说明消耗标准液读数偏小,结果偏低,故b错误;
c.未除净可与EDTA反应的干扰离子,消耗标准液多,结果偏高,故c正确;
故答案为:③⑦;
| cmol/L×b×10-3L×250g/mol×5 |
| ag |
点评:本题通过制备硫酸铜晶体,考查了制备实验方案的设计,试题涉及硫酸铜晶体的制备方法、中和滴定的简单计算和误差的分析,题目难度中等,明确制备原理为解答本题关键,试题充分考查了学生的分析、理解能力及化学实验、化学计算能力.

练习册系列答案
相关题目
下列与化学反应能量变化相关的叙述正确的是( )
| A、生成物的总能量总是低于反应物的总能量 |
| B、应用盖斯定律,可计算某些难以直接测量的反应热 |
| C、化学反应中的能量变化都表现为热量变化 |
| D、需要加热才能发生的反应一定是吸热反应 |
一包白色粉末可能含有Al(NO3)3、KOH、NaCl的一种或多种,某研究性学习小组为了探究该白色粉末的组成,依次做了以下实验:
第一步:将该粉末加水溶解,得到澄清溶液;
第二步:取该澄清溶液少量,逐滴加入盐酸至过量,先产生白色沉淀,后沉淀溶解;
第三步:取第二步所得溶液少量,滴入AgNO3溶液,有白色沉淀出现.
则下列判断正确的是( )
第一步:将该粉末加水溶解,得到澄清溶液;
第二步:取该澄清溶液少量,逐滴加入盐酸至过量,先产生白色沉淀,后沉淀溶解;
第三步:取第二步所得溶液少量,滴入AgNO3溶液,有白色沉淀出现.
则下列判断正确的是( )
| A、该粉末中一定含有Al(NO3)3、KOH、NaCl |
| B、该粉末中一定含有Al(NO3)3、和KOH,但不能确定是否含有NaCl |
| C、该粉末中一定含有NaCl,但不能确定是否含有Al(NO3)3、和KOH |
| D、以上过程不能确定该溶液中含有哪种物质 |
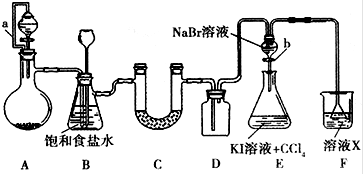
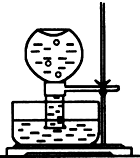 (1)如图所示,现有一瓶饱和氯水倒扣于水槽中,当日光照射到盛有氯水的装置时,可观察到平底烧瓶内有气泡产生,放置一段时间后溶液颜色变浅,产生上述现象的原因是(请用相关的反应方程式和简要文字说明)
(1)如图所示,现有一瓶饱和氯水倒扣于水槽中,当日光照射到盛有氯水的装置时,可观察到平底烧瓶内有气泡产生,放置一段时间后溶液颜色变浅,产生上述现象的原因是(请用相关的反应方程式和简要文字说明)