题目内容
在K2Cr2O7+14HCl=2KCl+2CrCl3+3Cl2↑+7H2O反应中,还原产物是 ,用双线桥法标出电子转移的方向和数目.
考点:氧化还原反应
专题:氧化还原反应专题
分析:反应中Cr元素化合价降低,被还原,K2Cr2O7作氧化剂被还原,生成CrCl3,氧化还原反应中氧化剂和还原剂之间得失电子的数目相等,表现为化合价升降总数相等.
解答:
解:反应中Cr元素化合价降低,被还原,K2Cr2O7作氧化剂被还原,生成CrCl3,则还原产物是CrCl3,氧化还原反应中氧化剂和还原剂之间得失电子的数目相等,表现为化合价升降总数相等,用双线桥法标出电子转移的方向和数目可表示为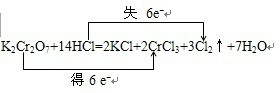 ,
,
故答案为:CrCl3; .
.
 ,
,故答案为:CrCl3;
 .
.
点评:本题考查氧化还原反应知识,侧重于学生的分析能力的考查,题目难度不大,注意从元素化合价的角度判断氧化还原反应的相关概念,注意能熟练用双线桥法标出电子转移的方向和数目.

练习册系列答案
相关题目
下列叙述正确的是( )
| A、一定温度、压强下,物质的体积由其分子的大小决定 |
| B、温度、压强一定时,气体体积由其分子数的多少决定 |
| C、气体摩尔体积是指1 mol任何气体所占的体积为22.4 L |
| D、不同的气体,若体积不等,则它们所含的分子数一定不相等 |
关于反映4Al+3TiO2+3C═2Al2O3+3TiC的叙述正确的是( )
| A、Al是还原剂,TiC是氧化产物 |
| B、TiO2是氧化剂,TiC是还原产物 |
| C、反应中氧化剂与还原剂的物质的量之比是1:1 |
| D、生成1molTiC时转移4mol电子 |
能正确表示下列反应的离子方程式的是( )
A、用铜做电极电CuSO4解溶液:2Cu2++2H2O
| ||||
| B、在NH4Fe(SO4)2溶液中,滴加少量Ba(OH)2溶液:2NH4++SO42-+Ba2++2OH-═2NH3?H2O+BaSO4↓ | ||||
| C、在Na2CO3溶液中逐滴滴入稀盐酸溶液,反应开始阶段:CO32-+H+═HCO3- | ||||
| D、在Na2S2O3溶液中加入稀硫酸:2S2O32-+4H+═SO42-+3S↓+2H2O |
下列条件变化能改变反应活化能的是( )
| A、催化剂 |
| B、增大压强 |
| C、减少浓度 |
| D、增大反应物的接触面积 |