题目内容
6.在标准状况下 ①6.72L CH4 ②3.01×1023个HCl分子 ③13.6g H2S ④0.2mol NH3下列对这四种气体的质量关系从大到小表达正确的是( )| A. | ③>②>①>④ | B. | ②>③>④>① | C. | ②>③>①>④ | D. | ①>③>④>② |
分析 根据m=nM计算各物质的质量,据此进行判断.
解答 解:6.72L CH4 物质的量为$\frac{6.72L}{22.4L/mol}$=0.3mol,②3.01×1023个HCl分子的物质的量为0.5mol,③13.6g H2S 的物质的量为$\frac{13.6g}{34g/mol}$=0.4mol,④0.2mol NH3.各物质的质量分别为①CH4 为0.3mol×16g/mol=4.8g,②HCl为0.5mol×36.5g/mol=18.25g,③H2S 13.6g,④NH3为0.2mol×17g/mol=3.4g,所以质量②>③>①>④,
故选C.
点评 本题考查物质的量的有关计算,内容涉及常用化学计量有关计算、阿伏伽德罗定律及推论,难度不大,旨在考查学生对基础知识的掌握.

练习册系列答案
 口算小状元口算速算天天练系列答案
口算小状元口算速算天天练系列答案 天天练口算系列答案
天天练口算系列答案
相关题目
14.下列电子式正确的是( )
| A. |  | B. | 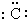 | C. | 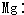 | D. | 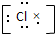 |
11.下列物质能产生丁达尔效应的是( )
| A. | Al(OH)3胶体 | B. | 蒸馏水 | C. | 饱和食盐水 | D. | 纯净的空气 |
18.为纪念俄国化学家门捷列夫,人们把第101号元素(人工合成元素)命名为钔.该元素最稳定的一种原子为 258 Md,关于该原子下列说法正确的是( )
| A. | 质子数是258 | B. | 质量数是101 | C. | 中子数是157 | D. | 电子数是359 |
15.分类法是学习和研究化学的一种常用的科学方法.下列分类合理的是( )
①Fe2O3、CaO、Al2O3都是碱性氧化物
②根据反应中是否有氧气参加,将化学反应分为氧化还原反应和非氧化还原反应
③根据元素原子最外层电子数的多少将元素分为金属元素和非金属元素
④根据纯净物中是否含氧元素,来判断是否属于氧化物
⑤根据分散系的稳定性将分散系分为胶体、溶液和浊液.
①Fe2O3、CaO、Al2O3都是碱性氧化物
②根据反应中是否有氧气参加,将化学反应分为氧化还原反应和非氧化还原反应
③根据元素原子最外层电子数的多少将元素分为金属元素和非金属元素
④根据纯净物中是否含氧元素,来判断是否属于氧化物
⑤根据分散系的稳定性将分散系分为胶体、溶液和浊液.
| A. | 只有①②④ | B. | 只有③⑤ | C. | 只有④ | D. | 都不对 |
1.某元素X的最高正化合价为+7价,下面的叙述不正确的是( )
| A. | 该元素的原子最外层上有7个电子 | |
| B. | 该元素最高价氧化物的化学式为XO3 | |
| C. | 该元素位于ⅦA族 | |
| D. | 该元素最高价氧化物对应水化物的化学式为HXO4 |