题目内容
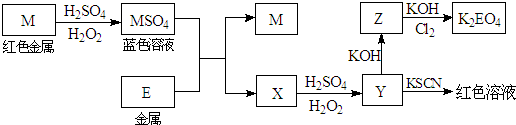
根据下列框图回答问题(答题时,方程式中的M、E用所对应的元素符号表示):

(1)写出M溶于稀H2SO4和H2O2混合液的化学方程式: 。
(2)某同学取X的溶液,在空气中放置一段时间后用酸酸化,再加入KI淀粉溶液,发现溶液变为蓝色。写出与上述变化过程相关的离子方程式:
、 。
(3)写出Cl2将Z氧化为K2EO4的化学方程式: 。
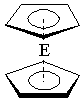 (4)由E制备的E(C5H5)2的结构如右图,其中氢原子的化学环境
(4)由E制备的E(C5H5)2的结构如右图,其中氢原子的化学环境
![]()
完全相同。但早期人们却错误地认为它的结构为: 。
核磁共振法能够区分这两种结构。在核磁共振氢谱中,正确的结构
有 种峰,错误的结构有 种峰。
(5)在1L 1mol/L的稀硝酸中加入0.3 mol金属E (还原产物只有NO),充分反应后,请简述检验溶液中的金属阳离子的实验操作及现象
(1)Cu + H2O2 + H2SO4 == CuSO4 + 2H2O (2分)
(2) 4Fe2+ + O2 + 4H+ == 4Fe3+ + 2H2O (2分)
2Fe3+ + 2I― == 2Fe2+ + I2 (2分)
(3) 10KOH + 3Cl2 + 2Fe(OH)3 == 2K2FeO4 + 6KCl + 8H2O (2分)
(4) 1 、 3 (各1分)
(5)a 取少量溶液 加KSCN溶液 出现红色 证明存在Fe3+ (2分)
b 取少量溶液 逐滴加入高锰酸钾溶液,高锰酸钾紫色褪去 证明存在Fe2+ (2分)


 (2008?江苏)根据下列框图回答问题(答题时,方程式中的M、E用所对应的元素符号表示):
(2008?江苏)根据下列框图回答问题(答题时,方程式中的M、E用所对应的元素符号表示):
 .核磁共振法能够区分这两种结构.在核磁共振氢谱中,正确的结构有
.核磁共振法能够区分这两种结构.在核磁共振氢谱中,正确的结构有