题目内容
 (2008?江苏)根据下列框图回答问题(答题时,方程式中的M、E用所对应的元素符号表示):
(2008?江苏)根据下列框图回答问题(答题时,方程式中的M、E用所对应的元素符号表示):
(1)写出M溶于稀H2SO4和H2O2混合液的化学方程式:
Cu+H2O2+H2SO4═CuSO4+2H2O
Cu+H2O2+H2SO4═CuSO4+2H2O
.(2)某同学取X的溶液,酸化后加入KI、淀粉溶液,变为蓝色.写出与上述变化过程相关的离子方程式:
4Fe2++O2+4H+═4Fe3++2H2O
4Fe2++O2+4H+═4Fe3++2H2O
、2Fe3++2I-═2Fe2++I2
2Fe3++2I-═2Fe2++I2
.(3)写出Cl2将Z氧化为K2EO4的化学方程式:
10KOH+3Cl2+2Fe(OH)3═2K2FeO4+6KCl+8H2O
10KOH+3Cl2+2Fe(OH)3═2K2FeO4+6KCl+8H2O
.(4)由E制备的E(C5H5)2的结构如图,其中氢原子的化学环境完全相同.但早期人们却错误地认为它的结构为:
 .核磁共振法能够区分这两种结构.在核磁共振氢谱中,正确的结构有
.核磁共振法能够区分这两种结构.在核磁共振氢谱中,正确的结构有1
1
种峰(即有几种化学环境完全相同H原子),错误的结构有3
3
种峰.分析:题中MSO4为蓝色溶液,则应为CuSO4,所以M为Cu,Y加KSCN呈红色,说明Y中含有Fe3+,则E为Fe,X为FeSO4,Z为Fe(OH)3,与氯气在碱性条件下反应生成K2FeO4,结合物质的性质和题目要求解答该题.
解答:解:MSO4为蓝色溶液,应为CuSO4,所以M为Cu,Y加KSCN呈红色,说明Y中含有Fe3+,则E为Fe,X为FeSO4,
Z为Fe(OH)3,与氯气在碱性条件下反应生成K2FeO4,则
(1)Cu和稀硫酸不反应,但在H2O2存在条件下,发生氧化还原反应生成硫酸铜和水,反应的化学方程式为Cu+H2O2+H2SO4═CuSO4+2H2O,
故答案为:Cu+H2O2+H2SO4═CuSO4+2H2O;
(2)Fe2+具有还原性,在酸性条件下能与空气中的氧气反应生成Fe3+,反应的离子方程式为4Fe2++O2+4H+═4Fe3++2H2O,具有强氧化性的Fe3+与具有还原性的I-反应生成I2,反应的离子方程式为2Fe3++2I-═2Fe2++I2,
故答案为:4Fe2++O2+4H+═4Fe3++2H2O;2Fe3++2I-═2Fe2++I2;
(3)根据反应物结合质量守恒可判断出生成物还应有KCl和水,
则反应的化学方程式为10KOH+3Cl2+2Fe(OH)3═2K2FeO4+6KCl+8H2O,
故答案为:10KOH+3Cl2+2Fe(OH)3═2K2FeO4+6KCl+8H2O;
(4)正确的结构H原子化学环境完全相同,只有1种峰,错误的结构中有3种不同环境的H,应有3种峰,
故答案为:1;3.
Z为Fe(OH)3,与氯气在碱性条件下反应生成K2FeO4,则
(1)Cu和稀硫酸不反应,但在H2O2存在条件下,发生氧化还原反应生成硫酸铜和水,反应的化学方程式为Cu+H2O2+H2SO4═CuSO4+2H2O,
故答案为:Cu+H2O2+H2SO4═CuSO4+2H2O;
(2)Fe2+具有还原性,在酸性条件下能与空气中的氧气反应生成Fe3+,反应的离子方程式为4Fe2++O2+4H+═4Fe3++2H2O,具有强氧化性的Fe3+与具有还原性的I-反应生成I2,反应的离子方程式为2Fe3++2I-═2Fe2++I2,
故答案为:4Fe2++O2+4H+═4Fe3++2H2O;2Fe3++2I-═2Fe2++I2;
(3)根据反应物结合质量守恒可判断出生成物还应有KCl和水,
则反应的化学方程式为10KOH+3Cl2+2Fe(OH)3═2K2FeO4+6KCl+8H2O,
故答案为:10KOH+3Cl2+2Fe(OH)3═2K2FeO4+6KCl+8H2O;
(4)正确的结构H原子化学环境完全相同,只有1种峰,错误的结构中有3种不同环境的H,应有3种峰,
故答案为:1;3.
点评:本题考查无机物的推断,题目难度中等,注意根据物质的特殊性质和反应现象作为推断的突破口,注意相关化学方程式的书写.

练习册系列答案
 小学数学口算题卡脱口而出系列答案
小学数学口算题卡脱口而出系列答案 优秀生应用题卡口算天天练系列答案
优秀生应用题卡口算天天练系列答案 浙江之星课时优化作业系列答案
浙江之星课时优化作业系列答案
相关题目
 (2008?江苏)香兰素是重要的香料之一,它可由丁香酚经多步反应合成.有关上述两种化合物的说法正确的是( )
(2008?江苏)香兰素是重要的香料之一,它可由丁香酚经多步反应合成.有关上述两种化合物的说法正确的是( )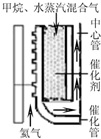 (2010?江苏二模)以天然气为原料经由合成气(CO、H2)制化学品是目前天然气转化利用的主导技术路线,主要工艺有以下几种:
(2010?江苏二模)以天然气为原料经由合成气(CO、H2)制化学品是目前天然气转化利用的主导技术路线,主要工艺有以下几种: