题目内容
14.下列物质属于共价化合物的是( )| A. | C60 | B. | CaCl2 | C. | KF | D. | H2O2 |
分析 一般来说,活泼金属和活泼非金属元素之间易形成离子键,非金属元素之间易形成共价键,只含共价键的化合物属于共价化合物,共价化合物中一定不含离子键,含有离子键的化合物属于离子化合物,离子化合物中可能含有共价键,据此分析解答.
解答 解:A.C60为单质,不属于共价化合物,故A错误;
B.CaCl2中只存在离子键,属于离子化合物,故B错误;
C.KF中只存在离子键,属于离子化合物,故C错误;
D.H2O2分子中只存在共价键,属于共价化合物,故D正确;
故选D.
点评 本题考查单质、化合物、离子化合物、共价化合物等基本概念,侧重考查学生对概念的理解,注意这几个概念的区别,题目难度不大.

练习册系列答案
 应用题天天练四川大学出版社系列答案
应用题天天练四川大学出版社系列答案
相关题目
4.下列各组物质属于同系物的是( )
| A. | 2,2-二甲基丙烷和新戊烷 | |
| B. | 2,2-二甲基-1-丙醇和2-甲基-1-丁醇 | |
| C. | 对氯甲苯和邻氯乙苯 | |
| D. | 甲基丙烯酸和甲酸丁酯 |
5.下表是元素周期表的一部分,针对表中元素,填写下列空白.
(1)写出Na+结构示意图 ,氯元素的原子结构示意图
,氯元素的原子结构示意图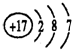 ;
;
(2)F、Cl、S的氢化物中稳定性最强的是HF(填氢化物名称);
(3)表中氧化性最强的单质的化学式为F2;
(4)这些元素的最高价氧化物的水化物中,碱性最强的是NaOH(填化学式);
(5)氧和钠两种元素中,离子半径较小的是Na+(填离子符号);
(6)氧,硫,磷三种元素的气态氢化物的稳定性强弱顺序为H2O>H2S>PH3(填化学式);
(7)碳与氧形成的化合物中,固态时俗称干冰的电子式 ,该化合物属于共价(填“共价”或“离子”)化合物.
,该化合物属于共价(填“共价”或“离子”)化合物.
族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA |
| 2 | Li | Be | B | C | N | O | F |
| 3 | Na | Mg | Al | Si | P | S | Cl |
 ,氯元素的原子结构示意图
,氯元素的原子结构示意图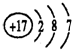 ;
;(2)F、Cl、S的氢化物中稳定性最强的是HF(填氢化物名称);
(3)表中氧化性最强的单质的化学式为F2;
(4)这些元素的最高价氧化物的水化物中,碱性最强的是NaOH(填化学式);
(5)氧和钠两种元素中,离子半径较小的是Na+(填离子符号);
(6)氧,硫,磷三种元素的气态氢化物的稳定性强弱顺序为H2O>H2S>PH3(填化学式);
(7)碳与氧形成的化合物中,固态时俗称干冰的电子式
 ,该化合物属于共价(填“共价”或“离子”)化合物.
,该化合物属于共价(填“共价”或“离子”)化合物.
2.最近媒体报道了一些化学物质,如爆炸力极强的N5,结构类似白磷的P4,比黄金还贵的18O2,太空中的甲醇气团等.下列说法正确的是( )
| A. | 2N5═5N2是化学变化 | B. | 18O2和16O2是同位素 | ||
| C. | 18O的原子内有9个中子 | D. | P4只有共价键 |
19.下列说法不正确的是( )
| A. | 微粒半径:Cl>S>N>O | B. | 稳定性:HF>HCl>HBr>HI | ||
| C. | 酸性:HClO4>H2SO4>H3PO4>H2SiO3 | D. | 碱性:KOH>Ca(OH)2>Mg(OH)2>Al(OH)3 |
6.关于pH相同的醋酸和盐酸溶液,下列叙述不正确的是( )
| A. | 取等体积的两种酸分别与完全一样的足量锌粒反应,开始时反应速率盐酸大于醋酸 | |
| B. | 取等体积的两种酸溶液分别稀释至原溶液的m倍和n倍,稀释后两溶液的pH仍然相同,则m<n | |
| C. | 取等体积的两种酸溶液分别与足量的锌粒反应,生成氢气的体积醋酸大于盐酸 | |
| D. | 取等体积的两种酸溶液分别与NaOH溶液中和,消耗NaOH的物质的量醋酸大于盐酸 |
3.四氯化碳是生产金属钛及其化合物的重要中间体,实验窒利用反应:TiO2(s)+2CCl4(g)$\frac{\underline{\;\;△\;\;}}{\;}$TiCl4(g)+CO2(g),制取TiCl4,实验装置如图所示: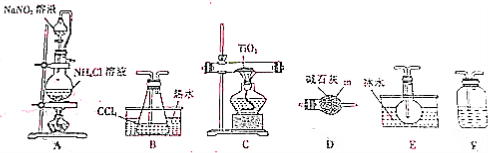
有关物质的性质如下表:
回答下列问题:
(1)仪器m的名称为球形干燥管.
(2)装置A中有氮气生成,该反应的化学方程式为NaNO2+NH4Cl$\frac{\underline{\;\;△\;\;}}{\;}$N2↑+NaCl+2H2O
(3)实验装置依次连接的顺序为A→F→B→C→E→D.装置F中盛有的物质是浓硫酸(4)装置D的作用是防止外界的水汽进入TiCl4收集装置里.
(5)欲分离装置E中态混合采用操作的名称是蒸馏.
(6)反应结束前进行如下操作:①停止通氮气②熄灭酒精灯③冷却至室温,正确的操作顺序②③①
(7)利用反应:TiO2(s)+2C(s)+2Cl2(g)$\frac{\underline{\;\;△\;\;}}{\;}$TiCl4(g)+CO2(g),也可以制取TiCl4,除了在上述实验装置中将装置A改为氯气的发生装置,撤去装置B之外,请件数对其他装置的改变:石英管内改为盛TiO2和C.

有关物质的性质如下表:
| 物质 | 熔点/℃ | 沸点/℃ | 其它 |
| CCl4 | -23 | 76 | 与 TiCl4互溶 |
| TiCl4 | -25 | 136 | 遇潮湿空气产生白雾,加热时能被氧气氧化 |
(1)仪器m的名称为球形干燥管.
(2)装置A中有氮气生成,该反应的化学方程式为NaNO2+NH4Cl$\frac{\underline{\;\;△\;\;}}{\;}$N2↑+NaCl+2H2O
(3)实验装置依次连接的顺序为A→F→B→C→E→D.装置F中盛有的物质是浓硫酸(4)装置D的作用是防止外界的水汽进入TiCl4收集装置里.
(5)欲分离装置E中态混合采用操作的名称是蒸馏.
(6)反应结束前进行如下操作:①停止通氮气②熄灭酒精灯③冷却至室温,正确的操作顺序②③①
(7)利用反应:TiO2(s)+2C(s)+2Cl2(g)$\frac{\underline{\;\;△\;\;}}{\;}$TiCl4(g)+CO2(g),也可以制取TiCl4,除了在上述实验装置中将装置A改为氯气的发生装置,撤去装置B之外,请件数对其他装置的改变:石英管内改为盛TiO2和C.
4.霉酚酸是一种生物活性化合物,其结构如下图所示.下列有关霉酚酸的说法正确的是( )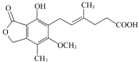

| A. | 该物质的分子式为C17H18O6 | |
| B. | 该物质中含有四种官能团 | |
| C. | 1 mol该物质可与4 mol Br2发生加成反应 | |
| D. | 1 mol该物质与足量金属钠反应产生1 mol氢气 |