题目内容
2.最近媒体报道了一些化学物质,如爆炸力极强的N5,结构类似白磷的P4,比黄金还贵的18O2,太空中的甲醇气团等.下列说法正确的是( )| A. | 2N5═5N2是化学变化 | B. | 18O2和16O2是同位素 | ||
| C. | 18O的原子内有9个中子 | D. | P4只有共价键 |
分析 A、根据同素异形体间的转化是化学反应;
B、根据质子数相同,而中子数不同的原子互为同位素;
C、根据质量数=质子数+中子数;
D、根据白磷分子是正四面体结构.
解答 解:A、2N5=5N2是同素异形体间的转化,是化学变化,故A正确;
B、18O2和16O2是两种分子,不是原子,不是同位素,故B错误;
C、18O的原子内有10个中子,故C错误;
D、白磷分子是正四面体结构,N4分子为正四面体结构,每个分子中含有6个共价键,故D正确;
故选AD.
点评 本题考查了核素、同素异形体、化学键的应用,关键同素异形体的转化是化学变化.

练习册系列答案
相关题目
12.根据表中7种短周期元素的有关信息判断,下列说法错误的是( )
| 元素编号 | ① | ② | ② | ④ | ⑤ | ⑥ | ⑦ |
| 原子半径/nm | 0.037 | 0.074 | 0.082 | 0.099 | 0.102 | 0.143 | 0.152 |
| 最高化合价或最低化合价 | +1 | -2 | +3 | -1 | -2 | +3 | +1 |
| A. | ⑦①可形成离子化合物 | |
| B. | 元素②⑥形成的化合物具有两性 | |
| C. | 元素②氢化物的沸点小于元素⑤氢化物的沸点 | |
| D. | 元素④气态氢化物的稳定性大于元素⑤气态氢化物的稳定性 |
13.下列方程式书写正确的是( )
| A. | 乙醇与金属钠反应产生氢气:CH3CH2OH+Na→CH3CH2ONa+H2↑ | |
| B. | 苯与浓硫酸、浓硝酸的混合溶液共热制硝基苯: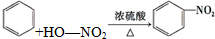 | |
| C. | 乙酸与乙醇发生反应生成乙酸乙酯:CH3CH2OH+CH3COOH$→_{△}^{催化剂}$CH3COOCH2CH3 | |
| D. | 乙烯使溴的四氯化碳溶液褪色:CH2=CH2+Br2→CH2BrCH2Br |
10.下列叙述中,可以说明金属甲的活动性比金属乙的活动性强的是( )
| A. | 将甲、乙作电极组成原电池时,甲是负极 | |
| B. | 同价态的阳离子,甲比乙的氧化性强 | |
| C. | 甲与稀盐酸反应放出氢气的体积比乙与稀盐酸反应放出氢气的体积大 | |
| D. | 在氧化还原反应中,甲原子失去的电子比乙原子失去的电子多 |
17.硫酸工业是利用反应2SO2+O2?2SO3制备SO3,该反应为放热反应.温度和压强对SO2平衡转化率影响的数据如下表.
从成本角度考虑,应选用的适宜压强和温度条件是( )
| 压强/MPa | ||||
| SO2平衡 | ||||
| 转化率/% | ||||
| 温度/℃ | 0.1 | 0.5 | 1 | 10 |
| 400 | 99.2 | 99.6 | 99.7 | 99.9 |
| 500 | 93.5 | 96.9 | 97.8 | 99.3 |
| 600 | 73.7 | 85.8 | 89.5 | 96.4 |
| A. | 0.1 MPa,400℃ | B. | 0.5 MPa,500℃ | C. | 1 MPa,600℃ | D. | 10 MPa,600℃ |
14.下列物质属于共价化合物的是( )
| A. | C60 | B. | CaCl2 | C. | KF | D. | H2O2 |
11.沼气是有机废弃物在隔绝空气的条件下发酵分解而成的气体,主要成分为甲烷.农村沼气池中发酵后的池底剩余物是很好的沤肥.下面有关结论中,错误的是( )
| A. | 沼气是一种清洁的能源 | |
| B. | 使用沼气做能源是解决农村能源的主要途径 | |
| C. | 使用沼气给农民的生活带来了不便 | |
| D. | 使用沼气是对化学能的充分利用 |
12.“魔酸”酸性是浓硫酸的1亿倍,可以将正丁烷转化为异丁烷,下列关于这一转化的说法中错误的是( )
| A. | 是化学变化 | B. | 没有能量变化 | ||
| C. | 有C-C、C-H键的断裂 | D. | 有C-C、C-H键的形成 |