题目内容
9.某含氧有机物的相对分子质量为60,1mol该有机物完全燃烧,生成36gH2O和44.8L CO2(标准状况下).(1)求该有机物分子式;
(2)又知此有机物具有弱酸性,能与金属钠反应,也能与碱溶液反应,试写出它可能的结构简式.
分析 (1)根据根据n=$\frac{m}{M}$和n=$\frac{V}{{V}_{m}}$计算H2O、CO2的物质的量,根据原子守恒计算有机物分子中C、H原子数目,再结合有机物的相对分子质量计算有机物分子中氧原子数目,进而确定有机物的分子式;
(2)有机物具有弱酸性,能与金属钠反应,也能与碱溶液反应,则有机物含有-COOH、-OH(酚羟基)中的至少一种,结合有机物的分子式书写其可能结构.
解答 解:(1)36g H2O的物质的量为:$\frac{36g}{18g/mol}$=2mol,则含有氢原子的物质的量为:n(H)=2mol×2=4mol,
标准状况下44.8LCO2 的物质的量为:$\frac{44.8L}{22.4L/mol}$=2mol,含有碳原子的物质的量为:n(C)=2mol,
故有机物分子中含有C、H原子数为:N(H)=$\frac{4mol}{1mol}$=4、N(C)=$\frac{2mol}{1mol}$=2,
该有机物分子中含有氧原子的数目为:N(O)=$\frac{60-4-12×2}{16}$=2,
所以该有机物的分子式为:C2H4O2,
答:该有机物的分子式为C2H4O2;
(2)有机物分子式为C2H4O2,有机物具有弱酸性,能与金属钠反应,也能与碱溶液反应,则有机物含有-COOH,其结构简式为:CH3COOH,
答:该有机物的结构简式为CH3COOH.
点评 本题考查有机物分子式、结构简式确定的计算,题目难度不大,注意掌握燃烧法利用元素原子守恒确定有机物的分子式,明确常见有机物组成、结构与性质,试题培养了学生的分析能力及化学计算能力.

练习册系列答案
 每日10分钟口算心算速算天天练系列答案
每日10分钟口算心算速算天天练系列答案
相关题目
19.有六种微粒分别是1940X、2040Y、1840Z、1940Q+、2040K2+、2040M,它们所属元素的种类为( )
| A. | 2种 | B. | 3种 | C. | 4种 | D. | 5种 |
20.A、B、C、D为短周期元素,请根据下表信息回答问题.
(1)B在元素周期表的位置:第二周期VA族;B气态氢化物的电子式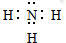
(2)C的最高价氧化物分别与强酸、强碱反应的离子方程式为Al2O3+6H+=2Al3++3H2O、Al2O3+2OH-=2AlO2-+H2O;
(3)D的单质与A的一种氢化物反应生成具有漂白性的物质的化学方程式为Cl2+H2O=HCl+HClO.
| 元素 | A | B | C | D |
| 性质或结构信息 | 工业上通过分离液态空气获得其单质,单质能助燃 | 气态氢化物显碱性 | +3价阳离子的核外电子排布与氖原子相同 | 第三周期原子半径最小 |
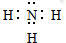
(2)C的最高价氧化物分别与强酸、强碱反应的离子方程式为Al2O3+6H+=2Al3++3H2O、Al2O3+2OH-=2AlO2-+H2O;
(3)D的单质与A的一种氢化物反应生成具有漂白性的物质的化学方程式为Cl2+H2O=HCl+HClO.
4.分子式为C10H12O2的有机物,满足以下两个条件:①苯环上只有两个取代基;②能与NaHCO3溶液反应生成气体.则满足该条件的有机物共有(不考虑立体异构)( )
| A. | 15种 | B. | 12种 | C. | 10种 | D. | 9种 |
14.2008年,我国的航天事业取得了巨大的成就,航天员翟志刚顺利实现了太空行走.下列说法不正确的是( )
| A. | 在生活舱中,可用过氧化钠制备氧气 | |
| B. | 金属镁可用作制造飞机、火箭的重要材料 | |
| C. | 在航天试验用的仪器仪表中大量使用了硅等非金属材料 | |
| D. | 返回舱外层的隔热瓦使用的是金属材料 |
1.对于反应MnO2+4HCl(浓)$\frac{\underline{\;△\;}}{\;}$MnCl2+Cl2↑+2H2O,下列说法正确的是( )
| A. | MnO2是还原剂 | B. | MnCl2是氧化产物 | C. | Cl2是氧化产物 | D. | H2O是还原产物 |
18.下列实验方案中,可达到预期目的是( )
| A. | 用萃取的方法分离Br2和CCl4混合物 | |
| B. | 加足量烧碱溶液过滤.除去混在镁粉中的少量铝粉 | |
| C. | 加人盐酸酸化的Ba(NO3)2溶液,可以鉴别Na2SO3和Na2SO4 | |
| D. | 用溶解、过滤的方法分离KNO3和NaCl的混合物 |
 表示的分子式C6H14;若它的一种同分异构体可由一种烯烃加成制得,则此同分异构体的结构体的结构简式为C(CH3)3CH2CH3;若它的一种同分异构体可由所有碳原子在同一平面的烯烃加成制得,该烯烃的结构简式是(CH3)2C=C(CH3)2.
表示的分子式C6H14;若它的一种同分异构体可由一种烯烃加成制得,则此同分异构体的结构体的结构简式为C(CH3)3CH2CH3;若它的一种同分异构体可由所有碳原子在同一平面的烯烃加成制得,该烯烃的结构简式是(CH3)2C=C(CH3)2. 中含有的官能团的名称为羟基、酯基.
中含有的官能团的名称为羟基、酯基.