题目内容
下列实验合理的是( )
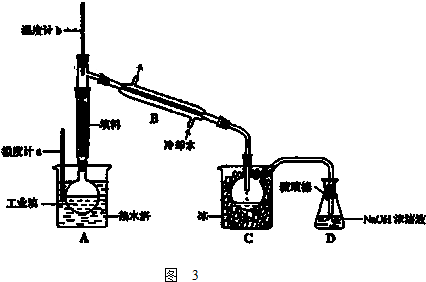
A、 分离苯和溴苯的混合物 |
B、 制备少量氨气 |
C、 配制一定浓度硫酸溶液 |
D、 收集CO2 |
考点:化学实验方案的评价
专题:实验评价题
分析:A.苯和溴苯的混合物,互溶,但沸点不同;
B.氧化钙和水反应放热,使氨水分解生成氨气;
C.不能直接将浓硫酸注入容量瓶中;
D.二氧化碳的密度比空气密度大.
B.氧化钙和水反应放热,使氨水分解生成氨气;
C.不能直接将浓硫酸注入容量瓶中;
D.二氧化碳的密度比空气密度大.
解答:
解:A.苯和溴苯的混合物,互溶,但沸点不同.则选图中蒸馏装置可分离,温度计位置、冷水方向等均合理,故A正确;
B.氧化钙和水反应放热,使氨水分解生成氨气,图中分液漏斗等仪器及原理均合理,可制备少量氨气,故B正确;
C.不能直接将浓硫酸注入容量瓶中,应在烧杯中稀释、冷却后转移到容量瓶中,操作不合理,故C错误;
D.二氧化碳的密度比空气密度大,应利用向上排空气法,图中气体应从长导管进入,故D错误;
故选AB.
B.氧化钙和水反应放热,使氨水分解生成氨气,图中分液漏斗等仪器及原理均合理,可制备少量氨气,故B正确;
C.不能直接将浓硫酸注入容量瓶中,应在烧杯中稀释、冷却后转移到容量瓶中,操作不合理,故C错误;
D.二氧化碳的密度比空气密度大,应利用向上排空气法,图中气体应从长导管进入,故D错误;
故选AB.
点评:本题考查化学实验方案的评价,为高频考点,涉及混合物分离、气体制备及溶液配制等,把握物质的性质、反应原理及实验装置的作用为解答的关键,侧重分析与实验能力的考查,注意实验的评价性分析,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
丙酮醛( )是重要的制药中间体,如果以2-溴丙烷为初始原料,通过多步反应制得.需要经过的反应依次是( )
)是重要的制药中间体,如果以2-溴丙烷为初始原料,通过多步反应制得.需要经过的反应依次是( )
 )是重要的制药中间体,如果以2-溴丙烷为初始原料,通过多步反应制得.需要经过的反应依次是( )
)是重要的制药中间体,如果以2-溴丙烷为初始原料,通过多步反应制得.需要经过的反应依次是( )| A、取代-氧化-加成-消去 |
| B、消去-取代-加成-氧化 |
| C、消去-加成-取代-氧化 |
| D、取代-消去-加成-氧化 |
松萝酸常作为牙膏和化妆品的添加剂,其结构简式如图所示,下列有关说法正确的是( )

| A、每个松萝酸分子中含有3个酚羟基 |
| B、每个松萝酸分子中含有1个手性碳原子 |
| C、松萝酸能发生加成、氧化、水解、消去等反应 |
| D、1mol松萝酸最多能与8molH2发生加成反应 |
下列说法正确的是( )
| A、硫酸、纯碱、碳酸钠和生石灰分别属于酸、碱、盐和氧化物 |
| B、光导纤维是以硅为主要原料制成的 |
| C、可依据是否有丁达尔现象区分溶液与胶体 |
| D、Fe(OH)3难溶于水,不存在氢氧化铁胶体 |
镁/H2O2酸性燃料电池采用海水作电解质(加入一定量的酸),下列说法正确的是( )
| A、电池总反应为:Mg+H2O2=Mg(OH)2 |
| B、正极发生的电极反应为:H2O2+2H++2e-=2H2O |
| C、工作时,正极周围海水的pH增大 |
| D、电池工作时,溶液中的H+向负极移动 |
下列反应的离子方程式不正确的是( )
| A、用盐酸清除水垢CaCO3+2H+=Ca2++CO2↑+H2O |
| B、Fe跟稀硫酸反应:Fe+2H+=Fe3++H2↑ |
| C、澄清石灰水跟稀盐酸:H++OH-=H2O |
| D、碳酸氢钠溶液跟氢氧化钠溶液反应 HCO3-+OH-=H2O+CO32- |
 (1)化学在环境保护中趁着十分重要的作用,催化反硝化法和电化学降解法可用于治理水中硝酸盐的污染.电化学降解NO
(1)化学在环境保护中趁着十分重要的作用,催化反硝化法和电化学降解法可用于治理水中硝酸盐的污染.电化学降解NO