题目内容
5.含NO3-的工业废水会造成水体富营养化,可利用如下反应将其转化为NH3:Al+口+口+口→口+口,反应中涉及到的另外3种微粒是H2O、AlO2-、OH-.下列说法正确的是( )| A. | 反应中的Al被还原,NO3-是还原剂 | |
| B. | 产物分别是NH3、AlO2-和OH- | |
| C. | 若有4mol Al参加反应,则有1.5mol NO3-被还原 | |
| D. | 随着反应的进行,溶液的碱性逐渐增强 |
分析 A1与NO3-发生氧化还原反应,Al转化为AlO2-化合价升高失电子,NO3-转化为NH3化合价降低得电子,则发生的反应为8Al+3NO3-+5OH-+2H2O=8AlO2-+3NH3↑,据此分析.
解答 解:A.A1与NO3-发生氧化还原反应,Al转化为AlO2-化合价升高失电子,则Al为还原剂,NO3-转化为NH3化合价降低得电子,则NO3-为氧化剂,故A错误;
B.反应为8Al+3NO3-+5OH-+2H2O=8AlO2-+3NH3↑,则OH-为反应物,故B错误;
C.若有8 mol Al参加反应,有3mol NO3-被还原,所以有4mol Al参加反应,则有1.5mol NO3-被还原,故C正确;
D.由于反应消耗OH-,所以随着反应的进行,溶液的碱性逐渐减弱,故D错误.
故选C.
点评 本题考查了氧化还原反应,题目涉及反应物和生成物的判断、方程式的书写等,注意根据化合价的变化分析,题目难度不大,侧重于考查学生对基础知识的分析应用能力.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
15.可逆反应达到化学平衡的标志是( )
| A. | 正、逆反应不再进行 | B. | 浓度为零 | ||
| C. | 正、逆反应都还在继续进行 | D. | 正、逆反应的速率相等 |
16.某溶液中存在Mg2+、Ag+、Ba2+三种金属离子,现用NaOH、Na2CO3、NaCl三种溶液使它们分别沉淀并分离出,要求每次只加一种溶液,滤出一种沉淀,所加溶液顺序正确的是( )
| A. | Na2CO3 NaCl NaOH | B. | NaOH NaCl Na2CO3 | ||
| C. | NaCl NaOH Na2CO3 | D. | NaCl Na2CO3 NaOH |
13.2010年5月2日,某煤矿发生瓦斯爆炸事故,造成多人伤亡,因此在矿井里,必须采取安全措施,如通风、严禁烟火等,而且要随时检查瓦斯的体积分数,如果空气中含甲烷5%~15.4%,遇明火会发生爆炸.发生最强烈爆炸时空气中甲烷所占的体积分数是( )
| A. | 5% | B. | 9.1% | C. | 10.5% | D. | 15.4% |
20.下列表示物质结构的化学用语正确的是( )
| A. | 8个中子的碳原子的核素符号:12C | B. | HF的电子式: | ||
| C. | 氯化镁  | D. | Cl-离子的结构示意图: |
10.下列离子方程式书写正确的是( )
| A. | Ca(HCO3)2 溶液中滴入过量NaOH溶液:HCO3-+Ca2++OH-═CaCO3↓+H2O | |
| B. | 向NaAlO2 溶液中通入过量的 CO2:CO2+2H2O+A1O2-═Al(OH)3↓+HCO3- | |
| C. | 0.01mol/L NH4Al(SO4)2 溶液与 0.02mol/L Ba(OH)2 溶液等体积混合:Al3++2SO42-+2Ba2++4OH-═2BaSO4↓+AlO2-+2H2O | |
| D. | 向Ca(ClO)2 溶液中通入过量的 SO2:C1O-+SO2+H2O═HClO+HSO3- |
17.下列说法正确的是( )
| A. | 钢件表面镀锌时,钢件与外电源的正极相连 | |
| B. | 由反应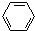 (g)+H2(g)→ (g)+H2(g)→ (g)△H=+28.7kJ.mol-1,则环已二烯比苯稳定 (g)△H=+28.7kJ.mol-1,则环已二烯比苯稳定 | |
| C. | 常温时,pH=11的氨水与pH=3的盐酸等体积混合,所得溶液pH>7 | |
| D. | 合成氨反应N2+3H2?2NH3,当满足v(N2)逆:v(H2)逆:v(NH3)逆=1:3:2时,标志该反应已达到平衡状态 |
14.下列实验中,分离和除杂所选试剂和方法均正确的是( )
| 选项 | 目的 | 试剂 | 方法 |
| A | 分离碘水中的碘 | 乙醇 | 萃取 |
| B | 分离乙酸乙酯和乙醇 | 氢氧化钠溶液 | 分液 |
| C | 除去乙醇中乙酸 | 氧化钙 | 蒸馏 |
| D | 除去乙烷中的乙烯 | 溴的四氯化碳溶液 | 洗气 |
| A. | A | B. | B | C. | C | D. | D |
15.常温下,下列各组离子在溶液一定能大量共存的是( )
| A. | I-Fe3+ Na+ | B. | Al3+Ba2+HCO3- | C. | K+Na+CO32- | D. | NH4+K+OH- |