题目内容
某强酸性溶液中仅含有Ba2+、Al3+、Fe3+、Fe2+、NH4+、CO32-、SO32-、SO42-、Cl-、NO3-中的一种或几种,取溶液进行下列连续实验,实验内容如下

根据以上信息,回答下列问题:
(1)①仅根据上述连续实验,不能确定溶液X中是否含有的离子是 ;
②气体D分子的电子式为 ;
③若要确定不能确定的溶液X中的阴离子是否存在,检验的最可靠的化学方法是(若无不能确定的阴离子,此文不必回答) ;
(2)写出下列有关离子方程式;
实验①中生成无色气体A:
实验③中生成沉淀H:
(3)假设实验②所用氢氧化钠溶液的浓度为4mol/L.加入氢氧化钠溶液的体积与产生沉淀的物质的量如图所示(不考虑离子的水解、气体的溶解等)根据有关信息填表(根据实际情况填写,可以不填满,也可以补充)


根据以上信息,回答下列问题:
(1)①仅根据上述连续实验,不能确定溶液X中是否含有的离子是
②气体D分子的电子式为
③若要确定不能确定的溶液X中的阴离子是否存在,检验的最可靠的化学方法是(若无不能确定的阴离子,此文不必回答)
(2)写出下列有关离子方程式;
实验①中生成无色气体A:
实验③中生成沉淀H:
(3)假设实验②所用氢氧化钠溶液的浓度为4mol/L.加入氢氧化钠溶液的体积与产生沉淀的物质的量如图所示(不考虑离子的水解、气体的溶解等)根据有关信息填表(根据实际情况填写,可以不填满,也可以补充)

| 原溶液中确定含有的阴离子的化学式 | 该阴离子的物质的量浓度 |
考点:常见阳离子的检验,常见阴离子的检验
专题:物质检验鉴别题
分析:在强酸性溶液中一定不会存在CO32-、SO32-离子;加入过量硝酸钡生成沉淀,则该沉淀C为BaSO4,说明溶液中含有SO42-离子,根据硫酸钡的质量可以计算硫酸根离子的物质的量,生成无色气体A,则A只能是NO,说明溶液中含有还原性离子,则一定为Fe2+离子,溶液B中加入过量NaOH溶液,沉淀F只为Fe(OH)3,生成气体D,则D为NH3,说明溶液中含有NH4+离子;溶液E中通入CO2气体,生成沉淀G,则I为Al(OH)3,H为NaOH和NaAlO2,说明溶液中含有Al3+离子,再根据离子共存知识,溶液中含有Fe2+离子,则一定不含NO3-离子和SO32-离子,那么一定含有SO42-离子,那么就一定不含Ba2+离子,不能确定是否含有的离子Fe3+和Cl-,以此进行解答.
解答:
解:在强酸性溶液中一定不会存在CO32-、SO32-离子;加入过量硝酸钡生成沉淀,则该沉淀C为BaSO4,说明溶液中含有SO42-离子,根据硫酸钡的质量可以计算硫酸根离子的物质的量,生成无色气体A,则A只能是NO,说明溶液中含有还原性离子,则一定为Fe2+离子,溶液B中加入过量NaOH溶液,沉淀F只为Fe(OH)3,生成气体D,则D为NH3,说明溶液中含有NH4+离子;溶液E中通入CO2气体,生成沉淀G,则I为Al(OH)3,H为NaOH和NaAlO2,说明溶液中含有Al3+离子,再根据离子共存知识,溶液中含有Fe2+离子,则一定不含NO3-离子和SO32-离子,那么一定含有SO42-离子,那么就一定不含Ba2+离子,不能确定是否含有的离子Fe3+和Cl-,
(1)①根据以上分析可知,溶液中不能确定的阳离子为Fe3+,溶液中不能确定的阴离子为Cl-,故答案为:Fe3+、Cl-;
②气体D为氨气,氨气分子的电子式为: ,故答案为:
,故答案为: ;
;
③若要确定不能确定的溶液X中的阴离子是否存在,检验的最可靠的化学方法是:取少许X溶液于试管中,加入AgNO3溶液,再加入足量稀HNO3,有白色沉淀,则说明有氯离子,否则没有,故答案为:取少许X溶液于试管中,加入AgNO3溶液,再加入足量稀HNO3,有白色沉淀,则说明有氯离子,否则没有;
(2)中得到的气体A是NO,Fe2+离子被氧化为Fe3+离子,NO3-离子被还原为NO气体,反应的离子方程式为:3Fe2++NO3-+4H+=3Fe3++NO↑+2H2O,E中NaAlO2,沉淀G为氢氧化铝,偏铝酸根离子与二氧化碳反应生成氢氧化铝沉淀,反应的离子方程式为:AlO2-+CO2+2H2O=Al(OH)3↓+HCO3-,
故答案为:3Fe2++4H++NO3-=3Fe3++NO↑+2H2O;AlO2-+CO2+2H2O=Al(OH)3↓+HCO3;
(3)由图象可知,沉淀溶解需要氢氧化钠的体积为2.5mL,那么物质的量为:0.0025L×4mol/L=0.01mol,即铝离子的物质的量为0.01mol;沉淀铝离子,需要氢氧化钠为0.03mol,即沉淀铁离子,需要氢氧化钠为(55-7.5-10)×-3×4mol/L=0.15mol,故铁离子为:0.05mol,无色气体A体积为224mL,即物质的量为:
=0.01mol,沉淀C为硫酸钡,物质的量为:
=0.08mol,故硫酸根离子的物质的量为:0.08mol,n(+)=0.05×3+0.01×3+0.01=0.19,n(-)=0.08×2=0.16,依旧电中性原则:故需要负电荷为:0.03mol,故答案为:Cl-;0.03mol.
(1)①根据以上分析可知,溶液中不能确定的阳离子为Fe3+,溶液中不能确定的阴离子为Cl-,故答案为:Fe3+、Cl-;
②气体D为氨气,氨气分子的电子式为:
 ,故答案为:
,故答案为: ;
;③若要确定不能确定的溶液X中的阴离子是否存在,检验的最可靠的化学方法是:取少许X溶液于试管中,加入AgNO3溶液,再加入足量稀HNO3,有白色沉淀,则说明有氯离子,否则没有,故答案为:取少许X溶液于试管中,加入AgNO3溶液,再加入足量稀HNO3,有白色沉淀,则说明有氯离子,否则没有;
(2)中得到的气体A是NO,Fe2+离子被氧化为Fe3+离子,NO3-离子被还原为NO气体,反应的离子方程式为:3Fe2++NO3-+4H+=3Fe3++NO↑+2H2O,E中NaAlO2,沉淀G为氢氧化铝,偏铝酸根离子与二氧化碳反应生成氢氧化铝沉淀,反应的离子方程式为:AlO2-+CO2+2H2O=Al(OH)3↓+HCO3-,
故答案为:3Fe2++4H++NO3-=3Fe3++NO↑+2H2O;AlO2-+CO2+2H2O=Al(OH)3↓+HCO3;
(3)由图象可知,沉淀溶解需要氢氧化钠的体积为2.5mL,那么物质的量为:0.0025L×4mol/L=0.01mol,即铝离子的物质的量为0.01mol;沉淀铝离子,需要氢氧化钠为0.03mol,即沉淀铁离子,需要氢氧化钠为(55-7.5-10)×-3×4mol/L=0.15mol,故铁离子为:0.05mol,无色气体A体积为224mL,即物质的量为:
| 0.224L |
| 22.4L/mol |
| 18.64g |
| 233g/mol |
点评:本题考查了常见阴阳离子的检验、无机推断,题目难度中等,注意掌握常见离子的性质及检验方法,(3)为难点、易错点,注意溶液电中性知识在化学计算中的应用方法,试题充分考查了学生的分析、理解能力及灵活应用所学知识的能力.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
氯仿(CHCl3)未密封保存,在空气中会发生2CHCl3+O2=2COCl2+2HCl生成剧毒的光气(COCl2).氯仿发生的反应属于( )
| A、取代反应 | B、置换反应 |
| C、氧化反应 | D、加成反应 |
下列各溶液的叙述中不正确的是( )
A、等pH的硫酸与醋酸稀释后pH的变化如图所示,则曲线Ⅱ表示的是醋酸的稀释图象 |
| B、容有等物质的量的NaClO、NaHCO3的溶液中:c(HClO)+c(ClO-)=c(HCO3-)+c(H2CO3)+c(CO32-) |
| C、若NH4HCO3溶液、NH4HSO4溶液中c(NH4+)相等,则c(NH4HSO4)<c(NH4HCO3) |
| D、已知某温度下Ksp(CH3COOAg)=2.8×10-3,浓度均为0.1mol?L-1的AgNO3溶液和CH3COONa溶液等体积混合一定能产生CH3COOAg沉淀 |
根据酸碱质子理论,凡是能给出质子的分子或离子都是酸,凡是能结合质子的分子或离子都是碱.按照这个理论,下列微粒属于两性物质的是( )
| A、HCO3- |
| B、CO32- |
| C、Fe(OH)3 |
| D、CH3COOH |
已知:A(g)+2B(g)═2C(g)△H=-Q kJ/mol (Q>0),在恒容的密闭容器中充入1mol A和2mol B,在一定条件下反应.下列有关说法正确的是( )
| A、平衡前,随着反应的进行,容器内气体密度逐渐减小 |
| B、平衡时,该反应放出的热量为Q kJ |
| C、平衡后,再向容器中通入1mol 氦气,A的转化率增大 |
| D、平衡后,缩小容器体积,A的浓度增大 |
下列有关物质的性质与应用不相对应的是( )
| A、SO2具有氧化性,可用于漂白纸浆 |
| B、FeCl3溶液能与Cu反应,可用于蚀刻印刷电路 |
| C、明矾能水解生成Al(OH)3胶体,可用作净水剂 |
| D、Zn具有还原性和导电性,可用作锌锰干电池的负极材料 |
将如图中所示实验装置的K闭合,下列判断正确的是( )


| A、电子沿Zn→a→b→Cu路径流动 |
| B、Cu电极质量增加 |
| C、甲池与乙池中的溶液互换,闭合K,电流没有明显变化 |
| D、片刻后可观察到滤纸b点变红色 |
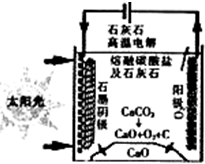 资源化利用二氧化碳不仅可减少温室气体的排放,还可重新获得燃料或重要工业产品.
资源化利用二氧化碳不仅可减少温室气体的排放,还可重新获得燃料或重要工业产品.