题目内容
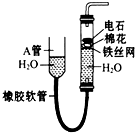 如图中的实验装置可用于制取乙炔.请填空:
如图中的实验装置可用于制取乙炔.请填空:(1)图中A管的作用是
(2)乙炔通入酸性KMnO4溶液中观察到的现象是
(3)乙炔通入溴的CCl4溶液中发生的化学反应类型是
(4)写出由乙炔合成聚氯乙烯的化学方程式:
考点:乙炔的性质实验
专题:
分析:(1)依据连通器原理可知,上下移动A管可以使右边的电石和水接触或分离,水与碳化钙反应生成氢氧化钙和乙炔;
(2)乙炔具有还原性能够发生氧化还原反应,还原酸性的高锰酸钾使其褪色;
(3)乙炔含有碳碳三键,能够与溴发生加成反应;
(4)乙炔与氯化氢发生加成反应生成氯乙烯,氯乙烯加成聚合生成聚氯乙烯.
(2)乙炔具有还原性能够发生氧化还原反应,还原酸性的高锰酸钾使其褪色;
(3)乙炔含有碳碳三键,能够与溴发生加成反应;
(4)乙炔与氯化氢发生加成反应生成氯乙烯,氯乙烯加成聚合生成聚氯乙烯.
解答:
解:(1)通过调节A管的高度,从而使右边的电石和水接触或分离,控制反应的发生和停止,水与碳化钙反应生成氢氧化钙和乙炔,方程式为:CaC2+2H2O→Ca(OH)2+C2H2↑;
故答案为:通过调节A管的高度,从而使右边的电石和水接触或分离,控制反应的发生和停止;CaC2+2H2O→Ca(OH)2+C2H2↑;
(2)乙炔具有还原性能够发生氧化还原反应,还原酸性的高锰酸钾使其褪色;
故答案为:酸性KMnO4溶液褪色;氧化反应;
(3)乙炔含有碳碳三键,能够与溴发生加成反应,化学方程式为:CH≡CH+2Br2→CHBr2-CHBr2;
故答案为加成,CH≡CH+2Br2→CHBr2-CHBr2;
(4)乙炔与氯化氢发生加成反应生成氯乙烯,氯乙烯加成聚合生成聚氯乙烯,化学方程式为:CH≡CH+HCl→CH2=CHCl,nCH2=CHCl
 ;
;
故答案为:CH≡CH+HCl→CH2=CHCl,nCH2=CHCl
 .
.
故答案为:通过调节A管的高度,从而使右边的电石和水接触或分离,控制反应的发生和停止;CaC2+2H2O→Ca(OH)2+C2H2↑;
(2)乙炔具有还原性能够发生氧化还原反应,还原酸性的高锰酸钾使其褪色;
故答案为:酸性KMnO4溶液褪色;氧化反应;
(3)乙炔含有碳碳三键,能够与溴发生加成反应,化学方程式为:CH≡CH+2Br2→CHBr2-CHBr2;
故答案为加成,CH≡CH+2Br2→CHBr2-CHBr2;
(4)乙炔与氯化氢发生加成反应生成氯乙烯,氯乙烯加成聚合生成聚氯乙烯,化学方程式为:CH≡CH+HCl→CH2=CHCl,nCH2=CHCl
| 引发剂 |
 ;
;故答案为:CH≡CH+HCl→CH2=CHCl,nCH2=CHCl
| 引发剂 |
 .
.
点评:本题考查乙炔的实验室制法及其性质,侧重基础知识的考查,有利于培养学生的分析能力和实验能力,注意相关基础知识的积累,题目难度不大.

练习册系列答案
相关题目
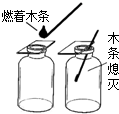 观察如图中的有关操作和现象,判断下列叙述正确的是( )
观察如图中的有关操作和现象,判断下列叙述正确的是( )| A、集气瓶中的气体可能是CO2 |
| B、集气瓶中的气体可能是空气 |
| C、集气瓶中的气体一定是O2 |
| D、集气瓶中的气体一定是N2 |
下列物质的转化在给定条件下能实现的是( )
①Al2O3
NaAlO2(aq)
Al(OH)3
②S
SO3
H2SO4
③NaHCO3溶液
NaHCO3
Na2CO3
④Fe2O3
FeCl3(aq)
无水FeCl3
⑤MgCl2(aq)
Mg(OH)2
MgO.
①Al2O3
| NaOH(aq) |
| △ |
| CO2 |
②S
| O2/点燃 |
| H2O |
③NaHCO3溶液
| 蒸干 |
| △ |
④Fe2O3
| HCl(aq) |
| △ |
⑤MgCl2(aq)
| 石灰乳 |
| 煅烧 |
| A、①③⑤ | B、②③④ |
| C、②④⑤ | D、①④⑤ |
下列说法不正确的是( )
| A、硫粉在过量的纯氧中燃烧可以生成大量的SO2 |
| B、可以用品红溶液鉴别SO2和CO2 |
| C、SO2能使品红溶液、酸性KMnO4溶液褪色,但褪色原理不同 |
| D、少量SO2通过CaCl2的溶液能生成白色沉淀 |
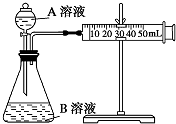 甲、乙两个实验小组利用KMnO4酸性溶液与H2C2O4溶液反应研究影响反应速率的因素.
甲、乙两个实验小组利用KMnO4酸性溶液与H2C2O4溶液反应研究影响反应速率的因素.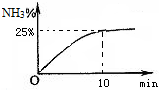 含氮化合物对人类生活有十分重大的意义.
含氮化合物对人类生活有十分重大的意义.