题目内容
氮的单质有N2、N4(标准状况下是气体)、N30等,NA表示阿伏加德罗常数.下列说法正确的是( )
| A、N2、N4、N30是同分异构体 |
| B、相同质量的N2、N4、N30含有的分子数相同 |
| C、N2、N4、N30分子中的化学键只有共价键 |
| D、2.24L N2和1.12L N4中所含有的氮原子数都是0.2NA |
考点:同素异形体,阿伏加德罗常数,不同晶体的结构微粒及微粒间作用力的区别
专题:化学键与晶体结构,化学反应速率专题
分析:A.相同元素组成,不同形态的单质互为同素异形体;
B.等质量时:分子数与摩尔质量成反比;
C.分子晶体中只含有共价键;
D.温度与压强未知,故无法计算氮原子数.
B.等质量时:分子数与摩尔质量成反比;
C.分子晶体中只含有共价键;
D.温度与压强未知,故无法计算氮原子数.
解答:
解:A.N2、N4、N30是由氮元素形成的不同单质,互为同素异形体,故A错误;
B.N2、N4、N30的摩尔质量不同,故相同质量的N2、N4、N30含有的分子数不同,故B错误;
C.N2、N4、N30都是非金属单质,故分子中的化学键只有共价键,故C正确;
D.温度与压强未知,故无法计算氮原子数,故D错误;
故选C.
B.N2、N4、N30的摩尔质量不同,故相同质量的N2、N4、N30含有的分子数不同,故B错误;
C.N2、N4、N30都是非金属单质,故分子中的化学键只有共价键,故C正确;
D.温度与压强未知,故无法计算氮原子数,故D错误;
故选C.
点评:本题考查同素异形体的概念、物质的量的相关计算、分子晶体及摩尔体积的应用,难度不大.要注意基础知识的积累.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
在配制物质的量浓度时,以下情况会使所配溶液浓度偏高的是( )
| A、定容时仰视刻度线 |
| B、未等溶液冷却至室温就进行定容 |
| C、转移溶液后,未洗涤烧杯和玻璃棒 |
| D、溶液在引流时溅出容器外 |
对下列有机反应类型的判断中不正确的是( )
A、CH3CH2OH+CH3COOH
| |||
B、CH2=CH2+HOCl
| |||
C、2CH3CH2OH+O2
| |||
D、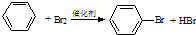 加成反应 加成反应 |
下列电离方程式错误的是( )
| A、(NH4 )2SO4=2NH4++SO42- |
| B、H2CO3=2H++CO32- |
| C、NaHCO3=Na++HCO3- HCO3-?H++CO32- |
| D、Ba(OH)2=Ba2++2OH- |
下列物质的酸性强弱比较正确的是( )
| A、HBrO4<HIO4 |
| B、H2SO4<H3PO4 |
| C、HClO3<HClO |
| D、H2SO4>H2SO3 |
若a g二氧化碳气体中含有b个电子 则阿伏伽德罗常数可以表示为( )
A、
| ||
B、
| ||
C、
| ||
D、
|
在甲烧杯中放入盐酸,乙烧杯中放入醋酸,两溶液的体积和pH都相等,向两烧杯中同时加入质量不等的锌粒,反应结束后得到等量的氢气.下列说法不正确的是( )
| A、反应开始时的速率:甲=乙 |
| B、反应所需的时间:甲>乙 |
| C、参加反应锌的质量:甲=乙 |
| D、两份酸溶液的物质的量浓度:甲>乙 |
下列说法不正确的是( )
| A、霾的形成与PM2.5有直接关系 |
| B、自行车钢架生锈主要是化学腐蚀所致 |
| C、用加热的方法杀死H7N9禽流感病毒是采用了蛋白质变性原理 |
| D、电子垃圾的回收利用,可减少对土壤和水源的污染 |
关于下列各装置图的叙述中,不正确的是( )
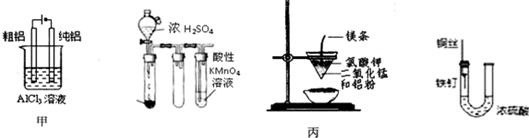

| A、用甲图装置电解精炼铝 |
| B、乙图中酸性KMnO4溶液中出现气泡,且颜色逐渐褪去 |
| C、丙图装置可制得金属锰,用同样的装置可制得金属铬 |
| D、丁图装置中的铁钉几乎没被腐蚀 |