题目内容
几种短周期元素的原子半径及主要化合价如下表:已知X是短周期中最活泼的金属,且与R同周期.下列叙述不正确的是( )
| 元素代号 | X | Y | Z | M | R |
| 原子半径/nm | 0.186 | 0.102 | 0.075 | 0.074 | 0.143 |
| 主要化合价 | +1 | +6-2 | +5-3 | -2 | +3 |
| A、离子半径大小:R3+<X+<M2- |
| B、Y与M组成的化合物是光化学烟雾的原因之一 |
| C、将YM2通入Ba(NO3)2溶液中有大量白色沉淀产生 |
| D、M氢化物的熔沸点高于Z氢化物的熔沸点 |
考点:原子结构与元素的性质
专题:
分析:Y和M的化合价都有-2价,应为周期表第ⅥA族元素,Y的最高价为+6价,应为S元素,M无正价,应为O元素;Z的化合价为+5、-3价,应为周期表第ⅤA族,原子半径小于硫元素原子,故处于第二周期,为N元素;R的化合价为+3价,应为周期表第ⅢA族元素,R原子半径大于硫元素,为Al元素;X的化合价为+1价,应为周期表第ⅠA族元素,原子半径大于Al元素,处于第三周期,为Na元素,结合元素周期律及元素化合物性质知识解答该题.
解答:
解:Y和M的化合价都有-2价,应为周期表第ⅥA族元素,Y的最高价为+6价,应为S元素,M无正价,应为O元素;Z的化合价为+5、-3价,应为周期表第ⅤA族,原子半径小于硫元素原子,故处于第二周期,为N元素;R的化合价为+3价,应为周期表第ⅢA族元素,R原子半径大于硫元素,为Al元素;X的化合价为+1价,应为周期表第ⅠA族元素,原子半径大于Al元素,处于第三周期,为Na元素,
A.电子层结构相同核电荷数越大离子半径越小,电子层越多离子半径越大,故离子半径Al3+<Na+<O2-,故A正确;
B.Y与M组成的化合物二氧化硫,是形成酸雨的原因之一,不是光化学烟雾的原因之一,故B错误;
C.将SO2通入Ba(NO3)2溶液中,酸性条件下SO2被硝酸根离子氧化为硫酸根离子,所以能反应生成硫酸钡白色沉淀,故C正确;
D.M氢化物为水,Z的氢化物为氨气,水的熔沸点高于氨气的熔沸点,故D正确;
故选B.
A.电子层结构相同核电荷数越大离子半径越小,电子层越多离子半径越大,故离子半径Al3+<Na+<O2-,故A正确;
B.Y与M组成的化合物二氧化硫,是形成酸雨的原因之一,不是光化学烟雾的原因之一,故B错误;
C.将SO2通入Ba(NO3)2溶液中,酸性条件下SO2被硝酸根离子氧化为硫酸根离子,所以能反应生成硫酸钡白色沉淀,故C正确;
D.M氢化物为水,Z的氢化物为氨气,水的熔沸点高于氨气的熔沸点,故D正确;
故选B.
点评:本题考查元素位置结构和性质的关系及应用,题目难度中等,正确把握元素化合价、原子半径与元素性质的关系是解答该题的关键,注意元素周期律的递变规律的应用.

练习册系列答案
相关题目
常温下,向一定体积pH=12的Ba(OH)2溶液中,逐滴加入一定物质的量浓度的NaHSO4溶液,当溶液中的Ba2+恰好完全沉淀时,停止滴加,此时溶液pH=11.若反应后溶液的体积等于Ba(OH)2溶液与NaHSO4溶液体积之和,则所加入的NaHSO4溶液与Ba(OH)2溶液体积之比是( )
| A、1:4 | B、4:1 |
| C、1:9 | D、9:1 |
某些化学概念在逻辑上存在下图所示关系,则下列说法中正确的是:( )

| A、纯净物(B)与混合物(A)属于包含关系 |
| B、化合物(B)与氧化物(A)属于包含关系 |
| C、单质与化合物属于交叉关系 |
| D、氧化反应与化合反应属于并列关系 |
下列说法中正确的是( )
| A、1mol任何纯净物都含有相同的原子数 |
| B、1molO2中约含有6.02×1023个氧分子 |
| C、1mol水中含有8mol电子 |
| D、阿伏加德罗常数就是6.02×1023mol-1 |
1998年诺贝尔化学奖授予科恩(美)和波普尔(英),以表彰他们在理论化学领域作出的重大贡献.他们的工作使实验和理论能够共同协力探讨分子体系的性质,引起整个化学领域正在经历一场革命性的变化.下列说法正确的是( )
| A、化学不做实验,就什么都不知道 |
| B、化学不再需要实验 |
| C、化学不再是纯实验科学 |
| D、未化学的方向是经验化 |
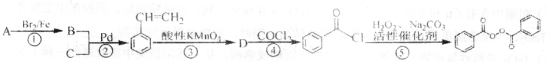
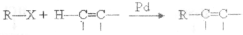
 ),在一定条件下能发生银镜反应,且1molE最多可得到4molAg;
),在一定条件下能发生银镜反应,且1molE最多可得到4molAg;