题目内容
(1)铝位于元素周期表第 周期 族,原子结构示意图为 电子排布式 自然界中的铝全部以 存在.
(2)写出氯水与溴化钠溶液反应的离子方程式
(3)浓硫酸与乙醇溶液加热反应,浓硫酸的作用是
(4)实验室制取氨气的化学方程式
(5)单质硅是常用做 的材料.
(6)高锰酸钾和乙醇放在一起容易发生 所以要分开房间存放.
(2)写出氯水与溴化钠溶液反应的离子方程式
(3)浓硫酸与乙醇溶液加热反应,浓硫酸的作用是
(4)实验室制取氨气的化学方程式
(5)单质硅是常用做
(6)高锰酸钾和乙醇放在一起容易发生
考点:氯气的化学性质,浓硫酸的性质,硅和二氧化硅,乙醇的化学性质,氨的制取和性质
专题:
分析:(1)铝位于元素周期表中位于第三周期第ⅢA族元素,原子结构示意图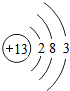 ,Al元素为13号元素,原子核外有13个电子,所以核外电子排布式为:1s22s22p63s23p1,自然界中的铝全部以铝土矿的形式存在;
,Al元素为13号元素,原子核外有13个电子,所以核外电子排布式为:1s22s22p63s23p1,自然界中的铝全部以铝土矿的形式存在;
(2)氯气通入溴化钠溶液是置换反应;
(3)浓硫酸与乙醇溶液加热反应,浓硫酸的作用是脱水剂和催化剂;
(4)根据盐碱的复分解反应确定方程式;
(5)硅单质常用作半导体材料、太阳能电池;
(6)高锰酸钾为强氧化剂,易氧化乙醇,而且乙醇有可燃性.
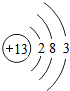 ,Al元素为13号元素,原子核外有13个电子,所以核外电子排布式为:1s22s22p63s23p1,自然界中的铝全部以铝土矿的形式存在;
,Al元素为13号元素,原子核外有13个电子,所以核外电子排布式为:1s22s22p63s23p1,自然界中的铝全部以铝土矿的形式存在;(2)氯气通入溴化钠溶液是置换反应;
(3)浓硫酸与乙醇溶液加热反应,浓硫酸的作用是脱水剂和催化剂;
(4)根据盐碱的复分解反应确定方程式;
(5)硅单质常用作半导体材料、太阳能电池;
(6)高锰酸钾为强氧化剂,易氧化乙醇,而且乙醇有可燃性.
解答:
解:(1)(1)铝位于元素周期表中位于第三周期第ⅢA族元素,原子结构示意图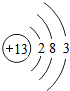 ,Al元素为13号元素,原子核外有13个电子,所以核外电子排布式为:1s22s22p63s23p1,自然界中的铝全部以铝土矿的形式存在,故答案为:三;ⅢA;1s22s22p63s23p1;铝土矿;
,Al元素为13号元素,原子核外有13个电子,所以核外电子排布式为:1s22s22p63s23p1,自然界中的铝全部以铝土矿的形式存在,故答案为:三;ⅢA;1s22s22p63s23p1;铝土矿;
(2)氯气通入溴化钠溶液是置换反应,2Br-+Cl2=Br2+2Cl-,故答案为:2Br-+Cl2=Br2+2Cl-;
(3)浓硫酸与乙醇溶液加热反应,浓硫酸的作用是脱水剂和催化剂,故答案为:脱水剂和催化剂;
(4)实验室制取氨气的化学方程式:2NH4Cl+Ca(OH)2
CaCl2+2NH3↑+2H2O,故答案为:2NH4Cl+Ca(OH)2
CaCl2+2NH3↑+2H2O;
(5)硅单质常用作半导体材料、太阳能电池等,故答案为:半导体材料、太阳能电池;
(6)酒精和高锰酸钾混一起会发生火灾,故答案为:火灾.
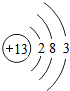 ,Al元素为13号元素,原子核外有13个电子,所以核外电子排布式为:1s22s22p63s23p1,自然界中的铝全部以铝土矿的形式存在,故答案为:三;ⅢA;1s22s22p63s23p1;铝土矿;
,Al元素为13号元素,原子核外有13个电子,所以核外电子排布式为:1s22s22p63s23p1,自然界中的铝全部以铝土矿的形式存在,故答案为:三;ⅢA;1s22s22p63s23p1;铝土矿;(2)氯气通入溴化钠溶液是置换反应,2Br-+Cl2=Br2+2Cl-,故答案为:2Br-+Cl2=Br2+2Cl-;
(3)浓硫酸与乙醇溶液加热反应,浓硫酸的作用是脱水剂和催化剂,故答案为:脱水剂和催化剂;
(4)实验室制取氨气的化学方程式:2NH4Cl+Ca(OH)2
| ||
| ||
(5)硅单质常用作半导体材料、太阳能电池等,故答案为:半导体材料、太阳能电池;
(6)酒精和高锰酸钾混一起会发生火灾,故答案为:火灾.
点评:本题考查元素在元素周期表中位置、核外最子排布、离子方程式和化学方程式的书写,以及物质的应用,综合性强,但比较容易.

练习册系列答案
 课课优能力培优100分系列答案
课课优能力培优100分系列答案 优百分课时互动系列答案
优百分课时互动系列答案
相关题目
下列说法正确的是( )
| A、已知20℃时,KNO3的溶解度为31.6g.则20℃时KNO3饱和溶液的质量分数等于31.6% |
| B、1mol/L的食盐溶液中含有58.5gNaCl |
| C、所有物质的溶解度随着温度的升高而上升 |
| D、实验室需要230mL 0.1mol/L的H2SO4溶液,应选用250mL容量瓶配制 |
下列物质属于纯净物的是( )
| A、氯化钠 | B、氨水 |
| C、漂白粉 | D、碘酒 |
设NA为阿伏加德罗常数的值,下列叙述正确的是( )
| A、标准状况下,11.2 L Cl2通入含0.5molFeBr2的溶液中转移电子数为1.5NA |
| B、0.1 mol?L-1的AlCl3溶液与足量NaOH溶液反应所得产物中含AlO2-为0.1NA |
| C、足量Zn与浓硫酸共热可生成标准状况下的气体2.24 L,则参加反应的硫酸为0.4 NA |
| D、常温常压下,5.6g环丙烷和聚乙烯的混合物中含有的碳原子数为0.4NA |
几种短周期元素的原子半径及主要化合价如下表:已知X是短周期中最活泼的金属,且与R同周期.下列叙述不正确的是( )
| 元素代号 | X | Y | Z | M | R |
| 原子半径/nm | 0.186 | 0.102 | 0.075 | 0.074 | 0.143 |
| 主要化合价 | +1 | +6-2 | +5-3 | -2 | +3 |
| A、离子半径大小:R3+<X+<M2- |
| B、Y与M组成的化合物是光化学烟雾的原因之一 |
| C、将YM2通入Ba(NO3)2溶液中有大量白色沉淀产生 |
| D、M氢化物的熔沸点高于Z氢化物的熔沸点 |
某实验兴趣小组用0.1000mol/L的标准盐酸溶液测定未知NaOH溶液,进行了4次中和滴定,数据如下:该待测NaOH的浓度为( )
| 实验序号 | 待测液数据/mL | 标准液数据/mL | ||
| 滴定前 | 滴定后 | 取用前 | 取用后 | |
| 1 | 0.10 | 20.10 | 0.00 | 20.00 |
| 2 | 0.80 | 22.60 | 0.00 | 20.00 |
| 3 | 0.40 | 20.20 | 0.00 | 20.00 |
| 4 | 1.20 | 21.40 | 0.00 | 20.00 |
| A、0.1000 mol/L |
| B、0.0978 mol/L |
| C、0.9780 mol/L |
| D、0.1020 mol/L |
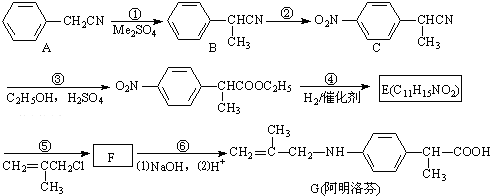
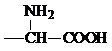 ②含有对位二取代苯环
②含有对位二取代苯环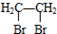
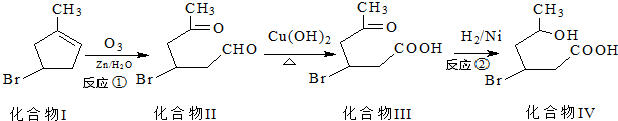
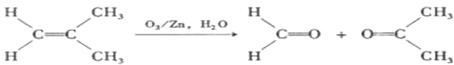
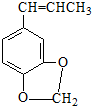 )发生类似反应①的反应,得到乙醛和化合物Y,Y的结构简式为
)发生类似反应①的反应,得到乙醛和化合物Y,Y的结构简式为