题目内容
6.常温下,将0.1mol/LHA溶液与0.1 mol/L的NaOH溶液 等体积混合后,溶液的pH为8,则c(Na+)-c(A-)=(9.9×10-7)mol/L(精确计算).分析 等体积混合后生成NaA,溶液的pH为8,可知水解显碱性,结合电荷守恒可知c(Na+)+c(H+)=c(A-)+c(OH-),则c(Na+)-c(A-)=c(OH-)-c(H+),以此来解答.
解答 解:常温下,Kw=1×10-14,溶液的pH为8,可知水解显碱性,c(OH-)=10-6mol/L,c(H+)=10-8mol/L,
由电荷守恒可知c(Na+)+c(H+)=c(A-)+c(OH-),则c(Na+)-c(A-)=c(OH-)-c(H+)=10-6mol/L-10-8mol/L═9.9×10-7 mol/L,
故答案为:9.9×10-7.
点评 本题考查酸碱混合的计算,为高频考点,把握水解生成氢氧根离子的浓度、电荷守恒为解答的关键,侧重分析与计算能力的考查,注意kw的应用,题目难度不大.

练习册系列答案
 53随堂测系列答案
53随堂测系列答案
相关题目
16.下列关于有机物的说法正确的是( )
| A. | 制备CH3CHCl2:乙烷在光照条件下和氯气反应或乙烯和氯水反应 | |
| B. | 沸点和在水中的溶解度:乙醇大于乙烷 | |
| C. | 鉴别溴苯和CCl4:硝酸银溶液 | |
| D. | 除去乙酸乙酯中混有的乙酸和乙醇:NaOH溶液 |
17.下列做法或操作中正确的是( )
①做实验时可用手直接拿取金属钠
②夜间发生厨房煤气泄漏,应立即开灯检查煤气泄漏的原因,并打开所有门窗通风
③不慎将浓H2SO4沾在皮肤上,立即用NaOH溶液冲洗
④进行SO2性质实验时要在通风橱内进行,多余的SO2一律排到室外.
①做实验时可用手直接拿取金属钠
②夜间发生厨房煤气泄漏,应立即开灯检查煤气泄漏的原因,并打开所有门窗通风
③不慎将浓H2SO4沾在皮肤上,立即用NaOH溶液冲洗
④进行SO2性质实验时要在通风橱内进行,多余的SO2一律排到室外.
| A. | ①③④ | B. | ①②③ | C. | ②③④ | D. | ①②③④ |
14.下列各组溶液只用试管和胶头滴管就可以鉴别的是( )
①AlCl3溶液和NaOH溶液
②Ca(HCO3)2溶液和NaOH
③NaAlO2溶液和NaHSO4溶液
④Al2(SO4)3和氨水
⑤AgNO3溶液和氨水.
①AlCl3溶液和NaOH溶液
②Ca(HCO3)2溶液和NaOH
③NaAlO2溶液和NaHSO4溶液
④Al2(SO4)3和氨水
⑤AgNO3溶液和氨水.
| A. | ①③⑤ | B. | ①②③ | C. | ②③④ | D. | ③④⑤ |
1.下列物质能水解,且水解产物都有葡萄糖的是( )
①蔗糖
②果糖
③淀粉
④纤维素.
①蔗糖
②果糖
③淀粉
④纤维素.
| A. | ①②③④ | B. | ②③④ | C. | ①③④ | D. | ③④ |
11.化学与生产、生活密切相关.下列说法中不正确的是( )
| A. | 使用含有氯化钙的融雪剂会加速桥梁的腐蚀 | |
| B. | 雾霾是一种分散系,N95活性炭口罩可用于防霾,其原理是吸附作用 | |
| C. | 大力推广使用煤的液化、气化技术,能减少二氧化碳的排放 | |
| D. | 晶体硅制得的光电池,能直接将光能转化为电能 |
18.锌铜原电池装置如图所示,其中阳离子交换膜只允许阳离子和水分子通过,下列有关叙述正确的是( )
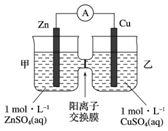

| A. | 锌电极上发生还原反应 | |
| B. | 电池工作一段时间后,甲池的 c(SO42-)不变 | |
| C. | 电池工作一段时间后,乙池溶液的总质量减少 | |
| D. | 阴阳离子分别通过交换膜向负极和正极移动,保持溶液中电荷平衡 |
11.能正确表示下列反应的离子方程式的是( )
| A. | 用浓盐酸酸化的KMnO4溶液与H2O2反应,证明H2O2具有还原性:2MnO4-+6H++5H2O2═2Mn2++5O2↑+8H2O | |
| B. | 向次氯酸钙溶液通入过量CO2:Ca2++2ClO-+CO2+H2O═CaCO3↓+2HClO | |
| C. | 向次氯酸钙溶液通入SO2:Ca2++2ClO-+SO2+H2O═CaSO3↓+2HClO | |
| D. | FeBr2溶液与等物质的量的Cl2反应:2Fe2++2Br-+2Cl2═2Fe3++4Cl-+Br2 |