题目内容
16.下列关于有机物的说法正确的是( )| A. | 制备CH3CHCl2:乙烷在光照条件下和氯气反应或乙烯和氯水反应 | |
| B. | 沸点和在水中的溶解度:乙醇大于乙烷 | |
| C. | 鉴别溴苯和CCl4:硝酸银溶液 | |
| D. | 除去乙酸乙酯中混有的乙酸和乙醇:NaOH溶液 |
分析 A.乙烯和氯水反应生成CH2ClCH2Cl;
B.乙醇分子间可形成氢键;
C.二者都不溶于水,密度比水大,且与硝酸银不反应;
D.乙酸乙酯与氢氧化钠溶液反应.
解答 解:A.乙烯和氯水反应生成CH2ClCH2Cl,不能生成CH3CHCl2,故A错误;
B.乙醇分子间可形成氢键,且与水形成氢键,而乙烷为非极性分子,则沸点和在水中的溶解度:乙醇大于乙烷,故B正确;
C.二者都不溶于水,密度比水大,且与硝酸银不反应,不能用硝酸银溶液检验,故C错误;
D.乙酸乙酯与氢氧化钠溶液反应,应用饱和碳酸钠溶液除杂,故D错误.
故选B.
点评 本题综合考查有机物的结构和性质,为高频考点,侧重考查学生的分析能力,注意把握有机物的结构和官能团的性质,把握常见有机物的物理性质和化学性质,难度不大.

练习册系列答案
相关题目
15.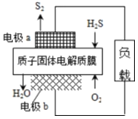 科学家设计出质子膜H2S燃料电池,实现了利用H2S废气资源回收能量并得到单质硫.质子膜H2S燃料电池的结构示意图如图所示.下列说法不正确的是( )
科学家设计出质子膜H2S燃料电池,实现了利用H2S废气资源回收能量并得到单质硫.质子膜H2S燃料电池的结构示意图如图所示.下列说法不正确的是( )
 科学家设计出质子膜H2S燃料电池,实现了利用H2S废气资源回收能量并得到单质硫.质子膜H2S燃料电池的结构示意图如图所示.下列说法不正确的是( )
科学家设计出质子膜H2S燃料电池,实现了利用H2S废气资源回收能量并得到单质硫.质子膜H2S燃料电池的结构示意图如图所示.下列说法不正确的是( )| A. | 电极a为电池的负极 | |
| B. | 电极b上发生的电极反应为:O2+4H++4e-═2H2O | |
| C. | 电路中每流过4 mol电子,在正极消耗44.8LH2S | |
| D. | 每17 g H2S参与反应,有1 mol H+经质子膜进入正极区 |
16.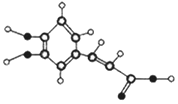 咖啡中的咖啡酸具有抗氧化、抗炎、抗粥样硬化等多种有益作用.其球棍模型如图所示,关于咖啡酸的下列说法正确的是( )
咖啡中的咖啡酸具有抗氧化、抗炎、抗粥样硬化等多种有益作用.其球棍模型如图所示,关于咖啡酸的下列说法正确的是( )
 咖啡中的咖啡酸具有抗氧化、抗炎、抗粥样硬化等多种有益作用.其球棍模型如图所示,关于咖啡酸的下列说法正确的是( )
咖啡中的咖啡酸具有抗氧化、抗炎、抗粥样硬化等多种有益作用.其球棍模型如图所示,关于咖啡酸的下列说法正确的是( )| A. | 分子式为C9H10O4 | |
| B. | 分子中至少有9个碳原子共平面 | |
| C. | 1 mol咖啡酸与足量NaHCO3反应生1 mol CO2 | |
| D. | 1 mol咖啡酸最多能够与5 mol H2发生加成反应 |
4.在给定条件下,下列选项所示的物质间转化均能实现的是( )
| A. | S$\stackrel{O_{2}、点燃}{→}$SO3$\stackrel{H_{2}O}{→}$H2SO4 | |
| B. | H2SO4(稀)$\stackrel{Cu}{→}$SO2$\stackrel{BaCl_{2}}{→}$BaSO4 | |
| C. | Fe2O3$\stackrel{盐酸}{→}$FeCl3(ap)$\stackrel{蒸发}{→}$无水FeCl3 | |
| D. | SiO2$\stackrel{NaOH}{→}$NaSiO3$\stackrel{HCl}{→}$H2SiO3 |
11.能用勒夏特列原理解释的是( )
| A. | 煅烧粉碎的硫铁矿有利于SO2生成 | |
| B. | 由H2、I2、HI三种气体组成的平衡体系加压后颜色变深 | |
| C. | 使用铁触媒,有利于N2和H2的混合气体合成NH3 | |
| D. | 实验室常用排饱和和食盐水法收集Cl2 |
5.下列关于丙烯(CH3CH=CH2)的说法正确的是( )
| A. | 丙烯分子有6个δ键,1个π键 | |
| B. | 丙烯分子中3个碳原子都是sp3杂化 | |
| C. | 丙烯分子中既存在极性键又存在非极性键 | |
| D. | 丙烯分子中所有原子在同一平面上 |
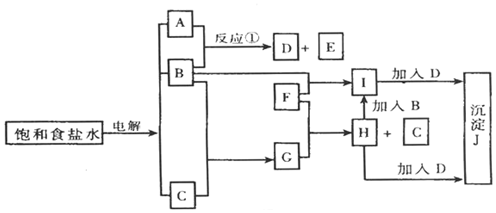
 ,G
,G ;
;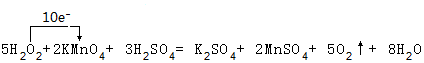 .
.