题目内容
14.浓度为0.1mol/L的醋酸溶液用水稀释后,下列说法错误的是( )| A. | 醋酸的电离度增大 | B. | H+数目增多 | ||
| C. | c(H+)增大 | D. | 导电性减弱 |
分析 醋酸是弱电解质,加水稀释醋酸溶液,促进醋酸电离,根据醋酸的电离程度确定溶液中微粒个数变化.
解答 解:A.醋酸是弱电解质,加水稀释醋酸溶液,促进醋酸电离,则醋酸的电离程度增大,故A正确;
B.加水稀释醋酸,促进醋酸电离,溶液中氢离子总数增多,故B正确;
C.加水稀释醋酸,虽然促进醋酸电离,但是溶液体积增大程度大于氢离子物质的量增大程度,所以c(H+)减小,故C错误;
D.加水稀释醋酸,虽然促进醋酸电离,溶液中离子个数增多,但离子浓度降低,所以导电能力减弱,故D正确;
故选C.
点评 本题考查弱电解质的电离,明确弱电解质电离特点是解本题关键,注意稀释醋酸时溶液中氢离子、醋酸分子、醋酸根离子浓度都减小,但氢氧根离子浓度增大,为易错点.

练习册系列答案
相关题目
4.下列实验能证明一定有二氧化硫存在的是( )
①能使澄清石灰水变浑浊;
②能使湿润的蓝色石蕊试纸变红;
③能使品红溶液褪色;
④通入足量的氢氧化钠溶液再加BaCl2溶液有白色沉淀产生,该沉淀溶于稀盐酸;
⑤通入气体能使溴水褪色,再滴加Ba(NO3)2溶液有白色沉淀产生.
①能使澄清石灰水变浑浊;
②能使湿润的蓝色石蕊试纸变红;
③能使品红溶液褪色;
④通入足量的氢氧化钠溶液再加BaCl2溶液有白色沉淀产生,该沉淀溶于稀盐酸;
⑤通入气体能使溴水褪色,再滴加Ba(NO3)2溶液有白色沉淀产生.
| A. | 只有⑤ | B. | 均能 | C. | ③④⑤ | D. | 均不能 |
5.下列有关实验装置及用途叙述完全正确的是( )
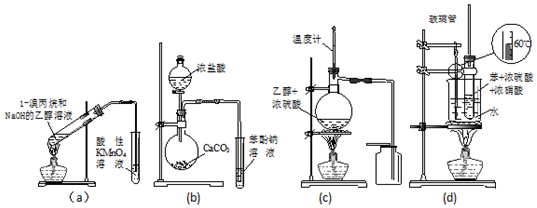

| A. | a装置直接用酸性KMnO4溶液检验消去反应的产物 | |
| B. | b装置检验酸性:盐酸>碳酸>苯酚 | |
| C. | c装置用于实验室制取并收集乙烯 | |
| D. | d装置用于实验室制硝基苯 |
9.卤族元素及其化合物在生活中应用广泛.下列有关说法正确的是( )
| A. | 氟氯烃作制冷剂会加剧雾霾天气的形成 | |
| B. | 从海水中提取溴需经历氧化还原反应 | |
| C. | 加碘食盐中含有碘元素,能使淀粉溶液变蓝 | |
| D. | 工业上制漂白粉,所得的氯化物都具有漂白性 |
3.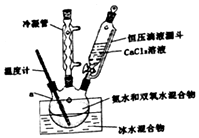 过氧化钙(CaO2)是一种白色结晶体粉末,极微溶于水,不溶于醇类、乙醚等,加热至150℃左右开始分解放出氧气,与水缓慢反应生成H2O2.易于酸反应生成H2O2
过氧化钙(CaO2)是一种白色结晶体粉末,极微溶于水,不溶于醇类、乙醚等,加热至150℃左右开始分解放出氧气,与水缓慢反应生成H2O2.易于酸反应生成H2O2
(Ⅰ)CaO2的制备原理:CaCl2+H2O2+2NH3•H2O+6H2O═CaO2•8H2O↓+2NH4Cl实验步骤如图、反应装置如图所示,请回答下列问题:
实验步骤:
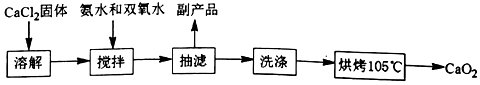
(1)仪器a的名称三颈烧瓶;
(2)①沉淀反应时常用冰水浴控制温度在0℃左右,其可能原因是减少H2O2受热分解;降低氨的挥发;降低温度促使产物析出(写出两点)
②过滤后洗涤沉淀的试剂最好用B.
A.热水 B.冷水 C.乙醇 D.乙醚
(3)某同学设计的实验装置示意图(如图,夹持装置及冷凝水省略)有一处不合理,请提出改进方案并说明理由温度计应该为搅拌器.该反应需要不断搅拌,且冰水浴条件无需温度计.
(Ⅱ)产品稳定性分析:取所得产品置于试剂瓶内保存一个月,并分别在放置前、放置后取一定质量的样品溶于水,加适量稀硫酸酸化,用0.1000mol•L-1酸性高锰酸钾溶液滴定生成H2O2(KMnO4反应后生成Mn2+),以此分析产品的稳定性,所得实验数据如表
已知:
①H2O2不稳定,加热,加入某些金属离子或加碱均有利于其分解.
②产品稳定性=$\frac{放置一个月后Ca{O}_{2}的质量分数}{放置前Ca{O}_{2}的质量分数}$×100%
(4)用KMnO4滴定,达到滴定终点时的现象是溶液由无色变淡紫色,且半分钟不褪色.
(5)该产品的“产品稳定性”=96%.
 过氧化钙(CaO2)是一种白色结晶体粉末,极微溶于水,不溶于醇类、乙醚等,加热至150℃左右开始分解放出氧气,与水缓慢反应生成H2O2.易于酸反应生成H2O2
过氧化钙(CaO2)是一种白色结晶体粉末,极微溶于水,不溶于醇类、乙醚等,加热至150℃左右开始分解放出氧气,与水缓慢反应生成H2O2.易于酸反应生成H2O2(Ⅰ)CaO2的制备原理:CaCl2+H2O2+2NH3•H2O+6H2O═CaO2•8H2O↓+2NH4Cl实验步骤如图、反应装置如图所示,请回答下列问题:
实验步骤:

(1)仪器a的名称三颈烧瓶;
(2)①沉淀反应时常用冰水浴控制温度在0℃左右,其可能原因是减少H2O2受热分解;降低氨的挥发;降低温度促使产物析出(写出两点)
②过滤后洗涤沉淀的试剂最好用B.
A.热水 B.冷水 C.乙醇 D.乙醚
(3)某同学设计的实验装置示意图(如图,夹持装置及冷凝水省略)有一处不合理,请提出改进方案并说明理由温度计应该为搅拌器.该反应需要不断搅拌,且冰水浴条件无需温度计.
(Ⅱ)产品稳定性分析:取所得产品置于试剂瓶内保存一个月,并分别在放置前、放置后取一定质量的样品溶于水,加适量稀硫酸酸化,用0.1000mol•L-1酸性高锰酸钾溶液滴定生成H2O2(KMnO4反应后生成Mn2+),以此分析产品的稳定性,所得实验数据如表
| 数据 时间 | 样品取用质量/(g) | 平均消耗体积(KMnO4)/mL |
| 放置前测定 | a | 25.00 |
| 放置一个月后测定 | a | 24.00 |
①H2O2不稳定,加热,加入某些金属离子或加碱均有利于其分解.
②产品稳定性=$\frac{放置一个月后Ca{O}_{2}的质量分数}{放置前Ca{O}_{2}的质量分数}$×100%
(4)用KMnO4滴定,达到滴定终点时的现象是溶液由无色变淡紫色,且半分钟不褪色.
(5)该产品的“产品稳定性”=96%.
5.下列叙述正确的是( )
| A. | 某溶液中加入硝酸银溶液时,生成白色沉淀,说明溶液中有Cl- | |
| B. | 某溶液中加入稀硫酸溶液时,生成无色气体,说明溶液中有CO32- | |
| C. | 某溶液中加入氯化钡溶液时,生成白色沉淀,说明溶液中有SO42- | |
| D. | 某溶液中加入盐酸溶液,无明显现象,再加入氯化钡溶液时,生成白色沉淀,说明溶液中有SO42- |
 ;
;