题目内容
6.普通泡沫灭火器的里面装着一只小塑料筒,塑料筒内盛装硫酸铝溶液,内筒和外筒之间盛装碳酸氢钠饱和溶液.使用时,倒置灭火器,两种药液相混合就会喷出含二氧化碳的白色泡沫.(1)产生此现象的离子方程式是Al3++3HCO3-=Al(OH)3↓+3CO2↑
(2)一般不用碳酸钠代替碳酸氢钠,是因为由1molCO32-转化为1molCO2需2molH+,H+由Al3+提供(水解),现因Al3+量不变,只能生成HCO3-,没有CO2,喷不出泡沫.(至少回答一点)
分析 (1)普通泡沫灭火器是碳酸氢钠和硫酸铝溶液混合发生双水解反应生成氢氧化铝沉淀和二氧化碳气体;
(2)碳酸根的水解是分步进行的,先水解得到碳酸氢根,进一步水解得到二氧化碳.
解答 解:(1)普通泡沫灭火器是碳酸氢钠和硫酸铝溶液混合发生双水解反应生成氢氧化铝沉淀和二氧化碳气体,反应的离子方程式为Al3++3HCO3-=Al(OH)3↓+3CO2↑,
故答案为:Al3++3HCO3-=Al(OH)3↓+3CO2↑;
(2)Al2(SO4)3溶液和NaHCO3溶液混合后会发生双水解反应,原理方程式为:Al2(SO4)3+6NaHCO3═2Al(OH)3↓+6CO2↑+3Na2SO4,Al2(SO4)3溶液和NaHCO3溶液的体积比约是1:6,由1mol的碳酸根离子转化为1molCO2需2molH+,H+由Al3+提供(水解),在Al3+量不变的情况下,碳酸根离子先水解得到碳酸氢根,只能生成HCO3-,没有CO2,喷不出泡沫,并且双水解时NaHCO3表面生成Al(OH)3后,会阻碍反应的进行,
故答案为:由1molCO32-转化为1molCO2需2molH+,H+由Al3+提供(水解),现因Al3+量不变,只能生成HCO3-,没有CO2,喷不出泡沫.
点评 本题考查了盐类水解的分析判断,溶液酸碱性分析理解,主要是盐类水解的应用,掌握基础是关键,题目较简单.

练习册系列答案
相关题目
16.如图所示的实验装置不能完成实验目的是( )
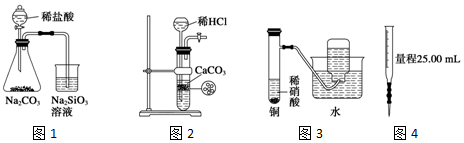

| A. | 图1为证明非金属性强弱:Cl>C>Si | |
| B. | 图2为制备少量CO2并控制反应 | |
| C. | 图3为制备并收集少量NO气体 | |
| D. | 图4量取0.10mol•L-1 KOH溶液20.00mL |
17.下列措施能提高合成氨[N2(g)+3H2(g)?2NH3(g)△H=-92.4kJ/mol]厂的生产效率和经济效益的是( )
①采用20MPa~50MPa的压强;
②使用催化剂;
③在合适的温度下进行反应;
④从平衡混合气体中液化分离出NH3,并将N2、H2循环使用.
①采用20MPa~50MPa的压强;
②使用催化剂;
③在合适的温度下进行反应;
④从平衡混合气体中液化分离出NH3,并将N2、H2循环使用.
| A. | ①③④ | B. | ③④ | C. | ①②③ | D. | 全部 |
14.浓度为0.1mol/L的醋酸溶液用水稀释后,下列说法错误的是( )
| A. | 醋酸的电离度增大 | B. | H+数目增多 | ||
| C. | c(H+)增大 | D. | 导电性减弱 |
1.下列物质的水溶液能导电,但属于弱电解质的是( )
| A. | CH3COOH | B. | C12 | C. | NH4HCO3 | D. | SO3 |
11.下列说法不正确的是( )
| A. | 高压钠灯常用于道路的照明 | B. | 饱和石灰水用来制漂白粉 | ||
| C. | 硅晶体用作半导体材料 | D. | 金属镁常用来制造信号弹和焰火 |
18.为了证明一水合氨(NH3•H2O)是弱电解质,常温下做以下实验没有意义的是( )
| A. | 用pH试纸测出0.010mol/L氨水的pH为10 | |
| B. | 用pH试纸测定0.10mol/LNH4Cl溶液为pH<7 | |
| C. | 取出10mL0.010mol/L氨水,滴入2滴酚酞溶液,显粉红色,再加入NH4C1晶体少量,颜色变浅 | |
| D. | 取出10mL0.010mol/L氨水,滴入2滴酚酞溶液,显粉红色,再稀盐酸少量,颜色变浅 |
15.根据官能团分类,下列物质中与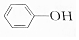 属于同一类物质的是( )
属于同一类物质的是( )
 属于同一类物质的是( )
属于同一类物质的是( )| A. | 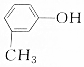 | B. | 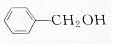 | C. | 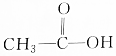 | D. | 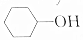 |
17.下列说法正确的是( )
| A. | NaCl溶于水电离出Na+和C1-,离子键发生断裂,属于化学变化 | |
| B. | 某晶体固态不导电,熔化时能导电,该晶体一定是离子晶体 | |
| C. | 干冰和水晶融化时,都克服分子间作用力 | |
| D. | PCl5、CO2、N2所有原子最外层都满足8电子结构 |