题目内容
14.下列离子在水溶液中能大量共存的是( )| A. | Na+、Cl-、HCO3-、Ca2+ | B. | OH-、Na+、Mg2+、HCO3- | ||
| C. | Na+、Cl-、H+、Ag+ | D. | Na+、SiO32-、H+、Cl- |
分析 根据离子之间不能结合生成沉淀、气体、水等,则离子大量共存,以此来解答.
解答 解:A.该组离子之间不反应,可大量共存,故A正确;
B.OH-、Mg2+结合生成沉淀,OH-、HCO3-结合生成水和碳酸根离子,不能共存,故B错误;
C.Cl-、Ag+结合生成沉淀,不能共存,故C错误;
D.SiO32-、H+结合生成沉淀,不能共存,故D错误;
故选A.
点评 本题考查离子的共存,为高频考点,把握常见离子之间的反应为解答的关键,侧重复分解反应的离子共存考查,题目难度不大.

练习册系列答案
相关题目
12.下图实验方案能达到实验目的是( )
| A. | 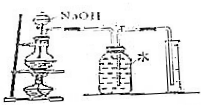 测定氨盐纯度 | B. | 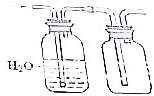 除去NO2并收集NO | ||
| C. | 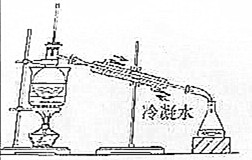 分离四氯化碳和二氯甲烷 | D. | 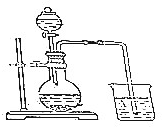 验证中和反应是放热反应 |
2.下列解释事实的方程式不正确的是( )
| A. | 室温下,测得0.1 mol/L 的氨水的pH为11:NH3•H2O?NH4++OH- | |
| B. | 酸性介质中KMnO4氧化H2O2:2MnO4-+5H2O2+6H+═2Mn2++5O2↑+8H2O | |
| C. | 向 NaAlO2溶液中通入过量CO2 制 Al(OH)3:CO2+AlO2-+2H20=HC03-+Al(OH)3↓ | |
| D. | 铅酸蓄电池在充电时的正极反应:PbO2+4H++SO42-+2e-═PbSO4+2H2O |
9.将4mol A气体和2mol B气体在2L固定体积的容器中混合,并在一定条件下发生如下反应:2A(g)+B(g)?2C(g).若经2s后测得C的浓度为0.6mol•L-1,现有下列几种说法,其中正确的是( )
| A. | 用物质A表示的反应的平均速率为0.6 mol•(L•s)-1 | |
| B. | 2 s时物质B的浓度为1.4 mol•L-1 | |
| C. | 2 s时物质A的转化率为70% | |
| D. | 2 s时物质A的体积分数为$\frac{14}{27}$ |
19.下列说法正确的是( )
| A. | 煤中存在苯、二甲苯,工业上可由煤蒸馏获得 | |
| B. | 直馏汽油和裂化汽油中分别加入溴的四氯化碳溶液均能发生化学反应 | |
| C. | 石油的裂化、裂解和煤的干馏、气化都属于化学变化 | |
| D. | 石油裂解是生产乙烯的主要方法,乙烯和聚乙烯均能使溴水发生反应而褪色 |
6.对K2CO3分类,不正确的是( )
| A. | 属于钾盐 | B. | 属于碳酸盐 | C. | 属于正盐 | D. | 属于酸式盐 |
3.氢氧电池以氢气作还原剂,氧气作氧化剂,电极为多孔镍,电解质溶液为30%的氢氧化钾溶液.以下有数种说法,其正确的组合是( )
①负极反应为O2+2H2O+4e-=4OH-
②负极反应为2H2+4OH--4e-=4H2O
③电池工作时正极区pH升高,负极区pH下降;
④电池工作时溶液中的阴离子移向正极.
①负极反应为O2+2H2O+4e-=4OH-
②负极反应为2H2+4OH--4e-=4H2O
③电池工作时正极区pH升高,负极区pH下降;
④电池工作时溶液中的阴离子移向正极.
| A. | ①③④ | B. | ②③ | C. | ②④ | D. | ①④ |
4.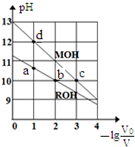 常温下,向体积均为V0、浓度均为c mol•L-1的MOH和ROH溶液中分别加水稀释至体积为V,溶液pH随-1g$\frac{{V}_{0}}{V}$的变化如图所示.下列叙述正确的是( )
常温下,向体积均为V0、浓度均为c mol•L-1的MOH和ROH溶液中分别加水稀释至体积为V,溶液pH随-1g$\frac{{V}_{0}}{V}$的变化如图所示.下列叙述正确的是( )
 常温下,向体积均为V0、浓度均为c mol•L-1的MOH和ROH溶液中分别加水稀释至体积为V,溶液pH随-1g$\frac{{V}_{0}}{V}$的变化如图所示.下列叙述正确的是( )
常温下,向体积均为V0、浓度均为c mol•L-1的MOH和ROH溶液中分别加水稀释至体积为V,溶液pH随-1g$\frac{{V}_{0}}{V}$的变化如图所示.下列叙述正确的是( )| A. | 碱性:MOH>ROH | |
| B. | b、c两点的溶液中:c(R+)>c(M+) | |
| C. | 溶液中水的电离程度α:αc>αb>αa>αd | |
| D. | c>0.1 |
