题目内容
Al粉投入某无色澄清的溶液中产生H2,则下列离子组合正确的是( )
| A、H+、Ca2+、Na+、CO32- |
| B、Na+、Mg2+、Al3+、Cl- |
| C、Cu2+、Mg2+、Cl-、OH- |
| D、Ba2+、Cl-、OH-、NO3- |
考点:离子共存问题
专题:
分析:Al粉投入某无色澄清的溶液中产生H2,为非氧化性酸或强碱溶液,根据离子之间不能结合生成沉淀、气体、水、弱电解质等,则离子大量共存,并结合离子的颜色来解答.
解答:
解:Al粉投入某无色澄清的溶液中产生H2,为非氧化性酸或强碱溶液,
A.Ca2+、CO32-结合生成沉淀,H+、CO32-结合生成水和气体,不能大量共存,故A不选;
B.碱性溶液中不能大量存在Mg2+、Al3+,酸性溶液中该组离子之间不反应,可大量共存,且离子均为无色,故B选;
C.Cu2+、Mg2+分别与OH-结合生成沉淀,且Cu2+为蓝色,与无色不符,故C不选;
D.碱性溶液中该组离子之间不反应,可大量共存,且离子均为无色,故D选;
故选BD.
A.Ca2+、CO32-结合生成沉淀,H+、CO32-结合生成水和气体,不能大量共存,故A不选;
B.碱性溶液中不能大量存在Mg2+、Al3+,酸性溶液中该组离子之间不反应,可大量共存,且离子均为无色,故B选;
C.Cu2+、Mg2+分别与OH-结合生成沉淀,且Cu2+为蓝色,与无色不符,故C不选;
D.碱性溶液中该组离子之间不反应,可大量共存,且离子均为无色,故D选;
故选BD.
点评:本题考查离子的共存,为高频考点,把握习题中的信息及常见离子之间的反应为解答的关键,侧重复分解反应的离子共存考查,注意常见离子的颜色,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
某有机化合物的结构简式为: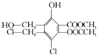 ,下列有关该物质的叙述正确的是( )
,下列有关该物质的叙述正确的是( )
 ,下列有关该物质的叙述正确的是( )
,下列有关该物质的叙述正确的是( )| A、1mol该物质最多可以消耗3 mol Na |
| B、1mol该物质最多可以消耗7 mol NaOH |
| C、不能与Na2CO3溶液反应 |
| D、易溶于水,可以发生加成反应和取代反应 |
 常温下,向10mL 0.1mol?L-1 NaOH溶液中逐滴加入0.1mol?L-1的CH3COOH溶液,其pH逐渐减小,图中a、b、c三点的pH为实验中所测得.下列有关说法中一定正确的是( )
常温下,向10mL 0.1mol?L-1 NaOH溶液中逐滴加入0.1mol?L-1的CH3COOH溶液,其pH逐渐减小,图中a、b、c三点的pH为实验中所测得.下列有关说法中一定正确的是( )| A、当7<pH<13时,溶液中c(Na+)>c(CH3COO-)>c(OH-)>c(H+) |
| B、当pH=7时,所加CH3COOH溶液的体积为10 mL |
| C、当5<pH<7时,溶液中c(CH3COO-)>c(Na+) |
| D、继续滴加0.1 mol?L-1的CH3COOH溶液,溶液的pH最终可以变化至1 |
C6H14的各种同分异构体中,所含甲基数和它的一氯取代物的数目与下列相等的是( )
| A、2个-CH3,能生成6种一氯代物 |
| B、3个-CH3,能生成4种一氯代物 |
| C、2个-CH3,能生成5种一氯代物 |
| D、4个-CH3,能生成4种一氯代物 |
下列粒子在溶液中能大量共存的是( )
| A、K+、NO3-、I-、H2SO3 |
| B、Na+、Fe3+、NO3-、CO32- |
| C、Al3+、NO3-、SO32-、OH- |
| D、NH4+、Na+、SO42-、CH3COOH |
在一定温度下,A2(g)+B2(g)?2AB(g)达到平衡的标志是( )
| A、单位时间内减少n mol A2,同时生成2n mol AB |
| B、单位时间内生成n mol B2,同时生成n mol AB |
| C、单位时间内生成 2xmol AB,同时生成xmol A2 |
| D、容器内各组成成分的物质的量之和不随时间变化而变化 |
 一定温度下,将1molM和1molN气体充入2L恒容密闭容器,发生反应M(g)+N(g)?xP(g)+Q(s),t1时达到平衡.在t2、t3时刻分别改变反应的一个条件,测得容器中气体P的浓度随时间变化如图所示.下列说法正确的是( )
一定温度下,将1molM和1molN气体充入2L恒容密闭容器,发生反应M(g)+N(g)?xP(g)+Q(s),t1时达到平衡.在t2、t3时刻分别改变反应的一个条件,测得容器中气体P的浓度随时间变化如图所示.下列说法正确的是( )| A、反应方程式中的x=1 |
| B、t2时刻改变的条件是使用催化剂 |
| C、t3时刻改变的条件是移去少量物质Q |
| D、t1~t3间该反应的平衡常数均为4 |
化学与生产生活、环境保护、资利用、能开发等密切相关.下列说法错误的是( )
| A、煤炭经气化、液化和干馏等过程,可以转化为清洁能 |
| B、利用二氧化碳制造全降解塑料,可以缓解温室效应 |
| C、利用生物方法脱除生活污水中的氮和磷,防止水体富营养化 |
| D、高纯硅广泛应用于太阳能电池、计算机芯片和光导纤维 |
下列物质中,只含有离子键的是( )
| A、H2O |
| B、CO2 |
| C、MgCl2 |
| D、KOH |